Clear Sky Science · he
חקר המנגנונים המולקולריים של עמידות לאמינוקוליקוזידים ב-Escherichia coli MG1655 באמצעות צלחת הגידול לעמידות לאנטיביוטיקה
מדוע פתוגנים שמשתנים במהירות חשובים לכולם
התרופות האנטי‑ביוטיות הצילו חיים רבים, אך החיידקים מתאימים עצמם בהדרגה לדרכים לעקוף אותן. מאמר זה בוחן כיצד חיידקי המעי השכיחים, Escherichia coli, יכולים להתפתח לעמידות כנגד אנטיביוטיקה נפוצה, גנטמיצין, בתוך יום–יומיים בלבד. על ידי צפייה בהתפתחות העמידות על צלחת גידול שעוצבה במיוחד ולאחר מכן חקירת ה‑DNA והמבנים המולקולריים של החיידקים, החוקרים מגלים פרטים חדשים על הדרכים שבהן המיקרובים מתחכמים לתרופה. ממצאיהם מסבירים מדוע העמידות יכולה להופיע במהירות ומצביעים על כלים שיכולים לחזות אילו טיפולים צפויים להיכשל.
צלחת חדשה לצפייה באבולוציה בפעולה
כדי להמחיש את הופעת העמידות, הצוות בנה מה שהם קוראים לו צלחת גידול לעמידות לאנטיביוטיקה (ARGP). דמיינו צלחת פטרי המחולקת לשלושה טבעות עגולות: ללא תרופה במרכז, מנה בינונית בטבעת האמצעית ומנה מאוד גבוהה בקצה החיצוני. הם זרעו במרכז זן סטנדרטי הרגיש לתרופה של E. coli ואפשרו לחיידקים לשחות החוצה דרך שכבה דקה וחצי‑מוצקה. כאשר המיקרובים התפשטו הם נתקלו ברמות גנטמיצין הולכות וגדלות. רובם נעצרו בגבולות בין האזורים, אך מדי פעם נוצרו ניצנים קטנים שהצליחו לעבור לטבעת הבאה ולהמשיך לגדול. בתוך יומיים–שלושה בלבד, כמה שושלות שגשגו בריכוזי אנטיביוטיקה גבוהים בעשר פעמים מהמינימום שעמד במקור לעצור את הזן המקורי. 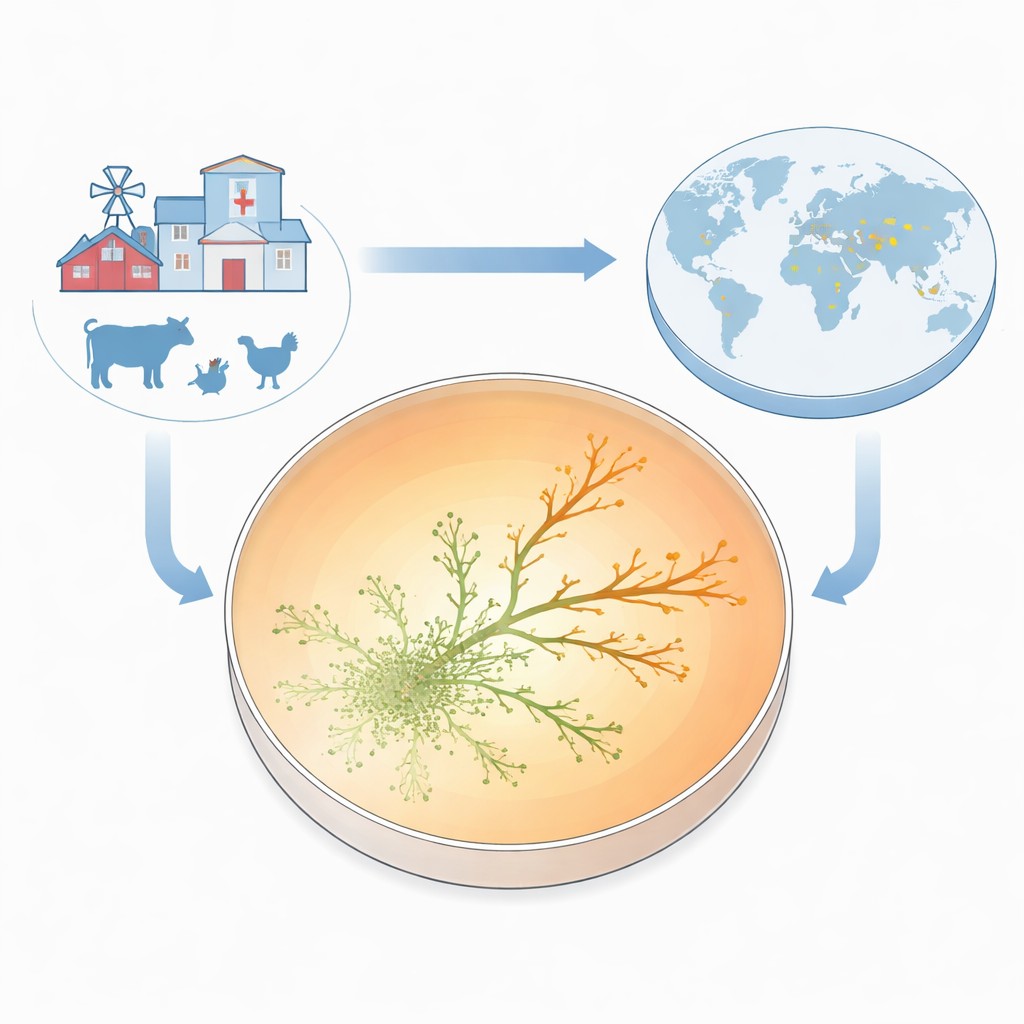
מעקב אחר השינויים הגנטיים מאחורי ההישרדות
הופעת מושבות עמידות היתה רק ההתחלה. המדענים אספו תאים מהניצנים הקשוחים הללו והשוו את רצף ה‑DNA המלא שלהם לזה של הזן המקורי. לאחר סינון קפדני של ארטיפקטים וקטעי זיהום, הם התמקדו בשינויים בגנים הידועים כמעורים בהפקת חלבונים בתוך התא. הם מצאו מוטציות בחלקים של הקוד הגנטי שמרכיבים את מכונת הסינתזה של החלבון: מספר עותקים של גן ה‑16S rRNA, וגן בשם fusA, שמקודד לחלבון מסייע מרכזי הידוע כ‑EF‑G. שני היעדים האלה הגיוניים מכיוון שגנטמיצין פועל על ידי הידוק אליו לריבוזום החיידקי, המורכב שקורא הוראות גנטיות ומרכיב חלבונים חדשים. כל כוונון שמשנה את המכונה הזו מבלי לשבור אותה לגמרי עשוי להחליש את השפעת התרופה.
איך שינוי יחיד בציר מרכך את יעילות התרופה
השינוי הבולט ביותר היה החלפה של אות אחת בודדת בגן fusA שמחליפה חומצת אמינו אחת—פרולין—באחרת—טריאונין—בעמדה 610 בחלבון EF‑G. EF‑G פועל כמו זרוע נעה שעוזרת להזיז tRNA ו‑mRNA דרך הריבוזום בעת בניית החלבון. באמצעות דגמים ממוחשבים של המבנה התלת‑ממדי של EF‑G, הצוות הראה שמיקום זה נמצא בציר בין שני דומיינים של EF‑G, שם החלבון מתכופף ומסתובב כאשר הוא דוחף את הריבוזום קדימה. הפרולין בציר זה נראה שמור באופן יוצא דופן בקרב חיידקים קרובים, מה שמרמז על חשיבותו. כאשר הוא מוחלף, הגמישות והדחיסות הכוללת של EF‑G משתנות, ומשנות בעדינות כיצד החלבון מתיישב נגד הריבוזום. סימולציות תזמון (docking) שממקמות וירטואלית את הגנטמיצין על קומפלקסים של ריבוזום–EF‑G מציעות שהתזוזה המרחבית הקטנה הזו משנה את הגיאומטריה של אזור קשירת התרופה. בצורה המוטנטית, גנטמיצין כבר לא יכול ללכוד את הריבוזום בשלב הפגיע שבו הוא בדרך כלל חוסם תנועה.
שינויים קלים במבנה ה‑RNA עם השלכות גדולות
המוטציות הופיעו גם בשניים מתוך עותקי גן ה‑16S rRNA המרובים שעוזרים ליצור את המחצית הקטנה של הריבוזום. באמצעות מיפוי השינויים האלה על מבני RNA ידועים, המחברים מצאו כי כולם התרכזו באזור "גוף 5′", קרוב לנקודה שבה בדרך כלל גנטמיצין וחלבון ריבוזומלי סמוך נקשרים. חיזויים ממוחשבים מפורטים הראו שהקיפול הכללי של ה‑RNA נשמר ברובו, אך לולאות ומקלות מקומיים בסמוך לבסיסים המוטנטים סודרו מחדש בעדינות. כוונונים מבניים קטנים אלה מספיקים לשנות את האינטראקציה של ה‑RNA עם חלבוני הריבוזום והתרופה, ולדחוף בסיסים קריטיים מעט החוצה מהמיקומים המדויקים שגנטמיצין זקוק להם לקשירה הדוקה. כאשר מצטרף לכך מוטציית הציר ב‑EF‑G, התוצאה היא ריבוזום שממשיך לקרוא הוראות גנטיות גם בנוכחות רמות גבוהות של התרופה. 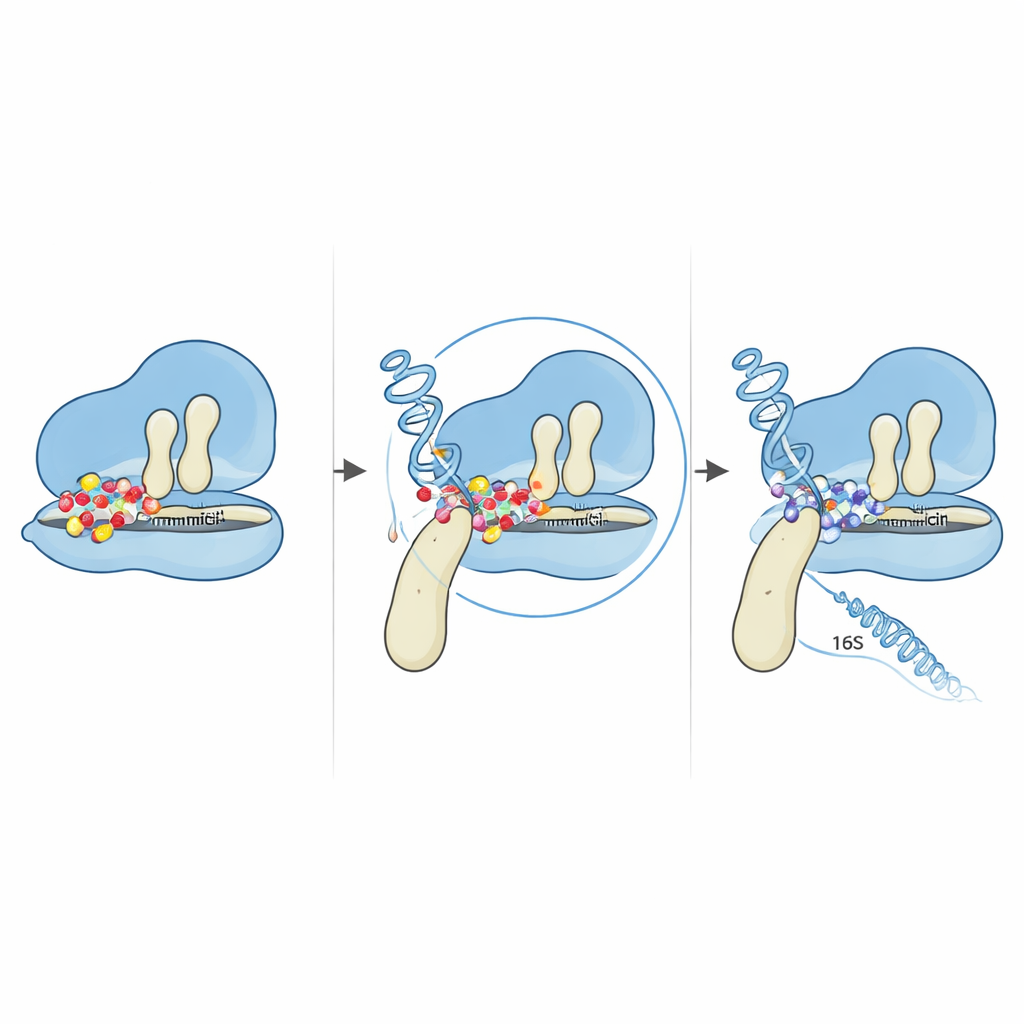
מה משמעות הדבר למאבק בעמידות
ביחד, העבודה מראה כי E. coli יכולה במהירות להרכיב מנגנון הגנה מדויק מאוד נגד גנטמיצין על‑ידי שינוי גם באתר העגינה של התרופה ב‑rRNA של הריבוזום וגם בחלק נייד של מנוע החלבון שמניע את התרגום. שינויים אלה אינם משמידים את מפעל החלבונים; הם מכוונים אותו במדויק מספיק כדי שהאנטיביוטיקה כבר לא תוכל לשתק אותו. מערכת ה‑ARGP מספקת דרך פשוטה וויזואלית ליצור ולחקור מסלולי עמידות כאלה בתנאים מבוקרים, וניתנת להתאמה לתרופות ולפתוגנים אחרים. לקוראים שאינם מומחים, המסר המרכזי הוא שעמידות אינה מגמה מעורפלת ואיטית — היא יכולה להופיע מהר באמצעות עריכות מולקולריות מדויקות. הבנת אותן עריכות בפירוט חיונית אם ברצוננו לעצב אנטיביוטיקות ואסטרטגיות טיפול חדשות שישארו צעד אחד לפני החיידקים המתפתחים.
ציטוט: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
מילות מפתח: עמידות לאנטיביוטיקה, gentamicin, Escherichia coli, ריבוזום, אבולוציה ניסויית