Clear Sky Science · zh
一种多尺度自适应滤波与 AtRes_SRU–transformer 协同的乳腺癌组织病理分类方法
这对患者和医生为何重要
早期发现乳腺癌往往意味着治疗更简单、预后更好,但显微镜下的组织检查既耗时又带有主观性。本文提出了一种新的计算机系统,帮助病理学家更准确、更高效地将乳腺组织图像分为良性与恶性病例。通过对图像进行精细清理并结合多种人工智能技术,该系统旨在支持更早的诊断、减少漏诊并降低不必要的误报。
在做判断前先清理图像
乳腺组织的显微图像远非完美,存在随机噪点、照明不均与染色带来的色彩差异,这些都会干扰即便是先进的算法。作者引入了一个称为多尺度自适应滤波的前端步骤,它像一种智能且温和的降噪器。该方法不是对所有细节一刀切地模糊处理,而是在多个尺度上观察图像,并根据局部对比度与纹理自适应调整。结果是干扰性噪声和染色伪影被抑制,同时重要的边缘——例如细胞簇之间的界限——得以保留。这为系统后续阶段提供了更清晰、更可靠的组织小块视图。
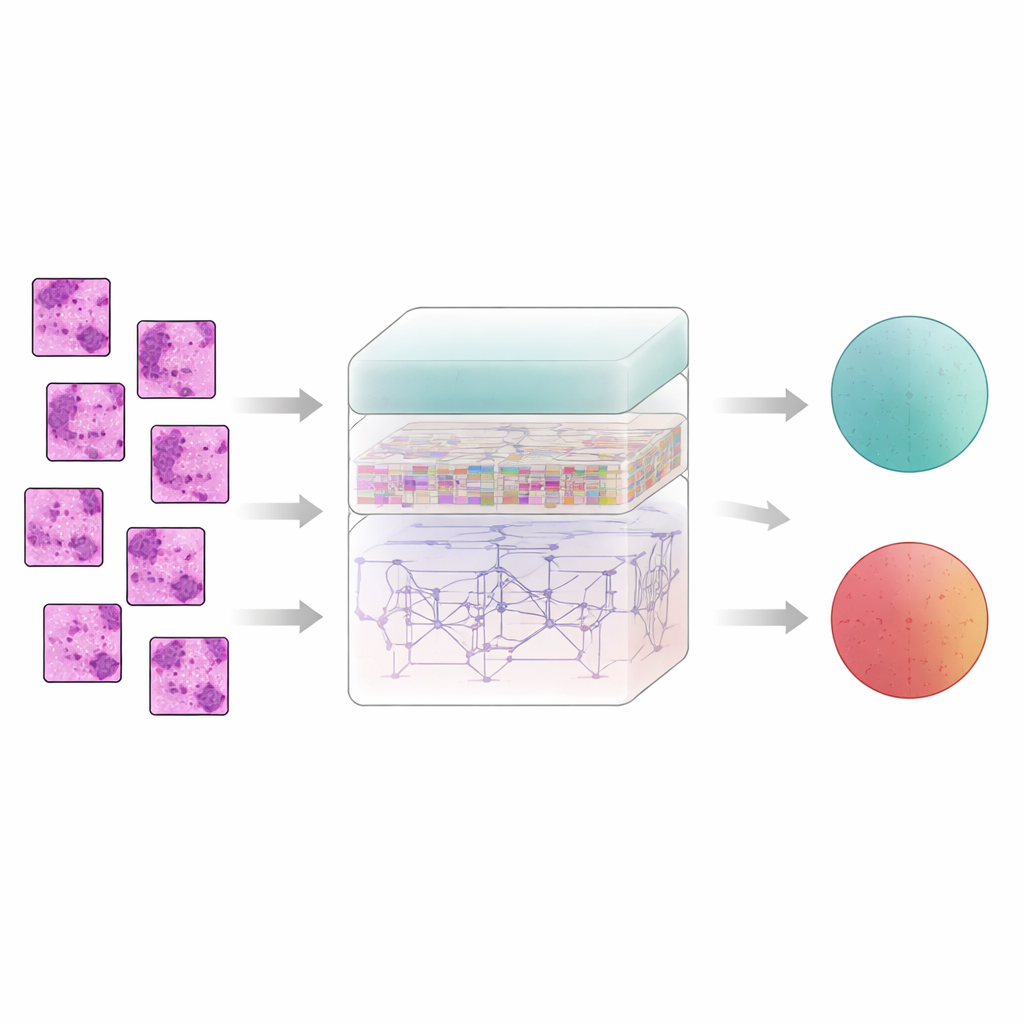
教会计算机识别组织格局
乳腺组织的意义并非由单个像素独立给出,而是从相邻区域之间的关系中显现。为捕捉这种关系,系统将每张滤波后图像切分为小块并输入称为 AtRes_SRU 的特征提取器。该模块将擅长捕捉形状与纹理的深度残差网络,与一种轻量级的循环单元相结合,将相邻图块视为序列中的步骤。尽管图像并非随时间变化,但按顺序排列图块让模型学习结构如何在切片上延续——细胞簇从何处开始或结束、腺体如何弯曲或断裂、异常区域如何嵌入常规组织之中。一个注意力机制进一步引导系统关注最可疑的区域,例如不规则的细胞核或异常致密的细胞簇。
看到整张切片,而非仅仅是微小片段
局部模式很重要,但癌症常常通过更大尺度的组织布局显露:异常区域的分布是否离散、扩散到多宽、以及它们如何与周围组织相互作用。为把握这种更广的图景,作者引入了 transformer 模块——一种最初为语言模型开发的技术。在这里,每个图块成为一个 token,transformer 学会建模任意两个图块间的关系。一种绝对位置编码告诉模型每个图块在原始切片中的精确位置,从而保留空间布局。在此之上,一个密集连接的决策层复用网络多个深度的特征,帮助系统在最终判定样本为良性或恶性时同时兼顾细节与全局语境。
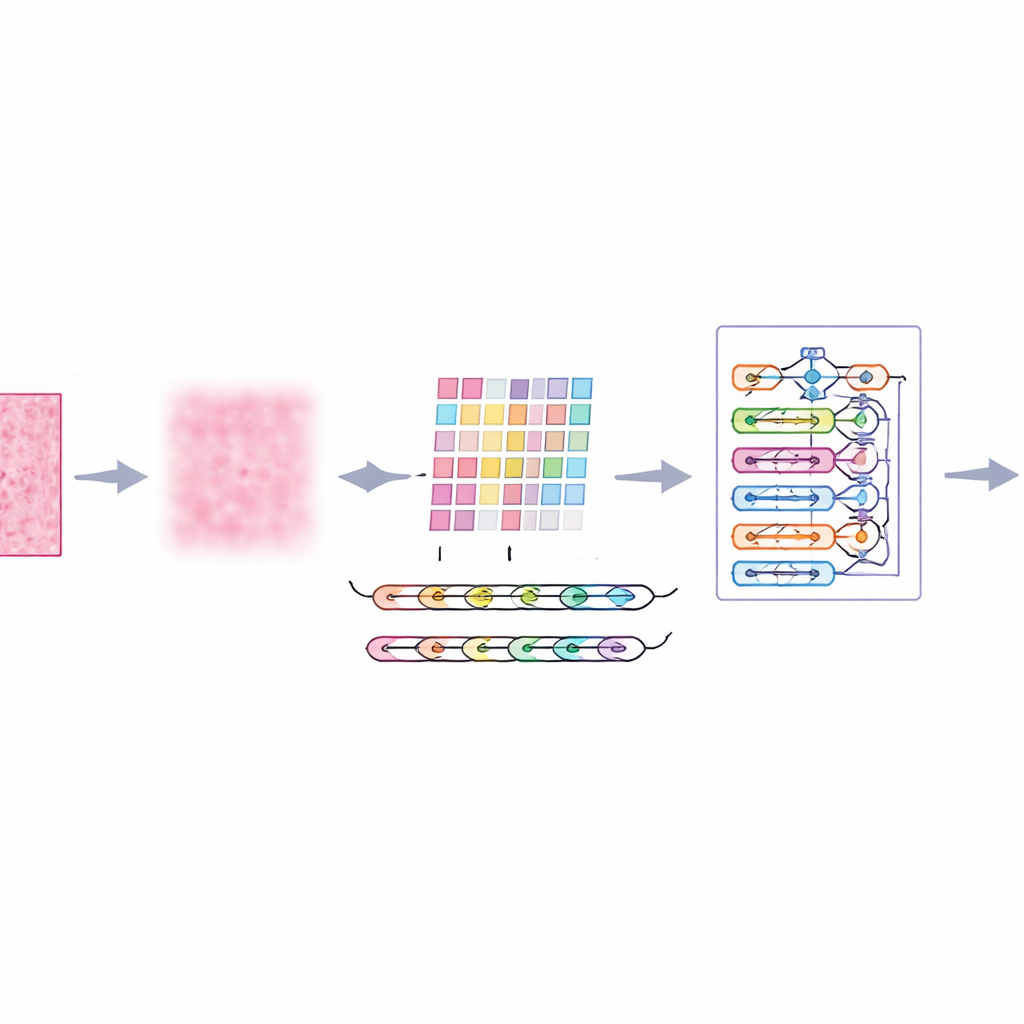
将系统付诸测试
研究人员在一个大型公开乳腺组织病理图像集上训练并评估了他们的“ImTranNet‑TriCore”框架,该数据集包含来自真实患者的二十多万张小图块,且在多个放大倍数下扫描得到。该数据集具有挑战性:切片间的组织外观差异很大,恶性区域可能很微妙或仅占图像的一小部分。尽管如此,新系统在区分癌变与非癌变图块时达到了约98%的准确率,并在各个放大级别上保持了强健的性能。它持续优于多种广泛使用的方法,包括传统卷积网络、增强注意力的模型以及将深度学习与传统机器学习混合的混合设计。
从数据到临床信任
仅有高准确率对医学应用还不够;医生需要理解系统作出决定的原因。因此作者使用热图和特征重要性工具检查了哪些图像区域对模型决策影响最大。他们发现系统倾向于突显病理学家关注的相同结构:细胞核的形状与边界、腺体的组织形式以及密集的异常组织簇。与此同时,模型保持低误报率,并表现出平滑校准的置信度分数,这对于避免漏诊与不必要的活检都很重要。尽管该方法在极高放大倍数下对一些非常细微的差别仍有困难,研究表明,将精细的图像清理、本地模式跟踪与整张切片的上下文结合起来,能使自动化乳腺癌评估更接近临床所需的可靠性。
引用: Saravana Kumar, N.M., Kandala, M.K., Kaveri, P.R. et al. A multi-scale adaptive filtering and AtRes_SRU–transformer synergy for breast cancer histopathology classification. Sci Rep 16, 14387 (2026). https://doi.org/10.1038/s41598-026-41153-7
关键词: 乳腺癌组织病理, 医学图像分析, 深度学习, Transformer 模型, 计算机辅助诊断