Clear Sky Science · tr
Meme kanseri histopatolojisi sınıflandırması için çok ölçekli uyarlanabilir filtreleme ve AtRes_SRU–transformer sinerjisi
Hastalar ve hekimler için neden önemli
Meme kanserini erken bulmak, basit bir tedavi ile hayatı tehdit eden bir hastalık arasındaki fark olabilir; ancak dokuya mikroskop altında bakmak yavaş ve özneldir. Bu makale, patoloji uzmanlarının meme dokusu görüntülerini zararsız ve tehlikeli vakalar olarak daha doğru ve verimli şekilde ayırmasına yardımcı olan yeni bir bilgisayar sistemi sunuyor. Görüntüleri dikkatle temizleyip çeşitli yapay zeka türlerini birleştirerek sistem, daha erken tanıya, daha az kaçırılan kanser vakasına ve daha az gereksiz alarma destek olmayı hedefliyor.
Karar vermeden önce görüntüyü temizlemek
Meme dokusunun mikroskop görüntüleri kusursuz değildir. Rastgele lekeler, düzensiz aydınlatma ve boyamadan kaynaklanan renk farklılıkları içerir; bunların hepsi gelişmiş algoritmaları bile yanıltabilir. Yazarlar, çok ölçekli uyarlanabilir filtreleme adını verdikleri bir ön adım tanıtıyor; bu, akıllı ve nazik bir gürültü filtresi gibi davranıyor. Her şeyi eşit şekilde bulanıklaştırmak yerine görüntüyü birkaç ayrıntı düzeyinde inceliyor ve yerel kontrast ile dokuya uyum sağlıyor. Sonuç olarak, dikkat dağıtan gürültü ve boyama artefaktları azaltılırken, hücre grupları arasındaki sınırlar gibi önemli kenarlar korunuyor. Bu, sistemin sonraki aşamalarına her doku yaması için daha net ve güvenilir bir görüntü sunuyor.
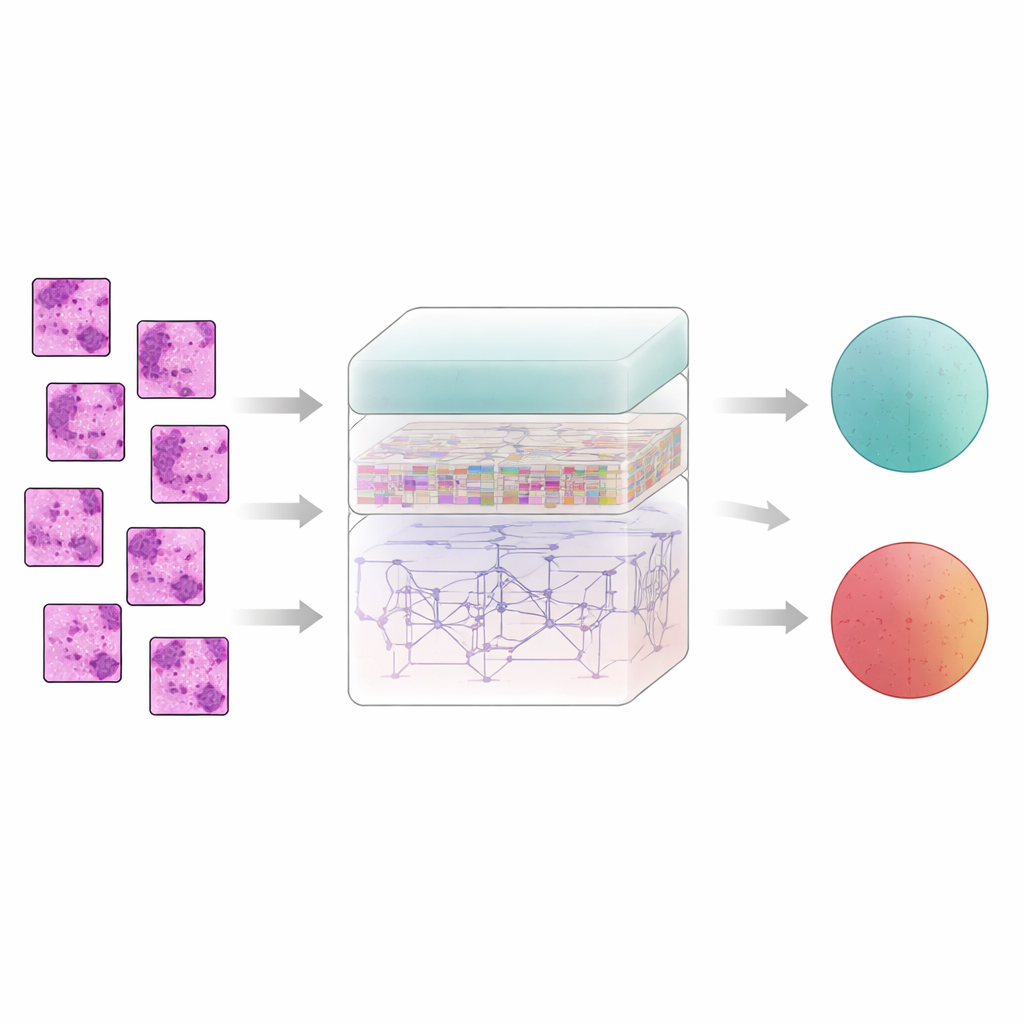
Bilgisayara doku desenlerini takip etmeyi öğretmek
Meme dokusu hikâyesini pikselleri tek tek anlatarak söylemez; anlam, bitişik bölgelerin birbirleriyle ilişkilerinden doğar. Bunu yakalamak için sistem, her filtrelenmiş görüntüyü küçük yamalara böler ve bunları AtRes_SRU adlı bir özellik çıkarıcıya besler. Bu bileşen, şekil ve dokuları saptamakta iyi olan derin bir residual ağ ile bitişik yamaları bir dizi adımı gibi ele alan hafif bir tekrarlı birimi birleştirir. Zaman içinde hareket eden bir şey olmasa da, yamaları sıra halinde düzenlemek modele yapının slayt boyunca nasıl aktığını—hücre kümelerinin nerede başlayıp bittiğini, bezlerin nasıl eğildiğini veya parçalandığını ve anormal bölgelerin daha düzenli doku içindeki konumunu—öğretir. Bir dikkat mekanizması da sistemi düzensiz çekirdekler veya olağandışı yoğun hücre kümeleri gibi en şüpheli bölgelere odaklanmaya yönlendirir.
Sadece küçük parçalara değil, tüm slayta bakmak
Yerel desenler önemli olmakla birlikte, kanser genellikle daha geniş ölçekli düzenlemelerle kendini gösterir: anormal bölgelerin ne kadar dağınık olduğu, ne kadar yayıldığı ve çevre doku ile nasıl etkileştiği. Bu daha geniş resmi yakalamak için yazarlar bir transformer modülü ekliyor; bu teknoloji ilk olarak dil modelleri için geliştirildi. Burada her yama bir token olur ve transformer her yamanın diğer tüm yamalarla nasıl ilişkili olduğunu öğrenir. Mutlak konum kodlamanın bir biçimi modele her yamanın orijinal slaytta tam olarak nereden geldiğini söyler ve mekânsal düzeni korur. Bunun üzerine, ağın birçok katmanındaki özellikleri yeniden kullanan yoğun bağlı bir karar katmanı eklenir; bu da sistemin nihai olarak örneğin benign mi yoksa malign mi olduğuna karar verirken hem ince ayrıntıları hem de küresel bağlamı akılda tutmasına yardımcı olur.
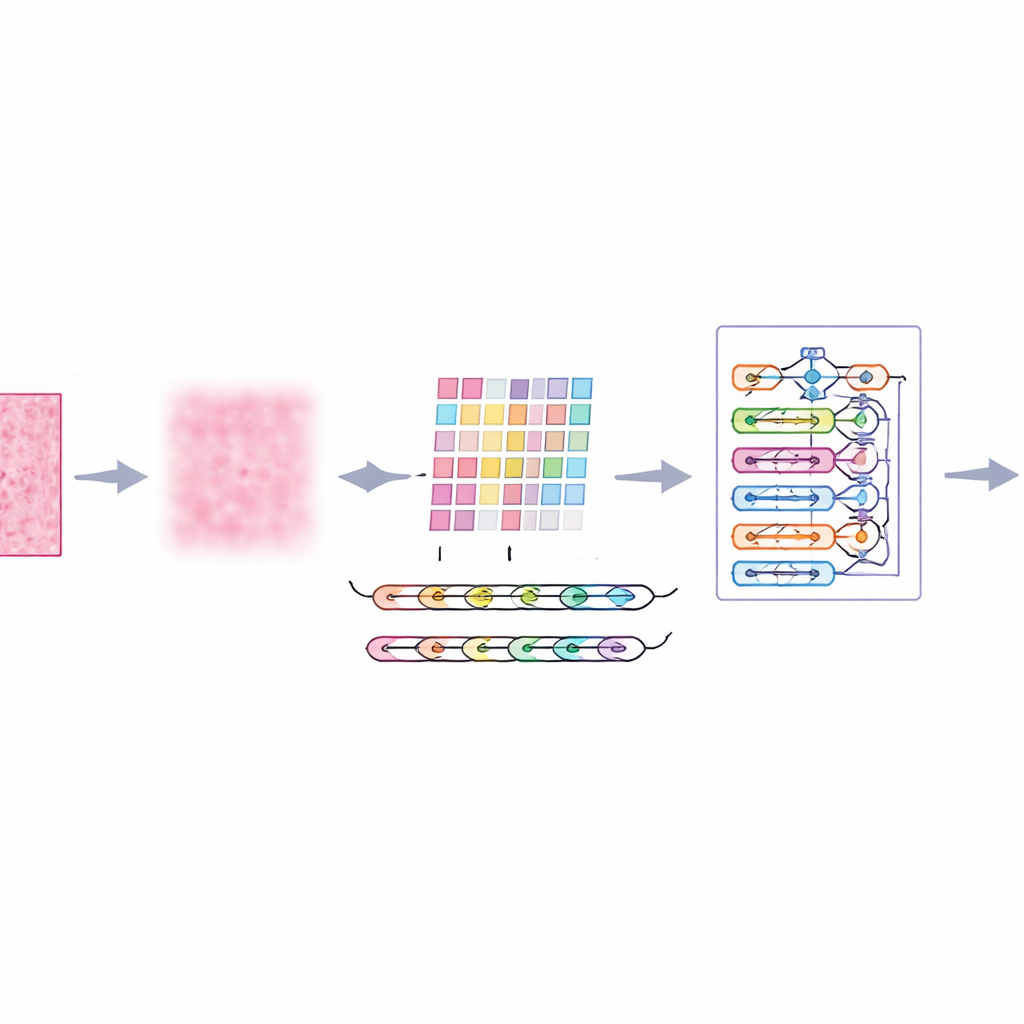
Sistemi teste sokmak
Araştırmacılar, "ImTranNet‑TriCore" çerçevelerini, gerçek hastalardan elde edilen ve birkaç büyütme düzeyinde taranan çeyrek milyondan fazla küçük yama içeren büyük bir kamu meme histopatoloji görüntüleri koleksiyonunda eğitti ve değerlendirdi. Veri seti zorludur: doku görünümü slaytlar arasında büyük ölçüde değişir ve malign bölgeler ince olabilir veya bir görüntünün yalnızca küçük bir bölümünü kaplayabilir. Buna rağmen, yeni sistem kanserli ile kanserli olmayan yamaları ayırt etmede yaklaşık %98 doğruluk elde etti ve tüm yakınlaştırma düzeylerinde güçlü performans gösterdi. Yaygın kullanılan yöntemler arasında yer alan geleneksel konvolüsyonel ağlar, dikkat destekli modeller ve derin öğrenmeyi geleneksel makine öğrenmesiyle karıştıran hibrit tasarımları tutarlı şekilde geride bıraktı.
Sayılar ile gerçek kliniklerde güven oluşturmak
Yüksek doğruluk tek başına tıp için yeterli değildir; hekimlerin bir sistemin neden bu karara vardığını anlaması gerekir. Bu nedenle yazarlar, ısı haritası ve özellik-önem araçları kullanarak modelin seçimlerini en çok hangi görüntü bölgelerinin etkilediğini incelediler. Sistemin patologların baktığı aynı yapıları vurgulamaya eğilimli olduğunu buldular: hücre çekirdeklerinin şekilleri ve sınırları, bezlerin düzeni ve yoğun anormal doku kümeleri. Aynı zamanda model yanlış alarmları düşük tutuyor ve hem kaçırılan kanserleri hem de gereksiz biyopsileri önlemek için önemli olan düzgün kalibre edilmiş güven skorları gösteriyor. Yöntem hâlâ bazı çok ince ayrımlarda ve aşırı büyütmede zorlanıyor olsa da, çalışma dikkatli görüntü temizliği, yerel desen takibi ve tüm slayt bağlamını birleştirmenin otomatik meme kanseri değerlendirmesini klinisyenlerin ihtiyaç duyduğu güvenilirliğe önemli ölçüde yaklaştırabileceğini öne sürüyor.
Atıf: Saravana Kumar, N.M., Kandala, M.K., Kaveri, P.R. et al. A multi-scale adaptive filtering and AtRes_SRU–transformer synergy for breast cancer histopathology classification. Sci Rep 16, 14387 (2026). https://doi.org/10.1038/s41598-026-41153-7
Anahtar kelimeler: meme kanseri histopatolojisi, tıbbi görüntü analizi, derin öğrenme, transformer modelleri, bilgisayar destekli tanı