Clear Sky Science · ar
ترشيح تكيفي متعدد المقياس وتكامل AtRes_SRU–محول لتصنيف الهستوباثولوجيا لسرطان الثدي
لماذا يهم هذا للمرضى والأطباء
يمكن أن يكون الكشف المبكر عن سرطان الثدي الفاصل بين علاج بسيط ومرض يهدد الحياة، ومع ذلك فإن فحص الأنسجة تحت المجهر عملية بطيئة وذاتية إلى حدٍّ ما. تقدم هذه الورقة نظامًا حاسوبيًا جديدًا يساعد علماء الأمراض على فرز صور أنسجة الثدي إلى حالات غير ضارة وخطيرة بدقة وكفاءة أكبر. عن طريق تنظيف الصور بعناية ودمج عدة أنواع من الذكاء الاصطناعي، يهدف النظام إلى دعم التشخيص المبكر، وتقليل حالات تفويت السرطان، وخفض الإنذارات غير الضرورية.
تنقية الصورة قبل اتخاذ القرار
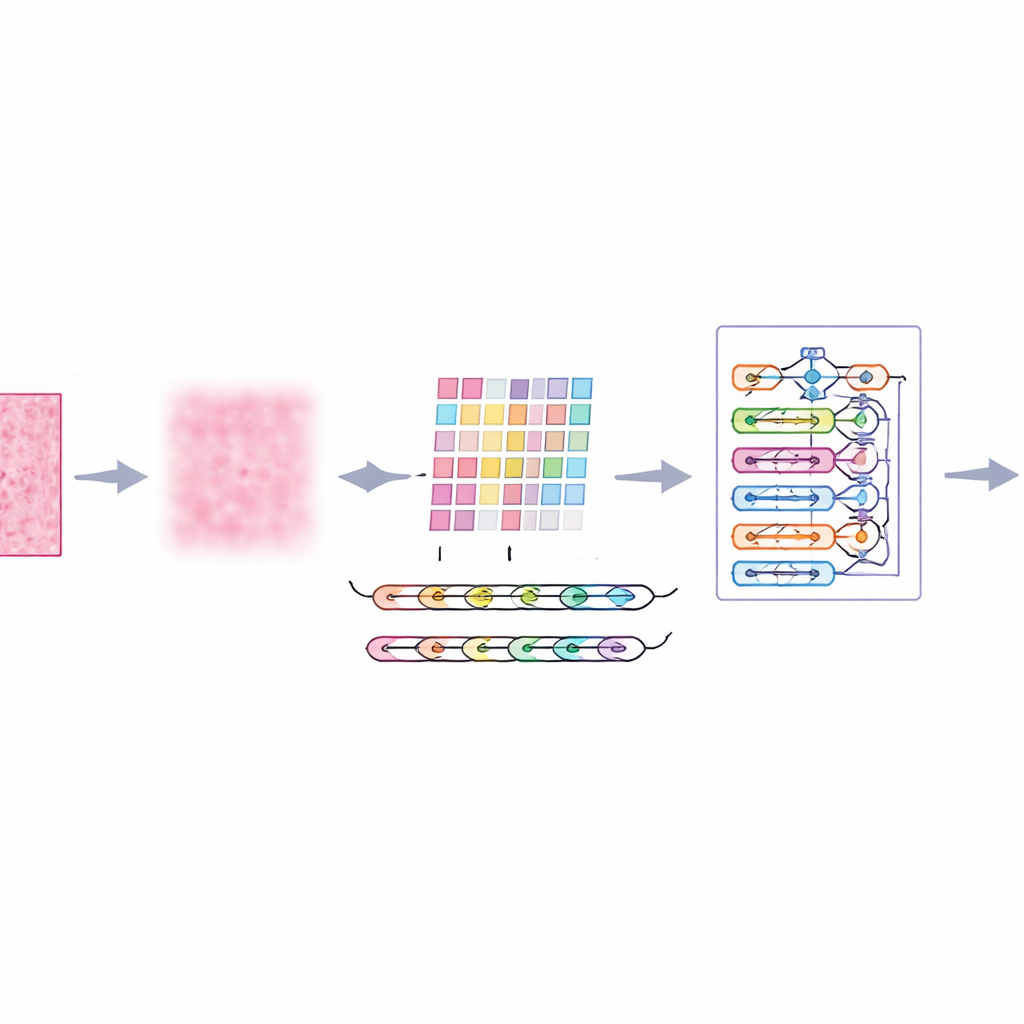
صور المجهر لأنسجة الثدي بعيدة عن الكمال. فهي تحتوي على بقع عشوائية، وإضاءة غير متساوية، وتباينات لونية ناجمة عن التلوين، وكلها قد تشتت حتى الخوارزميات المتقدمة. يقدم المؤلفون خطوة أمامية تسمى الترشيح التكيفي متعدد المقياس، تعمل كمرشح ذكي ولطيف للضوضاء. بدلاً من تمويه كل شيء بالتساوي، تنظر هذه الطريقة إلى الصورة عبر مستويات متعددة من التفاصيل وتتكيّف مع التباين المحلي والملمس. والنتيجة تقليل الضوضاء والتشوهات الناتجة عن التلوين، مع الحفاظ على الحواف المهمة — مثل حدود مجموعات الخلايا. هذا يمنح المراحل اللاحقة من النظام رؤية أوضح وأكثر موثوقية لكل رقعة نسيج.
تعليم الحاسوب تتبّع أنماط الأنسجة
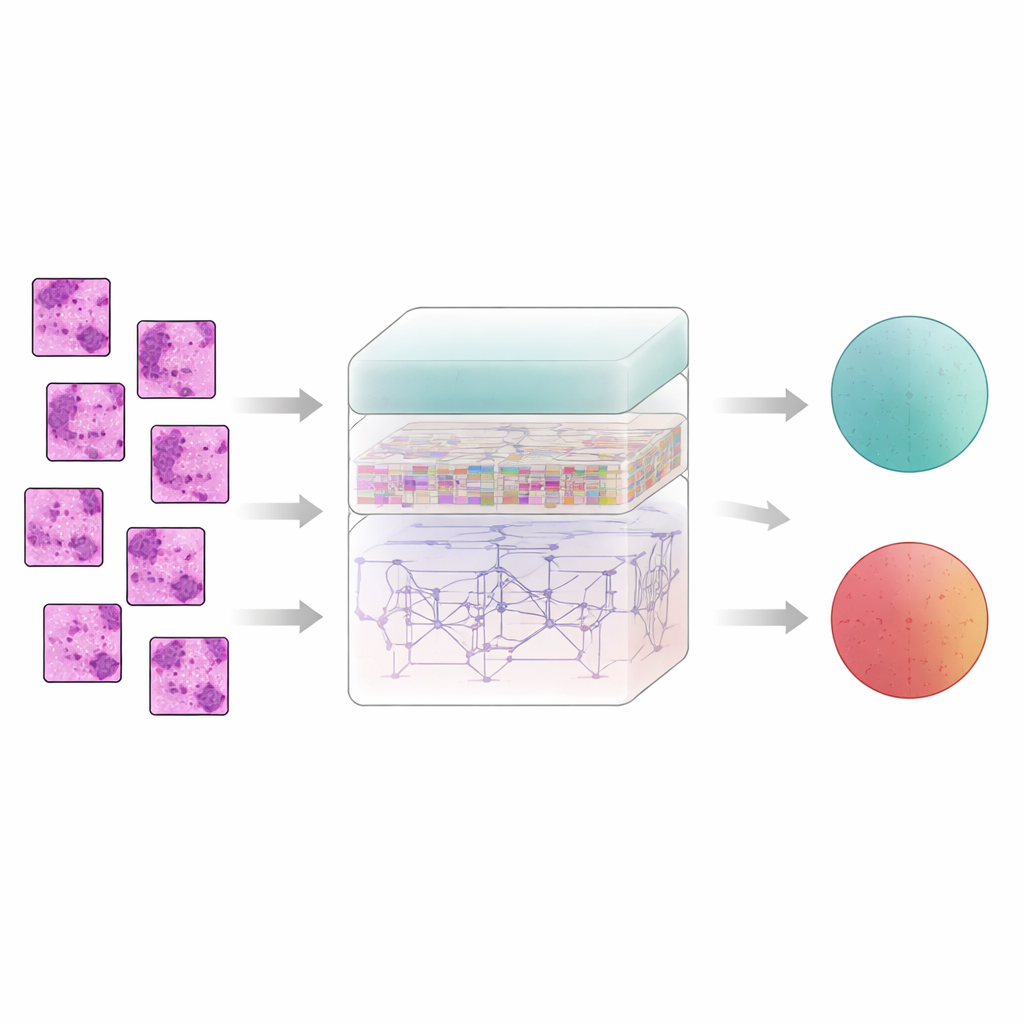
الأنسجة الثديية لا تكشف قصتها بكسل واحد في كل مرة؛ المعنى ينشأ من كيفية علاقة المناطق المجاورة ببعضها. لالتقاط هذا، يقوم النظام بتقسيم كل صورة مفلترة إلى رقع صغيرة ويدخلها إلى مستخرج ميزات يسمى AtRes_SRU. يجمع هذا الجزء بين شبكة احتياطية عميقة، جيدة في اكتشاف الأشكال والأنسجة، ووحدة متكررة خفيفة الوزن تتعامل مع الرقع المجاورة كما لو كانت خطوات في تسلسل. على الرغم من عدم وجود حركة زمنية فعلية، فإن ترتيب الرقع يسمح للنموذج بتعلّم كيفية تدفق البنى عبر الشريحة — أين تبدأ وتنتهي مجموعات الخلايا، كيف تنحني الغدد أو تنكسر، وكيف تجاور المناطق الشاذة الأنسجة الطبيعية. يدفع آلية الانتباه النظام أيضًا للتركيز على المناطق الأكثر اشتباهًا، مثل النوى غير المنتظمة أو التجمعات الخلوية الكثيفة غير الاعتيادية.
رؤية الشريحة كاملة، وليس قطعًا صغيرة فقط
بينما تهم الأنماط المحلية، غالبًا ما يكشف السرطان عن نفسه من خلال تنظيم أوسع نطاقًا: مدى تشتت المناطق الشاذة، مدى انتشارها، وكيف تتفاعل مع الأنسجة المحيطة. للإحاطة بهذه الصورة الأوسع، يضيف المؤلفون وحدة محول، وهي تقنية طورت أصلاً لنماذج اللغة. هنا تصبح كل رقعة رمزًا (توكن)، ويتعلم المحول كيفية ارتباط كل رقعة بكل أخرى. شكل من أشكال ترميز الموضع المطلق يخبر النموذج بمكان كل رقعة بالضبط في الشريحة الأصلية، محافظًا على التخطيط المكاني. علاوة على ذلك، تعيد طبقة قرار متصلة بكثافة استخدام الميزات من أعماق متعددة في الشبكة، مما يساعد النظام على الحفاظ على التفاصيل الدقيقة والسياق العام عند اتخاذ القرار النهائي بشأن كون العينة حميدة أم خبيثة.
اختبار النظام عمليًا
درّب الباحثون وقَيّموا إطارهم "ImTranNet‑TriCore" على مجموعة عامة كبيرة من صور هستوباثولوجيا الثدي، التي تتضمن أكثر من ربع مليون رقعة صغيرة مأخوذة من مرضى حقيقيين، ممسوحة بمستويات تكبير متعددة. تُعد قاعدة البيانات تحديًا: مظهر الأنسجة يختلف على نحو واسع عبر الشرائح، وقد تكون المناطق الخبيثة رقيقة أو تشغل جزءًا صغيرًا فقط من الصورة. ومع ذلك، حقق النظام الجديد دقة تقارب 98% في التمييز بين الرقع السرطانية وغير السرطانية واحتفظ بأداء قوي عبر جميع مستويات التكبير. تفوق باستمرار على مجموعة من الطرق الشائعة الاستخدام، بما في ذلك الشبكات الالتفافية التقليدية، والنماذج المحسنة بالانتباه، والتصاميم الهجينة التي تمزج التعلّم العميق مع تقنيات تعلم الآلة التقليدية.
من الأرقام إلى الثقة في العيادات الحقيقية
الدقة العالية وحدها لا تكفي في المجال الطبي؛ يحتاج الأطباء إلى فهم سبب توصّل النظام إلى قراراته. لذلك فحص المؤلفون أي مناطق الصور أثّرت أكثر على اختيارات النموذج باستخدام خرائط حرارية وأدوات أهمية الميزات. وجدوا أن النظام يميل إلى إبراز نفس البنى التي ينظر إليها أطباء الأمراض: أشكال وحدود نوى الخلايا، وتنظيم الغدد، وتجمعات كثيفة من الأنسجة الشاذة. وفي الوقت نفسه، يحافظ النموذج على معدلات إنذارات خاطئة منخفضة ويظهر درجات ثقة معايرة بسلاسة، وهو أمر مهم لتجنب كل من تفويت حالات السرطان وإجراء خزعات غير ضرورية. بينما لا تزال الطريقة تواجه صعوبة مع بعض الفروق الدقيقة جدًا عند تكبيرات قصوى، تشير الدراسة إلى أن دمج تنظيف الصور بعناية، وتعقب الأنماط المحلية، والسياق على مستوى الشريحة بأكملها يمكن أن يقرب تقييم سرطان الثدي المؤتمت كثيرًا من الموثوقية التي يحتاجها الأطباء.
الاستشهاد: Saravana Kumar, N.M., Kandala, M.K., Kaveri, P.R. et al. A multi-scale adaptive filtering and AtRes_SRU–transformer synergy for breast cancer histopathology classification. Sci Rep 16, 14387 (2026). https://doi.org/10.1038/s41598-026-41153-7
الكلمات المفتاحية: هستوباثولوجيا سرطان الثدي, تحليل الصور الطبية, التعلّم العميق, نماذج المحول, التشخيص بمساعدة الحاسوب