Clear Sky Science · ja
乳癌組織病理分類のためのマルチスケール適応フィルタリングとAtRes_SRU–トランスフォーマーの相乗効果
患者と医師にとってなぜ重要か
乳がんを早期に発見できれば、簡単な治療で済む場合と生命を脅かす事態との差が生まれますが、顕微鏡下での組織観察は時間がかかり主観的になりがちです。本論文は、病理医が乳腺組織画像を無害なケースと危険なケースにより正確かつ効率的に仕分けできるよう支援する新しいコンピュータシステムを提示します。画像を丁寧に前処理し、複数の人工知能手法を組み合わせることで、より早期の診断、見逃しの減少、不要な警告の低減を目指しています。
判断の前に画像をきれいにする
乳腺組織の顕微鏡画像は決して完璧ではありません。ランダムな斑点、照明のムラ、染色による色むらなどが含まれ、高度なアルゴリズムでも混乱を招きます。著者らはマルチスケール適応フィルタリングと呼ばれる前処理段階を導入しています。これは賢く穏やかなノイズフィルターのように動作します。すべてを均一にぼかす代わりに、複数の細部レベルで画像を観察し、局所的なコントラストやテクスチャに適応します。その結果、気を散らすノイズや染色アーティファクトは低減され、細胞集団の境界など重要なエッジは保持されます。これにより後続のシステム段階は各組織パッチをより明瞭で信頼できる形で解析できます。
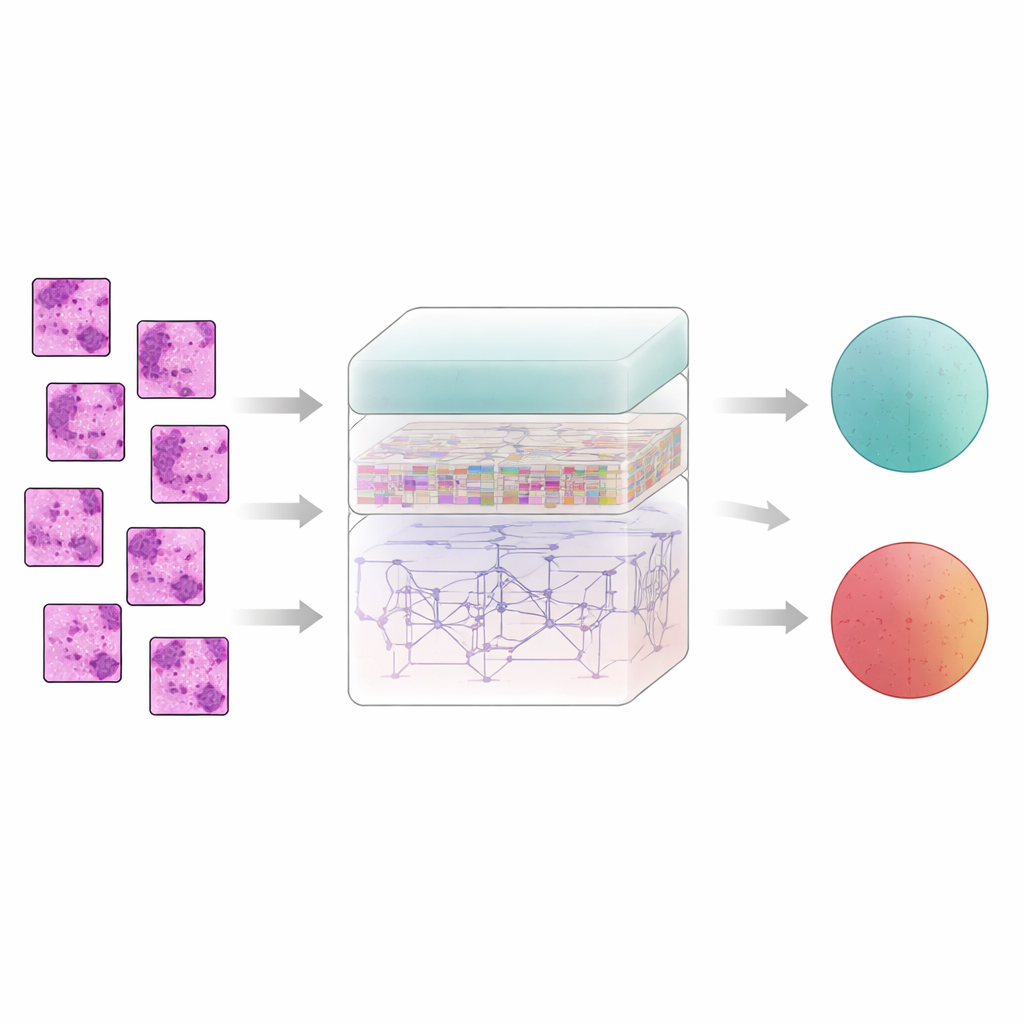
組織パターンをたどるように学習させる
乳組織はピクセル単位で単独に物語るわけではなく、隣接領域同士の関係から意味が生じます。これを捉えるために、システムはフィルタリングした画像を小さなパッチに分割し、AtRes_SRUと呼ばれる特徴抽出器に入力します。この部分は形状やテクスチャの検出が得意な深い残差ネットワークと、隣接するパッチを列のように扱う軽量な再帰ユニットを組み合わせています。時間的な動きは存在しないものの、パッチを順序立てて配置することで、モデルはスライド上で構造がどのように流れるかを学習できます――細胞クラスターがどこで始まり終わるか、腺がどのように曲がったり切れたりするか、異常領域がより規則的な組織の中でどのように存在するかなどです。さらに注意機構(アテンション)が、異常核や異常に密な細胞集団など、より疑わしい領域に焦点を当てるよう促します。
小片だけでなくスライド全体を見る
局所的なパターンは重要ですが、がんはしばしばより大きなスケールでの配置を通じて現れます:散在する異常領域がどれほど広がるか、どのくらいの範囲に及ぶか、周囲組織とどのように相互作用するか。こうした広い視点を把握するために、著者らはトランスフォーマーモジュールを追加しています。これは元々言語モデルのために開発された技術で、ここでは各パッチがトークンとなり、トランスフォーマーがすべてのパッチ同士の関係を学習します。絶対位置エンコーディングの一種が、各パッチが元のスライドのどこから来たかを正確にモデルに伝え、空間配置を保持します。その上で、密に接続された決定層がネットワークの多くの深さからの特徴を再利用し、最終的に良性か悪性かを判断する際に細部と全体文脈の両方を保持できるよう助けます。
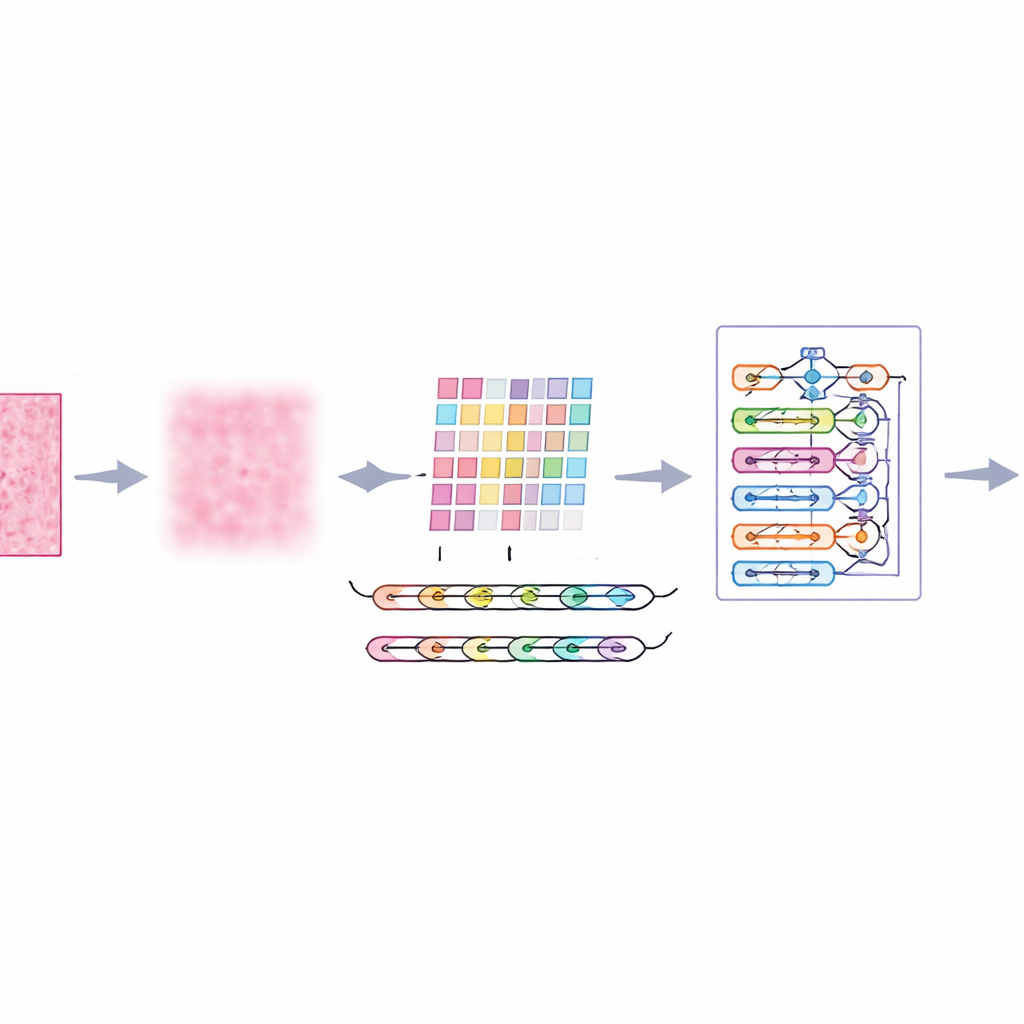
システムの検証
研究者らは大規模な公開乳腺組織病理画像コレクションで「ImTranNet‑TriCore」フレームワークを訓練・評価しました。このデータセットには実患者由来の小パッチが25万以上含まれ、複数の倍率でスキャンされています。データは挑戦的です:スライド間で組織の見え方が大きく異なり、悪性領域は微妙であったり画像の一部しか占めないことがあります。それにもかかわらず、新しいシステムは癌性と非癌性のパッチを判別する際に約98%の精度を達成し、すべてのズームレベルで安定した性能を示しました。従来の畳み込みネットワーク、アテンション強化モデル、深層学習と従来型機械学習を混合したハイブリッド設計など、広く用いられる手法の多くを一貫して上回りました。
数値から臨床での信頼へ
医療にとって高精度だけでは十分ではありません。医師はシステムがなぜその判断に至ったかを理解する必要があります。そこで著者らはヒートマップや特徴重要度解析を用いて、モデルの判断に最も影響を与えた画像領域を調べました。その結果、システムは病理医が注目するのと同じ構造を強調する傾向があることがわかりました:細胞核の形状や境界、腺の配置、異常組織の密なクラスターなどです。同時に誤警報は低く抑えられ、滑らかに較正された信頼度スコアを示しており、見逃しや不要な生検の回避に重要です。極端な倍率での非常に微細な差異には依然として苦戦する面はありますが、慎重な画像前処理、局所パターンの追跡、スライド全体の文脈を組み合わせることで、臨床に必要な信頼性に自動化された乳癌評価をより近づけられることを本研究は示唆しています。
引用: Saravana Kumar, N.M., Kandala, M.K., Kaveri, P.R. et al. A multi-scale adaptive filtering and AtRes_SRU–transformer synergy for breast cancer histopathology classification. Sci Rep 16, 14387 (2026). https://doi.org/10.1038/s41598-026-41153-7
キーワード: 乳癌組織病理, 医用画像解析, ディープラーニング, トランスフォーマーモデル, 診断支援システム