Clear Sky Science · ru
Многошкальное адаптивное фильтрование и синергия AtRes_SRU–трансформера для классификации гистопатологии рака молочной железы
Почему это важно для пациентов и врачей
Раннее обнаружение рака молочной железы может означать разницу между простой терапией и опасным для жизни заболеванием, однако исследование тканей под микроскопом — это медленная и субъективная работа. В этой статье представлена новая компьютерная система, которая помогает патологам более точно и эффективно сортировать изображения тканей молочной железы на безвредные и опасные случаи. Тщательно очищая изображения и комбинируя несколько типов искусственного интеллекта, система призвана способствовать более ранней диагностике, меньшему числу пропущенных случаев рака и снижению количества ложных тревог.
Очистка изображения перед принятием решения
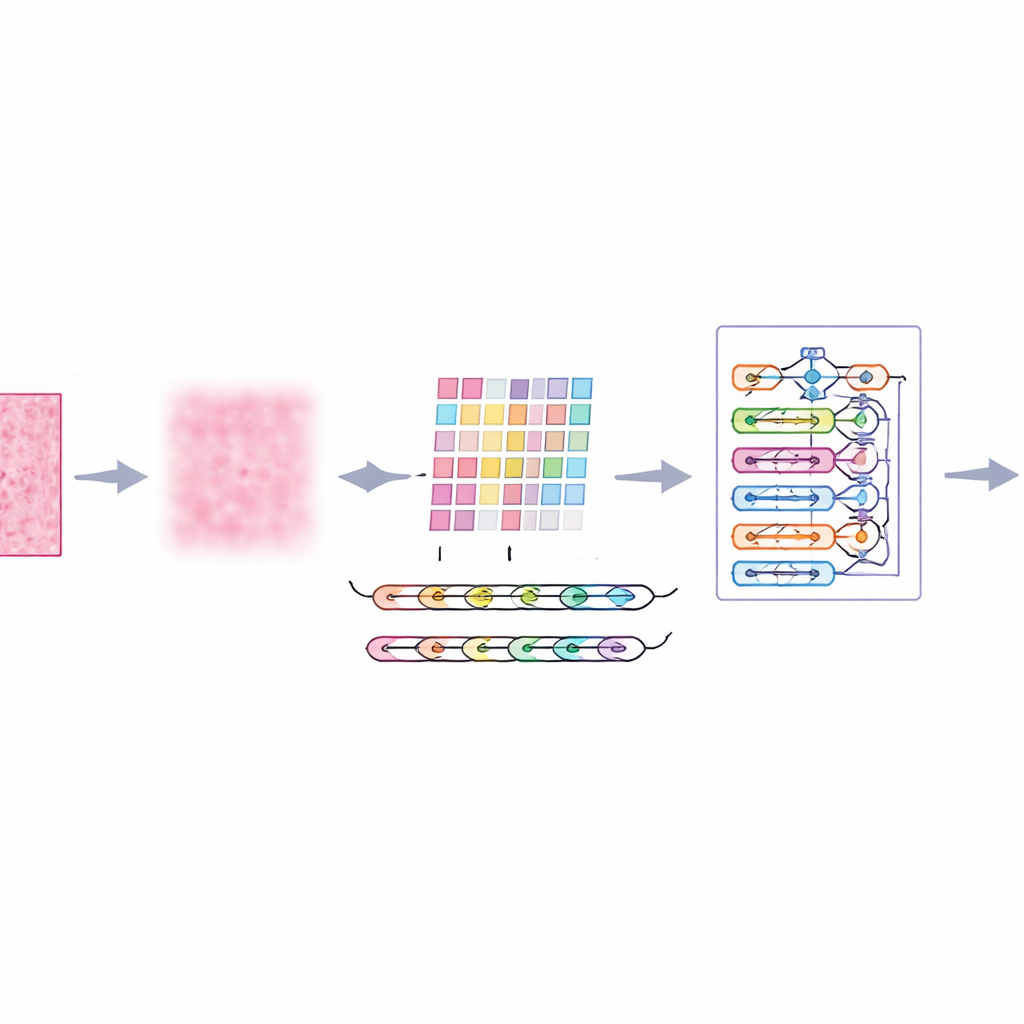
Микроскопические изображения тканей молочной железы далеки от идеала. Они содержат случайный шум, неравномерное освещение и цветовые вариации от окрашивания, которые могут сбивать с толку даже продвинутые алгоритмы. Авторы вводят передний этап, называемый многошкальным адаптивным фильтрованием, который действует как интеллектуальный, щадящий фильтр шума. Вместо того чтобы размазывать всё одинаково, он рассматривает изображение на нескольких уровнях детализации и адаптируется к локальному контрасту и текстуре. В результате уменьшаются отвлекающие шумы и артефакты окрашивания, при этом сохраняются важные границы — например, границы между группами клеток. Это даёт последующим этапам системы более ясное и надёжное представление каждого участка ткани.
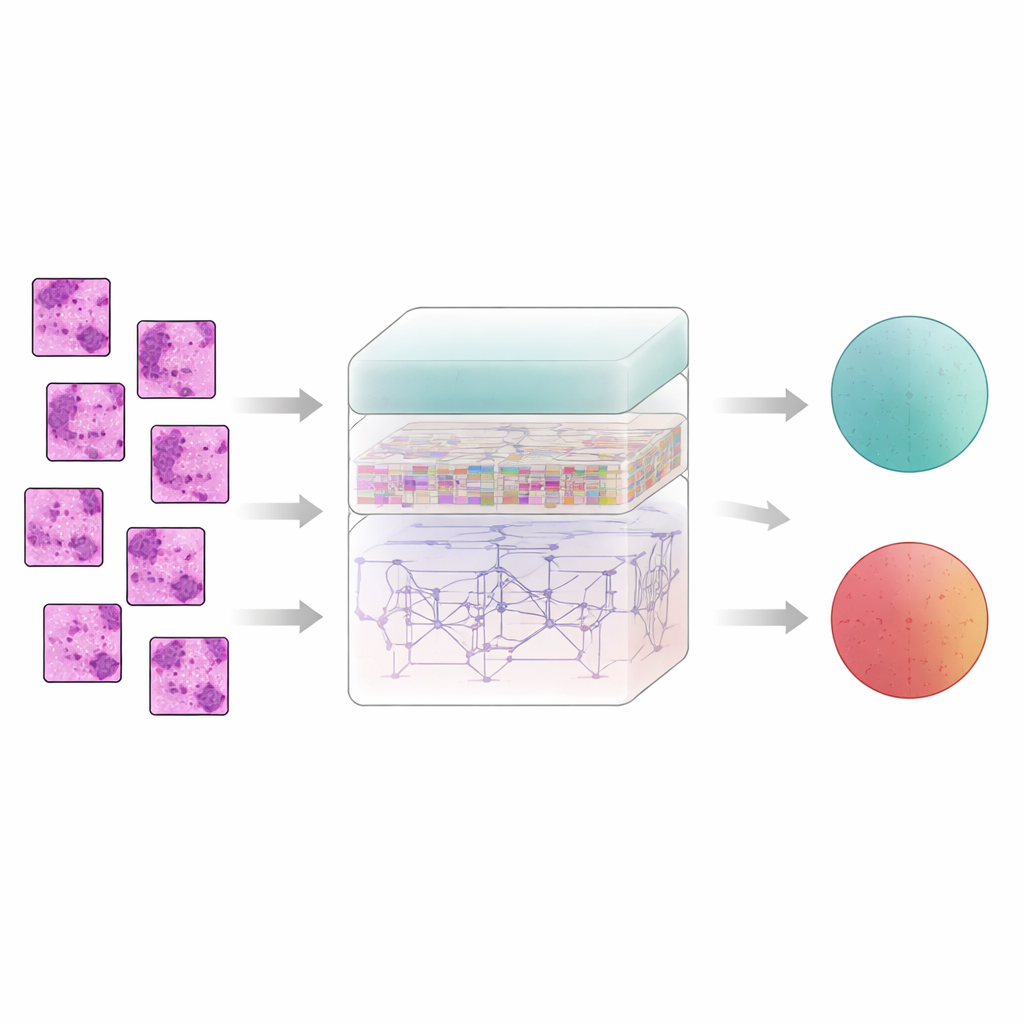
Обучение компьютера распознавать тканевые структуры
Ткань молочной железы не «рассказывает» свою историю по одному пикселю; смысл возникает из взаимосвязей соседних областей. Чтобы это зафиксировать, система разрезает каждое отфильтрованное изображение на небольшие фрагменты и подаёт их в извлекатель признаков, называемый AtRes_SRU. Эта часть объединяет глубокую остаточную сеть, хорошо распознающую формы и текстуры, с лёгким рекуррентным блоком, который рассматривает соседние фрагменты как шаги в последовательности. Хотя во времени ничего не движется, упорядочивание фрагментов позволяет модели учиться тому, как структуры распространяются по слайду — где начинаются и заканчиваются скопления клеток, как изгибаются или нарушаются железы и как аномальные области вписываются в более регулярную ткань. Механизм внимания дополнительно смещает фокус системы на наиболее подозрительные участки, такие как неправильной формы ядра или необычно плотные скопления клеток.
Видеть весь слайд, а не только мелкие фрагменты
Хотя локальные паттерны важны, рак часто проявляется через организацию в более крупном масштабе: насколько разбросаны аномальные зоны, как широко они распространены и как взаимодействуют с окружающей тканью. Чтобы охватить эту более широкую картину, авторы добавляют модуль‑трансформер, технологию, изначально разработанную для языковых моделей. Здесь каждый фрагмент становится токеном, и трансформер учится тому, как каждый фрагмент соотносится с каждым другим. Форма абсолютного позиционного кодирования сообщает модели точное местоположение каждого фрагмента на исходном слайде, сохраняя пространственную разметку. Поверх этого плотносвязный слой принятия решений повторно использует признаки из разных уровней сети, помогая системе учитывать и тонкие детали, и глобальный контекст при окончательном решении о доброкачественности или злокачественности образца.
Испытание системы
Исследователи обучали и оценивали свою структуру «ImTranNet‑TriCore» на большой публичной коллекции изображений гистопатологии молочной железы, которая включает более четверти миллиона маленьких фрагментов от реальных пациентов, отсканированных на нескольких увеличениях. Датасет непростой: внешний вид тканей сильно варьируется между слайдами, а злокачественные участки могут быть тонкими или занимать лишь небольшую часть изображения. Несмотря на это, новая система достигла примерно 98% точности в разделении раковых и нераковых фрагментов и сохранила высокую производительность на всех уровнях увеличения. Она последовательно превзошла ряд широко используемых методов, включая традиционные сверточные сети, модели с усиленным вниманием и гибридные конструкции, сочетающие глубокое обучение с классическими методами машинного обучения.
От чисел к доверию в клиниках
Одной высокой точности для медицины недостаточно; врачам важно понимать, почему система принимает те или иные решения. Поэтому авторы проанализировали, какие области изображения сильнее всего влияют на выбор модели, используя тепловые карты и инструменты оценки важности признаков. Они обнаружили, что система склонна выделять те же структуры, на которые обращают внимание патологи: формы и границы ядер клеток, организацию желез и плотные скопления аномальной ткани. При этом модель сохраняет низкий уровень ложных срабатываний и демонстрирует плавно откалиброванные оценки уверенности — важно для избежания как пропущенных случаев, так и ненужных биопсий. Хотя метод всё ещё испытывает трудности с некоторыми особо тонкими различиями при экстремальном увеличении, исследование показывает, что сочетание аккуратной очистки изображений, отслеживания локальных паттернов и учёта контекста всего слайда может существенно приблизить автоматическую оценку рака молочной железы к надёжности, требуемой клиницистами.
Цитирование: Saravana Kumar, N.M., Kandala, M.K., Kaveri, P.R. et al. A multi-scale adaptive filtering and AtRes_SRU–transformer synergy for breast cancer histopathology classification. Sci Rep 16, 14387 (2026). https://doi.org/10.1038/s41598-026-41153-7
Ключевые слова: гистопатология рака молочной железы, анализ медицинских изображений, глубокое обучение, модели‑трансформеры, системы поддержки диагностики