Clear Sky Science · nl
Een multi-schaal adaptieve filtering en AtRes_SRU–transformer synergie voor classificatie van borstkanker-histopathologie
Waarom dit belangrijk is voor patiënten en artsen
Het vroegtijdig opsporen van borstkanker kan het verschil betekenen tussen een eenvoudige behandeling en een levensbedreigende ziekte, maar het bekijken van weefsel onder de microscoop is traag en subjectief. Dit artikel presenteert een nieuw computersysteem dat pathologen helpt borstweefselbeelden nauwkeuriger en efficiënter in onschadelijke en gevaarlijke gevallen te sorteren. Door beelden zorgvuldig te reinigen en meerdere vormen van kunstmatige intelligentie te combineren, streeft het systeem ernaar eerdere diagnose te ondersteunen, minder gemiste kankers en minder onnodige alarmen te realiseren.
Het beeld schonen voordat er een oordeel volgt
Microscoopbeelden van borstweefsel zijn verre van perfect. Ze bevatten willekeurige ruis, oneven verlichting en kleurvariaties door kleuring, die zelfs geavanceerde algoritmen kunnen misleiden. De auteurs introduceren een voorspellende stap genaamd multi-schaal adaptieve filtering, die functioneert als een slimme, zachte ruisfilter. In plaats van alles gelijkmatig te vervagen, bekijkt het de afbeelding op meerdere detailniveaus en past het zich aan lokale contrasten en texturen aan. Het resultaat is dat afleidende ruis en kleuringartefacten worden verminderd, terwijl belangrijke randen—zoals grenzen tussen celgroepen—behouden blijven. Dit geeft latere systeemstadia een helder, betrouwbaarder beeld van elk weefselpatch.
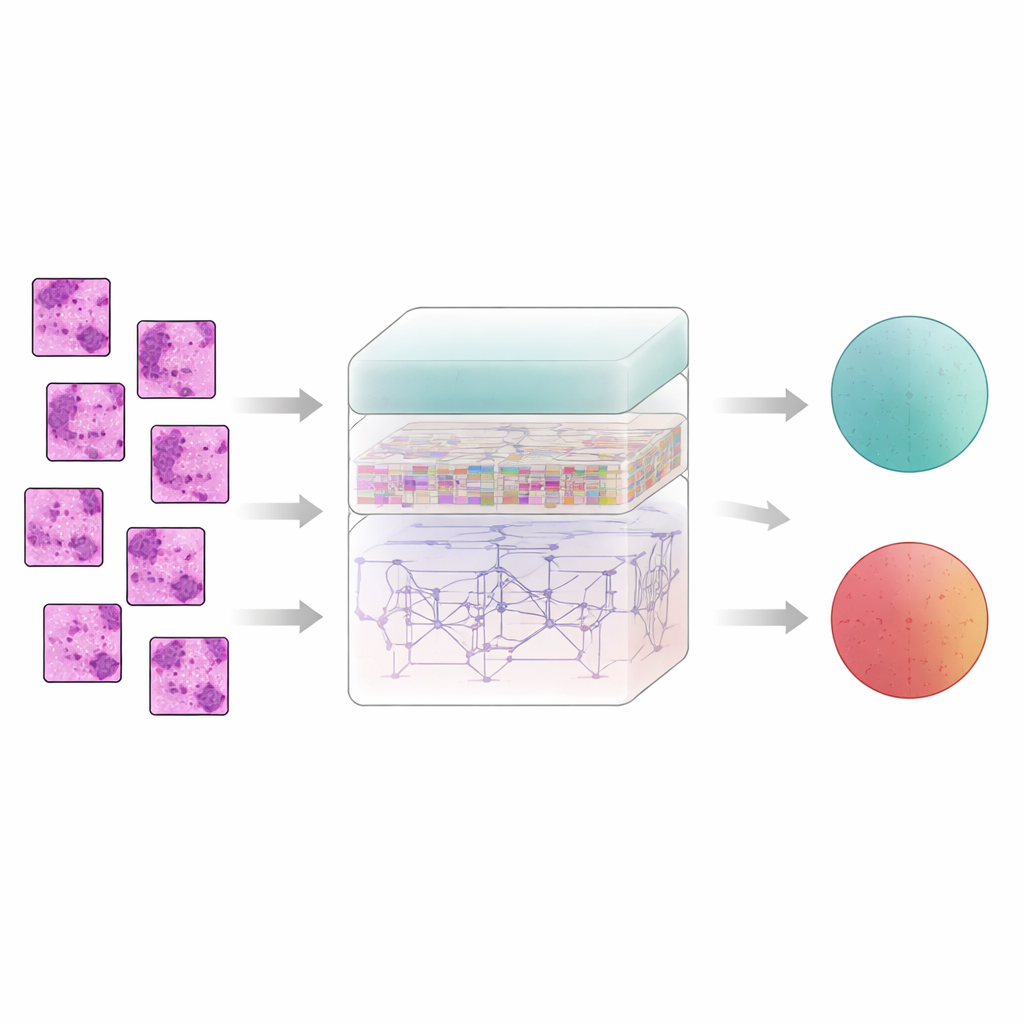
De computer leren weefselpatronen te volgen
Borstweefsel vertelt zijn verhaal niet per pixel; betekenis ontstaat uit hoe aangrenzende gebieden zich tot elkaar verhouden. Om dit vast te leggen, snijdt het systeem elke gefilterde afbeelding in kleine patches en voert die in een feature-extractor genaamd AtRes_SRU. Dit onderdeel combineert een diep residueel netwerk, dat goed is in het herkennen van vormen en texturen, met een lichtgewicht recurrente eenheid die aangrenzende patches behandelt als stappen in een sequentie. Hoewel er niets in de tijd beweegt, laat het ordentelijk rangschikken van patches het model leren hoe structuren over het preparaat vloeien—waar celclusters beginnen en eindigen, hoe klieren buigen of scheuren, en hoe abnormale gebieden zich binnen regelmatiger weefsel bevinden. Een attentiemechanisme stuurt het systeem verder om zich te concentreren op de meest verdachte regio’s, zoals onregelmatige kernen of ongewoon dichte celclusters.
Het hele preparaat zien, niet alleen kleine stukjes
Hoewel lokale patronen belangrijk zijn, onthult kanker zich vaak via grootschaligere organisatie: hoe verspreid abnormale zones zijn, hoe ver ze zich uitstrekken en hoe ze interageren met omliggend weefsel. Om dit bredere beeld te vatten voegen de auteurs een transformermodule toe, een technologie oorspronkelijk ontwikkeld voor taalmodellen. Hier wordt elke patch een token en leert de transformer hoe elke patch zich verhoudt tot alle andere. Een vorm van absolute positiecodering vertelt het model precies waar elke patch vandaan komt in het oorspronkelijke preparaat, waardoor de ruimtelijke indeling behouden blijft. Daarbovenop helpt een dicht verbonden beslissingslaag door kenmerken uit vele dieptes van het netwerk te hergebruiken, zodat het systeem zowel fijne details als globale context in acht neemt wanneer het uiteindelijk beslist of een monster goedaardig of kwaadaardig is.
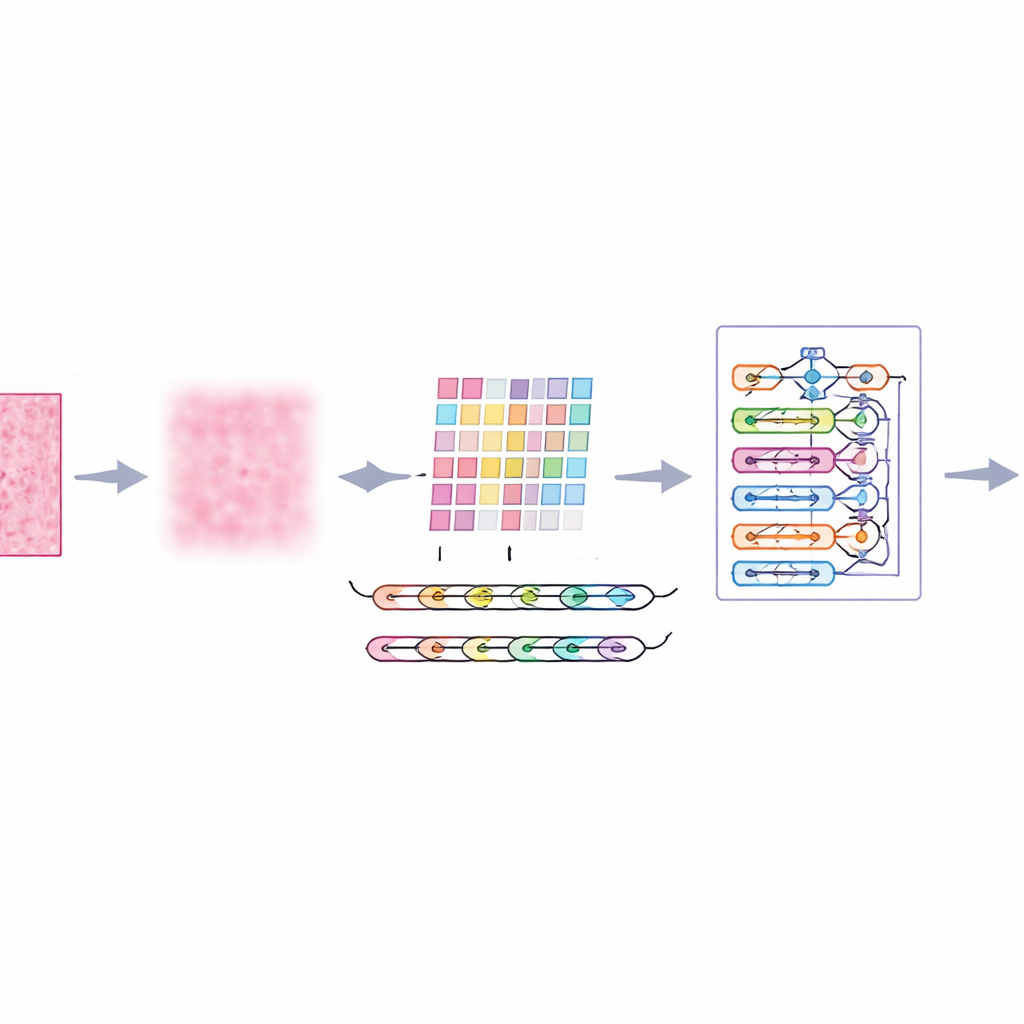
Het systeem aan de tand voelen
De onderzoekers trainden en evalueerden hun "ImTranNet‑TriCore"-kader op een grote openbare verzameling borst-histopathologiebeelden, die meer dan een kwart miljoen kleine patches van echte patiënten bevat, gescand op meerdere vergrotingsniveaus. De dataset is uitdagend: het voorkomen van weefsel varieert sterk tussen preparaten en kwaadaardige gebieden kunnen subtiel zijn of slechts een klein deel van een afbeelding beslaan. Desondanks behaalde het nieuwe systeem ongeveer 98% nauwkeurigheid in het onderscheiden van kankercellen van niet-kankerachtige patches en hield het sterke prestaties op alle zoomniveaus vast. Het presteerde consequent beter dan een reeks veelgebruikte methoden, waaronder conventionele convolutionele netwerken, attentie-versterkte modellen en hybride ontwerpen die deep learning met traditionele machine learning mixen.
Van cijfers naar vertrouwen in echte klinieken
Hoge nauwkeurigheid alleen is niet genoeg voor de geneeskunde; artsen moeten begrijpen waarom een systeem tot zijn beslissingen komt. Daarom onderzochten de auteurs welke beeldregio’s de keuzes van het model het meest beïnvloedden met behulp van heatmaps en toolen voor kenmerkbelang. Ze ontdekten dat het systeem de neiging heeft dezelfde structuren te benadrukken waar pathologen naar kijken: de vormen en grenzen van celkernen, de organisatie van klieren en dichte clusters abnormaal weefsel. Tegelijk houdt het model het aantal valse alarmen laag en geeft het soepel gekalibreerde betrouwbaarheidscores, wat belangrijk is om zowel gemiste kankers als onnodige biopsieën te vermijden. Hoewel de methode nog moeite heeft met sommige zeer fijnmazige verschillen bij extreme vergroting, suggereert de studie dat het combineren van zorgvuldige beeldreiniging, lokaal patroonvolgen en hele-preparaatcontext geautomatiseerde beoordeling van borstkanker veel dichter bij de betrouwbaarheid kan brengen die clinici nodig hebben.
Bronvermelding: Saravana Kumar, N.M., Kandala, M.K., Kaveri, P.R. et al. A multi-scale adaptive filtering and AtRes_SRU–transformer synergy for breast cancer histopathology classification. Sci Rep 16, 14387 (2026). https://doi.org/10.1038/s41598-026-41153-7
Trefwoorden: histopathologie van borstkanker, analyse van medische beelden, deep learning, transformermodelen, computerondersteunde diagnostiek