Clear Sky Science · pl
Wieloskalowe adaptacyjne filtrowanie i synergia AtRes_SRU–transformera do klasyfikacji histopatologii raka piersi
Dlaczego to ma znaczenie dla pacjentów i lekarzy
Wczesne wykrycie raka piersi może decydować o przejściu od prostego leczenia do choroby zagrażającej życiu, a jednocześnie ocena tkanek pod mikroskopem jest pracą powolną i subiektywną. W artykule przedstawiono nowy system komputerowy, który pomaga patologom sortować obrazy tkanek piersi na przypadki niegroźne i niebezpieczne bardziej dokładnie i wydajnie. Poprzez staranne oczyszczanie obrazów i połączenie kilku typów sztucznej inteligencji system ma wspierać wcześniejszą diagnozę, zmniejszać liczbę przeoczonych nowotworów oraz ograniczać niepotrzebne alarmy.
Oczyszczanie obrazu przed wydaniem opinii
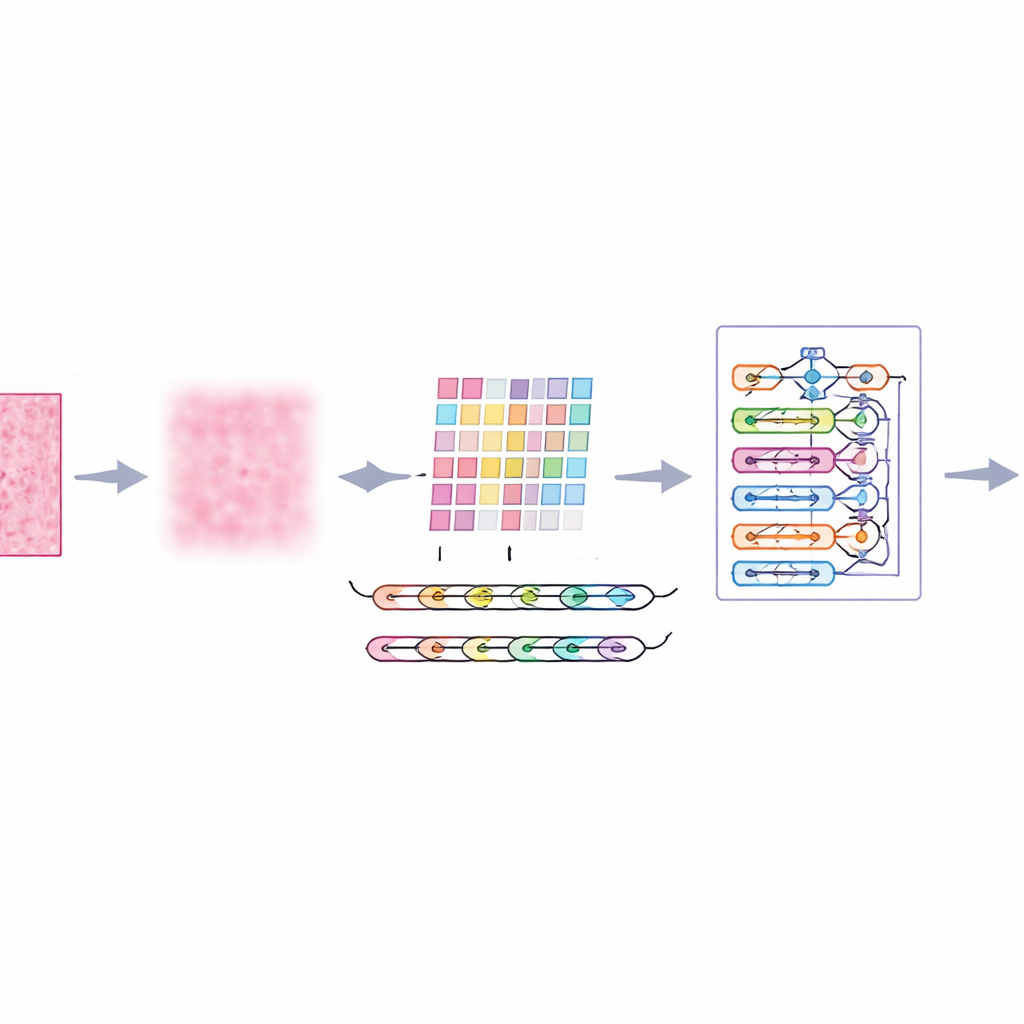
Obrazy mikroskopowe tkanek piersi są dalekie od ideału. Zawierają losowe plamki, nierówne oświetlenie i różnice kolorystyczne wynikające z barwienia, które mogą mylić nawet zaawansowane algorytmy. Autorzy wprowadzają etap wstępny nazwany wieloskalowym adaptacyjnym filtrowaniem, działający jak inteligentny, łagodny filtr przeciwzakłóceniowy. Zamiast jednak zuniformizowanego rozmywania, analizuje obraz na kilku poziomach szczegółu i dostosowuje się do lokalnego kontrastu oraz tekstury. W efekcie zmniejszają się rozpraszające szumy i artefakty barwienia, przy jednoczesnym zachowaniu istotnych krawędzi — na przykład granic między skupiskami komórek. Dzięki temu kolejne etapy systemu otrzymują jaśniejszy, bardziej wiarygodny obraz każdej łatki tkanki.
Nauczanie komputera rozpoznawania wzorów tkankowych
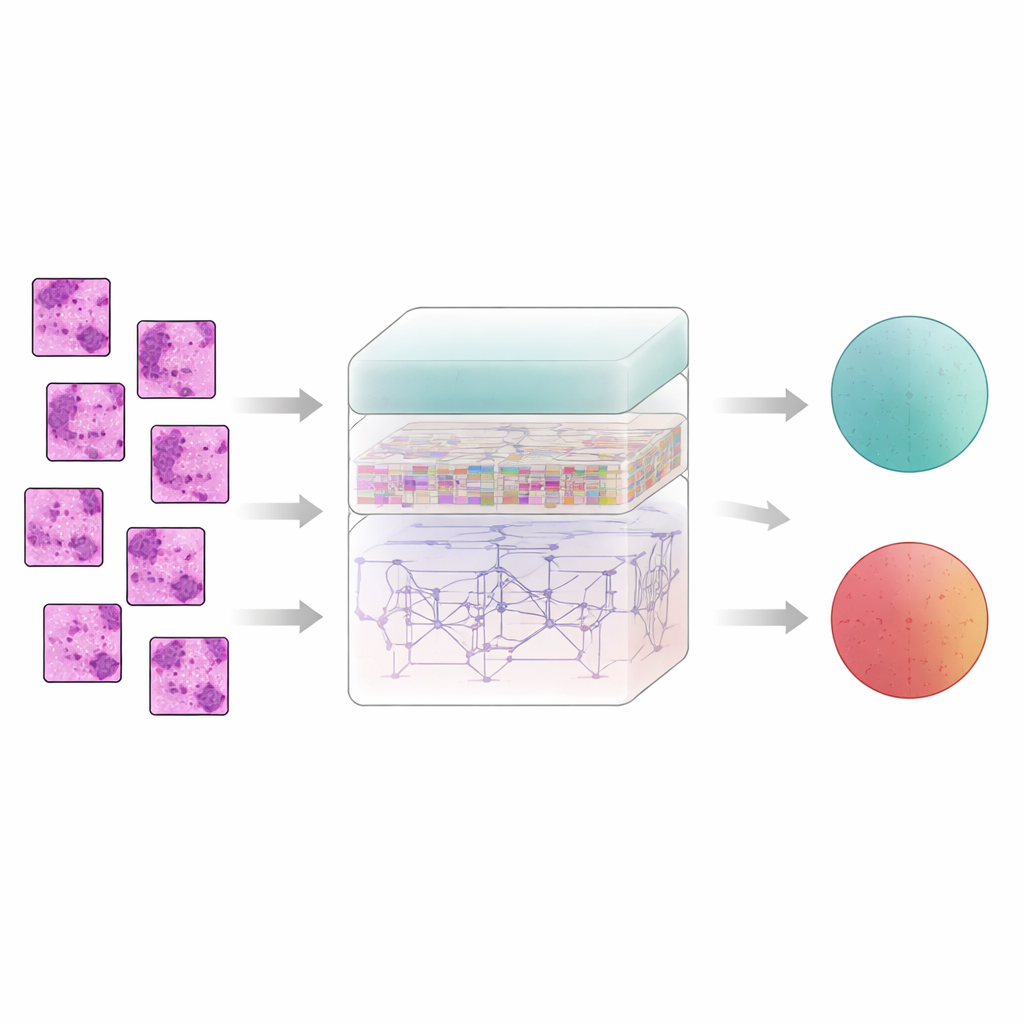
Tkanka piersi nie opowiada swojej historii piksel po pikselu; znaczenie wynika z relacji między sąsiednimi obszarami. Aby to uchwycić, system dzieli każdy przefiltrowany obraz na małe łatki i przekazuje je do ekstraktora cech nazwanego AtRes_SRU. Ta część łączy głęboką sieć rezydualną, dobrą w wykrywaniu kształtów i tekstur, z lekką jednostką rekurencyjną, która traktuje sąsiadujące łatki jak kolejne kroki w sekwencji. Choć nic w czasie się nie porusza, uporządkowanie łatk pozwala modelowi nauczyć się, jak struktury rozciągają się po preparacie — gdzie zaczynają i kończą się skupiska komórek, jak zatoki gruczołowe się wyginają lub przerywają oraz jak obszary nieprawidłowe osadzają się w obrębie bardziej regularnej tkanki. Mechanizm attention dodatkowo kieruje model na najbardziej podejrzane rejony, takie jak nieregularne jądra komórkowe czy nietypowo gęste skupiska komórek.
Widzenie całego preparatu, nie tylko maleńkich fragmentów
Choć lokalne wzory są istotne, rak często ujawnia się poprzez organizację w szerszej skali: jak rozproszone są strefy nieprawidłowe, jak szeroko się rozprzestrzeniają i jak wchodzą w interakcje z otaczającą tkanką. Aby uchwycić ten szerszy obraz, autorzy dodają moduł transformera, technologię opracowaną pierwotnie dla modeli językowych. Tutaj każda łatka staje się tokenem, a transformer uczy się, jak każda łatka odnosi się do wszystkich pozostałych. Forma absolutnego kodowania pozycji mówi modelowi dokładnie, skąd dana łatka pochodzi w oryginalnym preparacie, zachowując układ przestrzenny. Na to nakłada się gęsto połączona warstwa decyzyjna, która ponownie wykorzystuje cechy z różnych głębokości sieci, pomagając systemowi zachować zarówno drobne detale, jak i kontekst globalny przy ostatecznym rozstrzyganiu, czy próbka jest łagodna czy złośliwa.
Testowanie systemu
Naukowcy trenowali i oceniali swój framework „ImTranNet‑TriCore” na dużym publicznym zbiorze obrazów histopatologicznych piersi, obejmującym ponad ćwierć miliona małych łatk pochodzących od prawdziwych pacjentów, skanowanych na kilku poziomach powiększenia. Zbiór danych jest wymagający: wygląd tkanek różni się znacznie między preparatami, a obszary złośliwe mogą być subtelne lub zajmować tylko małą część obrazu. Mimo to nowy system osiągnął około 98% trafności w rozróżnianiu łatk nowotworowych od nienowotworowych i utrzymał wysoką wydajność na wszystkich poziomach powiększenia. System konsekwentnie przewyższał szereg powszechnie stosowanych metod, w tym konwencjonalne sieci konwolucyjne, modele z wzmocnioną uwagą oraz hybrydowe rozwiązania łączące uczenie głębokie z tradycyjnym uczeniem maszynowym.
Od liczb do zaufania w rzeczywistych klinikach
Sama wysoka dokładność nie wystarczy w medycynie; lekarze muszą rozumieć, dlaczego system podejmuje określone decyzje. Autorzy zatem zbadali, które rejony obrazu miały największy wpływ na wybory modelu, używając map cieplnych i narzędzi oceny ważności cech. Stwierdzili, że system zwykle podkreśla te same struktury, na które zwracają uwagę patolodzy: kształty i granice jąder komórkowych, organizację gruczołów oraz gęste skupiska nieprawidłowej tkanki. Jednocześnie model utrzymuje niską liczbę fałszywych alarmów i wykazuje płynnie skalibrowane oceny pewności, co jest ważne, by unikać zarówno przeoczonych nowotworów, jak i niepotrzebnych biopsji. Chociaż metoda wciąż ma trudności z niektórymi bardzo drobnymi różnicami przy skrajnych powiększeniach, badanie sugeruje, że połączenie starannego oczyszczania obrazu, śledzenia lokalnych wzorców i kontekstu całego preparatu może przybliżyć automatyczną ocenę raka piersi do niezawodności wymaganej przez klinicystów.
Cytowanie: Saravana Kumar, N.M., Kandala, M.K., Kaveri, P.R. et al. A multi-scale adaptive filtering and AtRes_SRU–transformer synergy for breast cancer histopathology classification. Sci Rep 16, 14387 (2026). https://doi.org/10.1038/s41598-026-41153-7
Słowa kluczowe: histopatologia raka piersi, analiza obrazów medycznych, uczenie głębokie, modele transformerowe, wspomaganie diagnostyki komputerowej