Clear Sky Science · pt
Filtragem adaptativa multiescala e sinergia AtRes_SRU–transformer para classificação histopatológica do câncer de mama
Por que isso importa para pacientes e médicos
Detectar o câncer de mama precocemente pode ser a diferença entre um tratamento simples e uma doença com risco de vida, mas analisar tecido ao microscópio é um trabalho lento e subjetivo. Este artigo apresenta um novo sistema computacional que ajuda patologistas a classificar imagens de tecido mamário em casos benignos e perigosos de maneira mais precisa e eficiente. Ao limpar cuidadosamente as imagens e combinar vários tipos de inteligência artificial, o sistema busca apoiar diagnósticos mais precoces, reduzir cânceres não detectados e diminuir alarmes desnecessários.
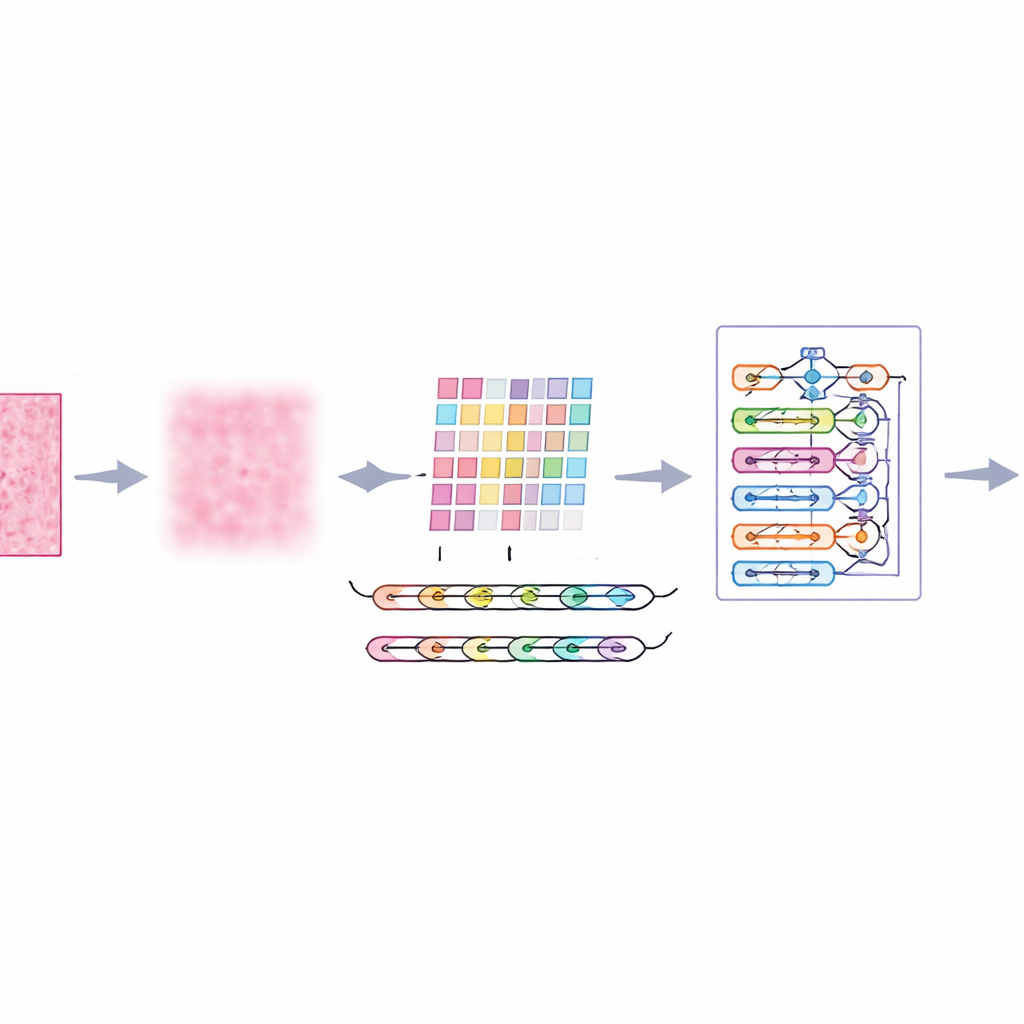
Limpar a imagem antes de tomar uma decisão
Imagens microscópicas de tecido mamário estão longe de ser perfeitas. Contêm manchas aleatórias, iluminação irregular e variações de cor devido à coloração, tudo isso pode confundir até algoritmos avançados. Os autores introduzem um passo de pré‑processamento chamado filtragem adaptativa multiescala, que funciona como um filtro de ruído inteligente e suave. Em vez de borrar tudo igualmente, ele analisa a imagem em vários níveis de detalhe e se adapta ao contraste e à textura locais. O resultado é a redução de ruídos e artefatos de coloração que distraem, enquanto bordas importantes — como limites entre grupos de células — são preservadas. Isso fornece às etapas posteriores do sistema uma visão mais clara e confiável de cada pedaço de tecido.
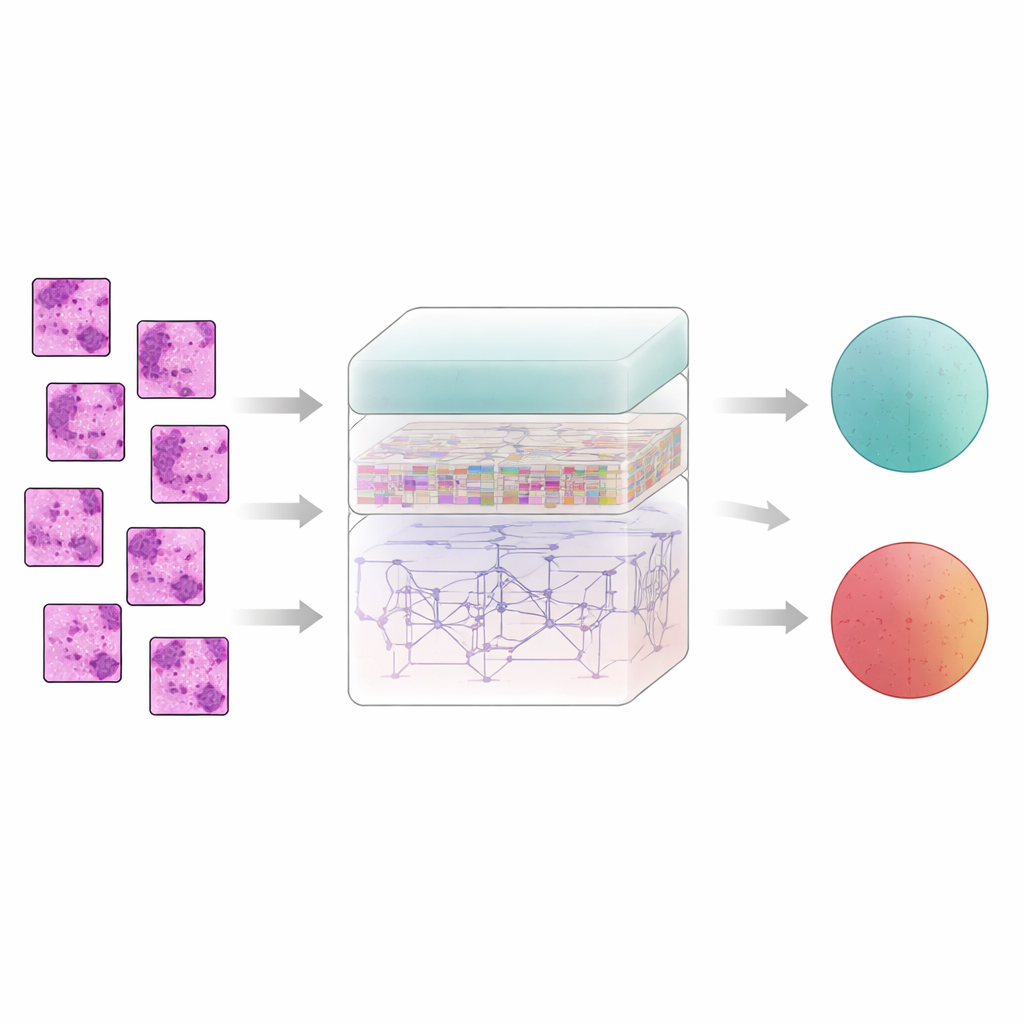
Ensinar o computador a seguir padrões no tecido
O tecido mamário não revela sua história pixel por pixel; o significado surge de como regiões vizinhas se relacionam. Para capturar isso, o sistema divide cada imagem filtrada em pequenos blocos e os alimenta em um extrator de características chamado AtRes_SRU. Essa parte combina uma rede residual profunda, boa em detectar formas e texturas, com uma unidade recorrente leve que trata blocos adjacentes como passos em uma sequência. Embora nada esteja se movendo no tempo, ordenar os blocos permite ao modelo aprender como as estruturas se estendem pelo preparado — onde aglomerados celulares começam e terminam, como glândulas se curvam ou se rompem, e como regiões anormais se situam dentro de tecido mais regular. Um mecanismo de atenção orienta ainda mais o sistema a focar nas regiões mais suspeitas, como núcleos irregulares ou aglomerados celulares incomumente densos.
Ver o preparado inteiro, não apenas pequenos pedacinhos
Enquanto padrões locais importam, o câncer frequentemente se revela pela organização em maior escala: como zonas anormais estão dispersas, quão amplas são e como interagem com o tecido ao redor. Para apreender esse panorama, os autores adicionam um módulo transformer, tecnologia originalmente desenvolvida para modelos de linguagem. Aqui, cada bloco vira um token, e o transformer aprende como cada bloco se relaciona com todos os outros. Uma forma de codificação de posição absoluta informa ao modelo exatamente de onde cada bloco veio no preparado original, preservando a disposição espacial. Sobre isso, uma camada de decisão densamente conectada reutiliza características de várias profundidades da rede, ajudando o sistema a manter em mente tanto detalhes finos quanto contexto global ao decidir, finalmente, se uma amostra é benigna ou maligna.
Submetendo o sistema ao teste
Os pesquisadores treinaram e avaliaram o arcabouço "ImTranNet‑TriCore" em uma grande coleção pública de imagens histopatológicas de mama, que inclui mais de um quarto de milhão de pequenos blocos de pacientes reais, digitalizados em vários níveis de ampliação. O conjunto de dados é desafiador: a aparência do tecido varia amplamente entre preparados, e regiões malignas podem ser sutis ou ocupar apenas uma pequena parte da imagem. Apesar disso, o novo sistema alcançou cerca de 98% de acurácia ao distinguir blocos cancerosos de não cancerosos e manteve desempenho forte em todos os níveis de zoom. Ele superou consistentemente uma gama de métodos amplamente usados, incluindo redes convolucionais convencionais, modelos com atenção aprimorada e projetos híbridos que misturam aprendizado profundo com aprendizagem de máquina tradicional.
Dos números à confiança em clínicas reais
Alta acurácia por si só não basta na medicina; os médicos precisam entender por que um sistema toma suas decisões. Por isso, os autores examinaram quais regiões da imagem mais influenciaram as escolhas do modelo usando mapas de calor e ferramentas de importância de características. Eles constataram que o sistema tende a destacar as mesmas estruturas que os patologistas observam: formas e contornos dos núcleos celulares, organização das glândulas e aglomerados densos de tecido anormal. Ao mesmo tempo, o modelo mantém baixos os falsos positivos e apresenta scores de confiança calibrados de forma suave, o que é importante para evitar tanto cânceres perdidos quanto biópsias desnecessárias. Embora o método ainda tenha dificuldades com algumas diferenças muito sutis em ampliações extremas, o estudo sugere que combinar limpeza cuidadosa da imagem, rastreamento de padrões locais e contexto de todo o preparado pode aproximar bastante a avaliação automatizada do câncer de mama da confiabilidade necessária para uso clínico.
Citação: Saravana Kumar, N.M., Kandala, M.K., Kaveri, P.R. et al. A multi-scale adaptive filtering and AtRes_SRU–transformer synergy for breast cancer histopathology classification. Sci Rep 16, 14387 (2026). https://doi.org/10.1038/s41598-026-41153-7
Palavras-chave: histopatologia do câncer de mama, análise de imagens médicas, aprendizado profundo, modelos transformer, diagnóstico assistido por computador