Clear Sky Science · sv
En flerskalig adaptiv filtrering och AtRes_SRU–transformer‑synergi för klassificering av bröstcancer i histopatologi
Varför detta är viktigt för patienter och läkare
Att upptäcka bröstcancer tidigt kan vara skillnaden mellan en enkel behandling och ett livshotande sjukdomsförlopp, men att granska vävnad i mikroskop är ett långsamt och subjektivt arbete. Denna artikel presenterar ett nytt datorstöd som hjälper patologer att sortera bilder av bröstvävnad i ofarliga och farliga fall mer träffsäkert och effektivt. Genom att noggrant rengöra bilderna och kombinera flera typer av artificiell intelligens syftar systemet till att stödja tidigare diagnoser, färre förbisedda cancrar och färre onödiga larm.
Rengör bilden innan beslut fattas
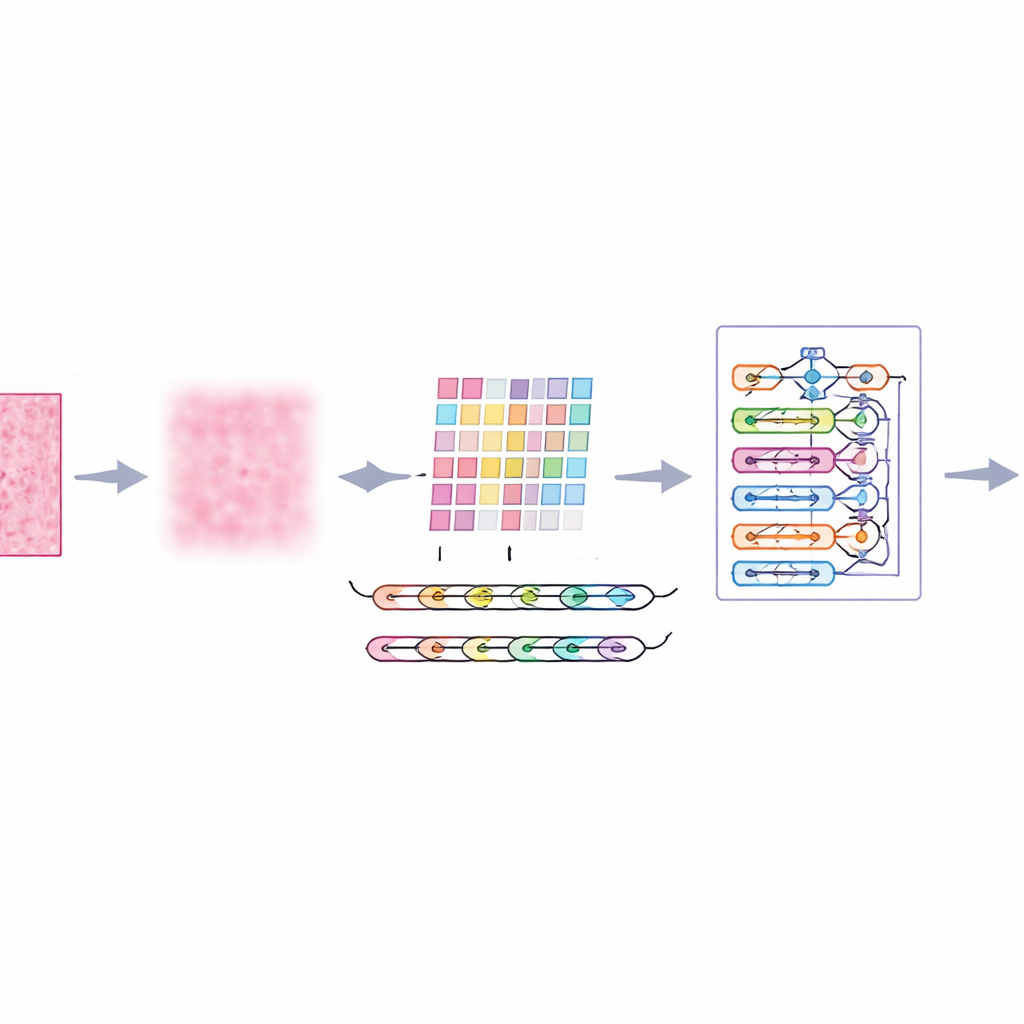
Mikroskopbilder av bröstvävnad är långt ifrån perfekta. De innehåller slumpmässiga prickar, ojämn belysning och färgvariationer från färgning, vilket kan vilseleda även avancerade algoritmer. Författarna introducerar ett förbehandlingssteg kallat flerskalig adaptiv filtrering, som fungerar som ett smart, mjukt brusfilter. Istället för att sudda ut allt lika ser det på bilden på flera detaljnivåer och anpassar sig efter lokal kontrast och struktur. Resultatet är att störande brus och färgningsartefakter reduceras medan viktiga kanter — som gränser mellan cellgrupper — bevaras. Det ger senare delar av systemet en tydligare och mer pålitlig bild av varje vävnadspatch.
Lära datorn följa vävnadsmönster
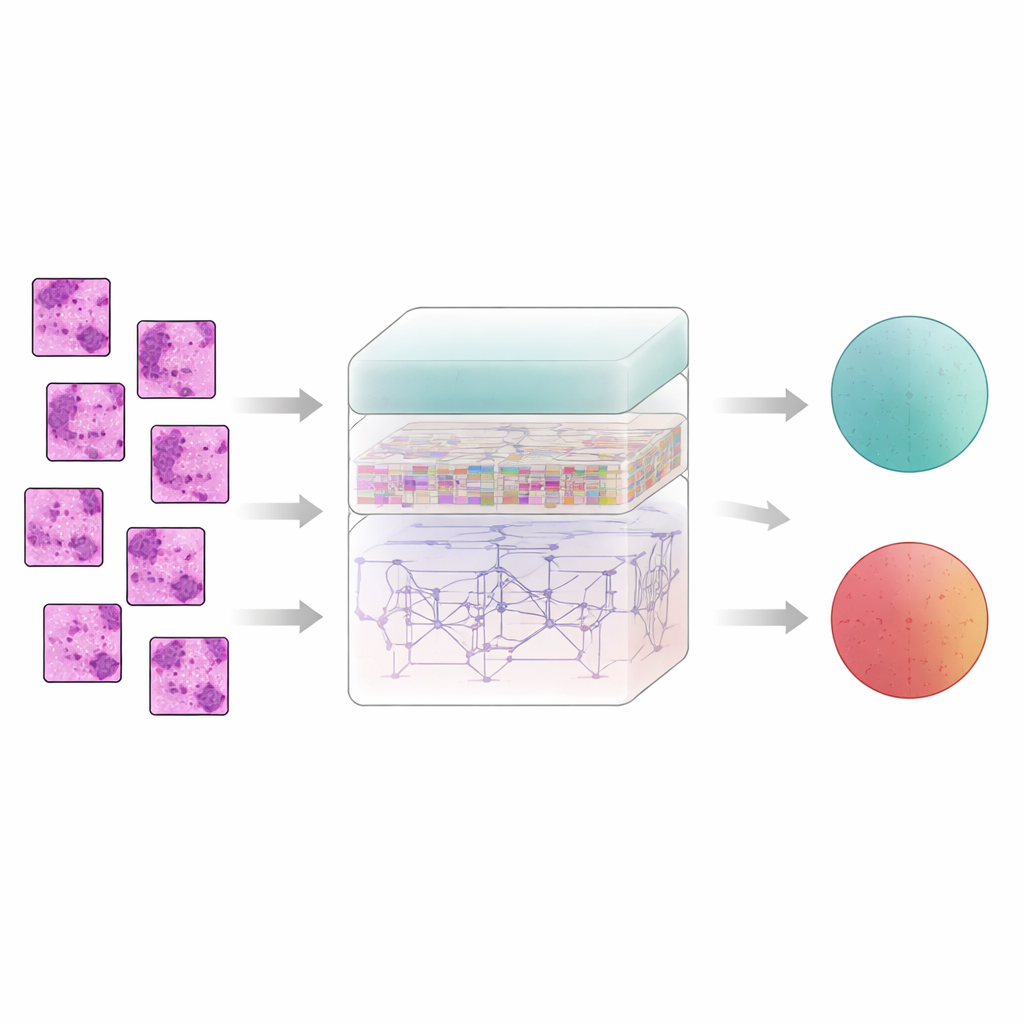
Bröstvävnad berättar inte sin historia en pixel i taget; mening uppstår ur hur närliggande områden förhåller sig till varandra. För att fånga detta delar systemet upp varje filtrerad bild i små patchar och matar dem till en funktionsextraktor kallad AtRes_SRU. Denna del kombinerar ett djupt residualnätverk, som är bra på att känna igen former och texturer, med en lättvikts rekurrent enhet som behandlar intilliggande patchar som steg i en sekvens. Även om inget rör sig i tiden låter ordningen av patcharna modellen lära sig hur strukturer flyter över preparatet — var cellkluster börjar och slutar, hur körtlar böjer sig eller bryts upp, och hur avvikande områden ligger i förhållande till mer regelbunden vävnad. En uppmärksamhetsmekanism riktar dessutom systemet mot de mest misstänkta regionerna, såsom oregelbundna cellkärnor eller ovanligt täta cellkluster.
Se hela snittet, inte bara små bitar
Medan lokala mönster är viktiga visar sig cancer ofta genom större skala: hur utspridda avvikande zoner är, hur vida de breder ut sig och hur de interagerar med omkringliggande vävnad. För att förstå denna bredare bild lägger författarna till en transformer‑modul, en teknik som ursprungligen utvecklades för språkmodeller. Här blir varje patch ett token och transformern lär sig hur varje patch förhåller sig till varje annan. En form av absolut positionskodning talar om för modellen exakt var varje patch kom ifrån i originalpreparatet och bevarar den spatiala layouten. Ovanpå detta hjälper ett tätt sammankopplat beslutslager som återanvänder funktioner från många nivåer i nätverket systemet att hålla både fina detaljer och global kontext i åtanke när det slutligen avgör om ett prov är benign eller malign.
Sätta systemet på prov
Forskarlaget tränade och utvärderade sin ramverk "ImTranNet‑TriCore" på en stor offentlig samling av histopatologiska bilder av bröstvävnad, som innehåller mer än en kvart miljon små patchar från verkliga patienter, skannade vid flera förstoringsnivåer. Datamängden är utmanande: vävnadens utseende varierar mycket mellan preparat och maligna områden kan vara subtila eller endast upptar en liten del av bilden. Trots detta uppnådde det nya systemet cirka 98 % noggrannhet i att skilja cancerösa från icke‑cancerösa patchar och bibehöll stark prestanda över alla zoomnivåer. Det överträffade konsekvent en rad välanvända metoder, inklusive konventionella konvolutionsnätverk, uppmärksamhetsförstärkta modeller och hybriddesigner som blandar djupinlärning med traditionell maskininlärning.
Från siffror till förtroende i kliniken
Hög noggrannhet räcker inte för medicin; läkare behöver förstå varför ett system når sina slutsatser. Författarna undersökte därför vilka bildregioner som påverkade modellens val mest med hjälp av värmekartor och verktyg för funktions‑viktning. De fann att systemet tenderar att lyfta fram samma strukturer som patologer tittar på: former och gränser hos cellkärnor, körtelorganisation och täta kluster av avvikande vävnad. Samtidigt håller modellen falsklarmen låga och uppvisar jämnt kalibrerade konfidenspoäng, vilket är viktigt för att undvika både missade cancrar och onödiga biopsier. Även om metoden fortfarande har problem med vissa mycket finfördelade skillnader vid extrem förstoringsgrad tyder studien på att kombinationen av noggrann bildrengöring, lokal mönsterföljning och helpreparatskontext kan föra automatisk bedömning av bröstcancer mycket närmare den tillförlitlighet kliniker kräver.
Citering: Saravana Kumar, N.M., Kandala, M.K., Kaveri, P.R. et al. A multi-scale adaptive filtering and AtRes_SRU–transformer synergy for breast cancer histopathology classification. Sci Rep 16, 14387 (2026). https://doi.org/10.1038/s41598-026-41153-7
Nyckelord: histopatologi vid bröstcancer, medicinsk bildanalys, djupinlärning, transformermodeller, datorstödd diagnostik