Clear Sky Science · zh
喹啉羧酸衍生物作为有效的外核苷酸酶抑制剂
为何平息癌症的“危险信号”至关重要
癌症不仅仅是生长;它也学会了隐藏。它常用的一招就是把受压细胞释放的自然危险信号转换为一种让免疫系统沉睡的抚慰性化学物质。本文探讨了一类旨在破坏这一逃逸通路的新型小分子,长期目标是帮助机体自身防御更好地识别并攻击肿瘤。
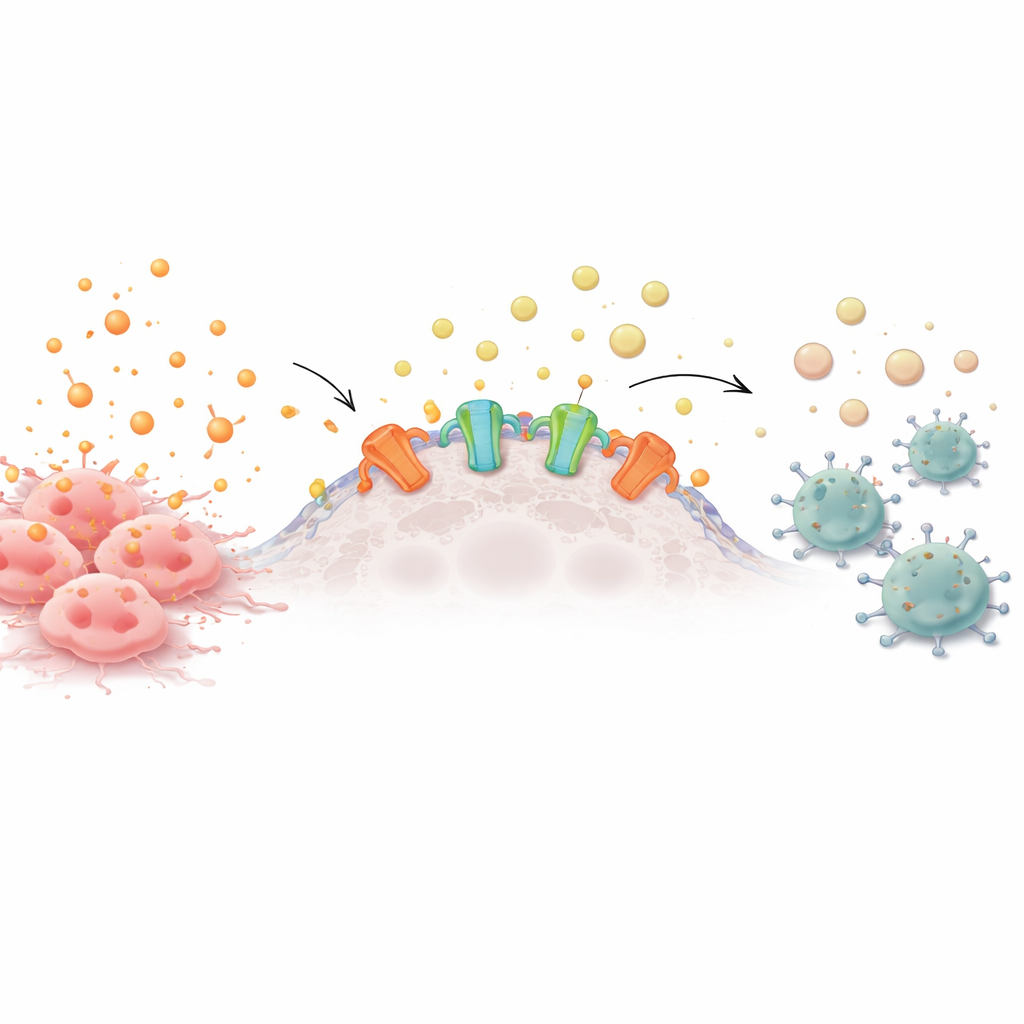
从警报钟到化学沉默
健康和癌变的细胞不断向周围释放携能分子。当这些分子(例如ATP)在细胞外积累时,它们像警报钟一样,吸引免疫细胞前来调查异常。然而,许多肿瘤细胞表面存在一种称为外核苷酸酶的酶,它们将ATP持续切割成腺苷——一种告诉免疫细胞撤退的抚慰信号。许多侵袭性癌症过度表达这些酶,形成一层保护性的腺苷云,削弱附近的T细胞、自然杀伤细胞和其他免疫防御者。
设计新的化学阻断剂
研究者着手设计并合成了一组以喹啉“核心”为骨架的十二种相关化合物——喹啉为平面环状结构,已知能与生物靶点相互作用并具有抗癌潜力。通过向该核心引入不同化学基团,他们构建了一个喹啉-6-羧酰胺衍生物的小型库。这些分子用标准化学方法进行了结构和纯度鉴定,然后在体外针对若干关键外核苷酸酶进行了测试,包括四种处理ATP及相关底物的成员,以及两种完成生成腺苷最后一步的酶。
寻找最有效的酶抑制者
当这些新分子与纯化的人源酶在实验室中混合测试时,有几种显示出强效抑制作用。其中一种标记为4d的化合物在极低浓度下就能强力抑制两种ATP处理酶(h-NTPDase1和h-NTPDase2),显示出作为广谱抑制剂的潜力。其他衍生物则表现出更具选择性的特性:化合物4a强效抑制负责生成腺苷的最后一步的ecto-5′-nucleotidase;4k在抑制另一种酶ENPP1方面表现最佳;而4b和4g则对不同的NTPDase亚型尤为有效。通过比较哪些化学取代基增强或削弱了活性,团队绘制出小幅结构变化如何显著调整酶抑制强度与选择性的图谱。
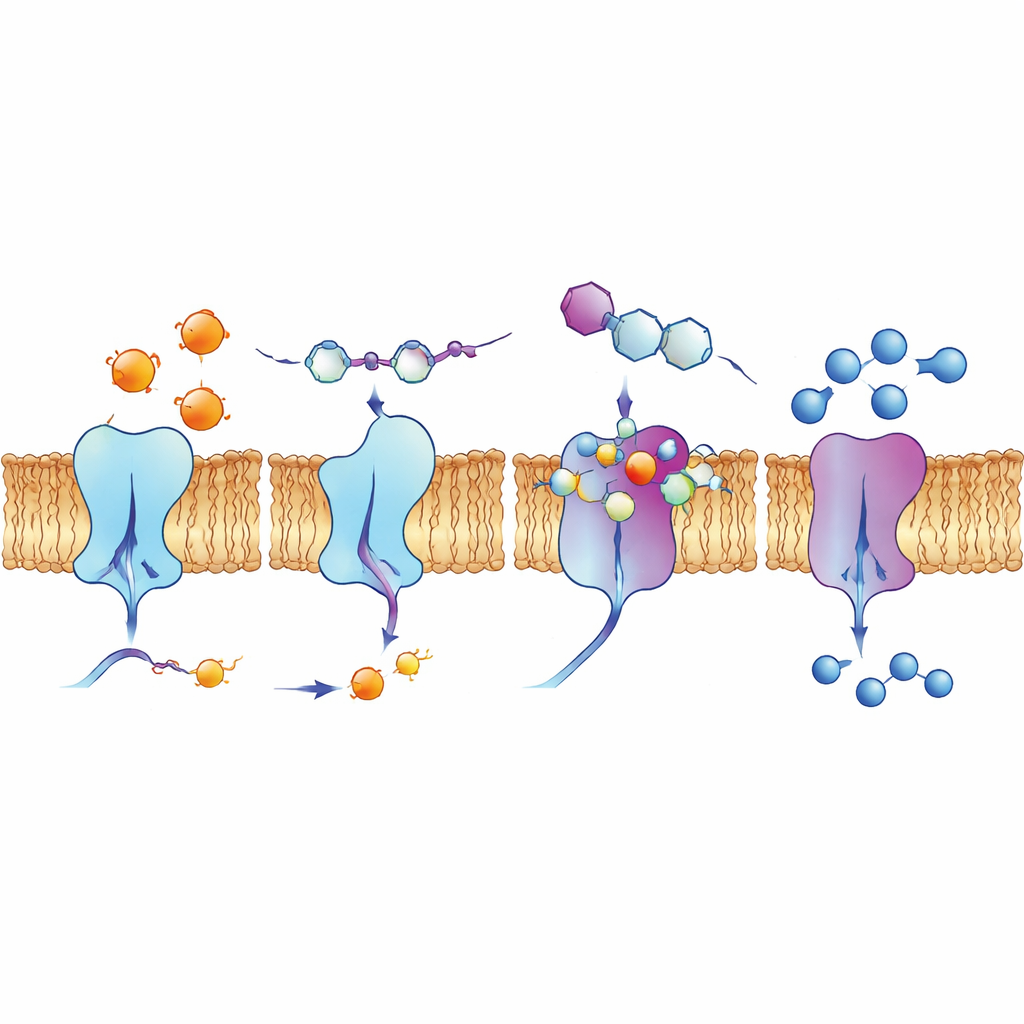
探查结合口袋与活细胞内的行为
为理解为何某些化合物效果显著,作者使用了基于计算的对接模拟和量子化学计算。这些模型显示喹啉基分子如何嵌入酶表面的沟槽,形成吸引力网络,包括氢键、平面环之间的堆积作用,以及涉及氟、氯或碘等卤素的相互作用。电子分布计算支持这样一个观点:最活性的化合物具有适当的稳定性与反应性平衡,能够与酶中的带电位点发生相互作用。团队还用荧光方法研究了一个先导化合物4d在人类肺癌细胞中的行为。该化合物在特定光照下会自然发光,成像显示它在细胞膜处富集——正是外核苷酸酶所在的位置,提示它能够在真实的生物环境中到达其预期靶点。
向抗癌作用迈出的早期步伐
因为有用的药物不仅要命中靶点,还要影响癌细胞生长,研究者评估了这些新分子对培养的乳腺癌细胞的影响。若干衍生物,尤其是4j和4k,降低了细胞存活并随时间减慢了细胞分裂,尽管其效力不及标准化疗药物。对吸收、分布及基本类药性进行的计算评估表明,大多数化合物具有与口服给药兼容的性质,并可能穿透血脑屏障,这为未来在难治肿瘤中的应用提供了可能性。
这对未来癌症疗法意味着什么
总体而言,该研究引入了一类新型喹啉基分子,能够有效阻断将免疫刺激信号转化为免疫抑制腺苷的酶。虽然这些化合物仍处于早期阶段,对癌细胞的直接杀伤作用仅为中等,但它们作为重塑肿瘤微环境的有前景工具,可以使机体自身免疫细胞更有效地发挥作用。通过进一步改进以提高效力和选择性,此类外核苷酸酶抑制剂有望成为现有免疫治疗的补充,帮助消除屏蔽肿瘤免受攻击的化学“雾”。
引用: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
关键词: 癌症免疫治疗, 腺苷信号传导, 酶抑制剂, 喹啉化合物, 肿瘤微环境