Clear Sky Science · fr
Dérivés d’acide quinoline-carboxylique comme inhibiteurs puissants des éctonucléotidases
Pourquoi il est important d’atténuer le « signal de danger » du cancer
Le cancer ne se contente pas de croître ; il apprend aussi à se dissimuler. L’une de ses ruses favorites consiste à transformer un signal naturel de danger libéré par des cellules stressées en une molécule apaisante qui assoupit le système immunitaire. Cet article examine une nouvelle famille de petites molécules visant à perturber cette voie d’évasion, avec pour objectif à long terme d’aider les défenses de l’organisme à mieux reconnaître et attaquer les tumeurs.
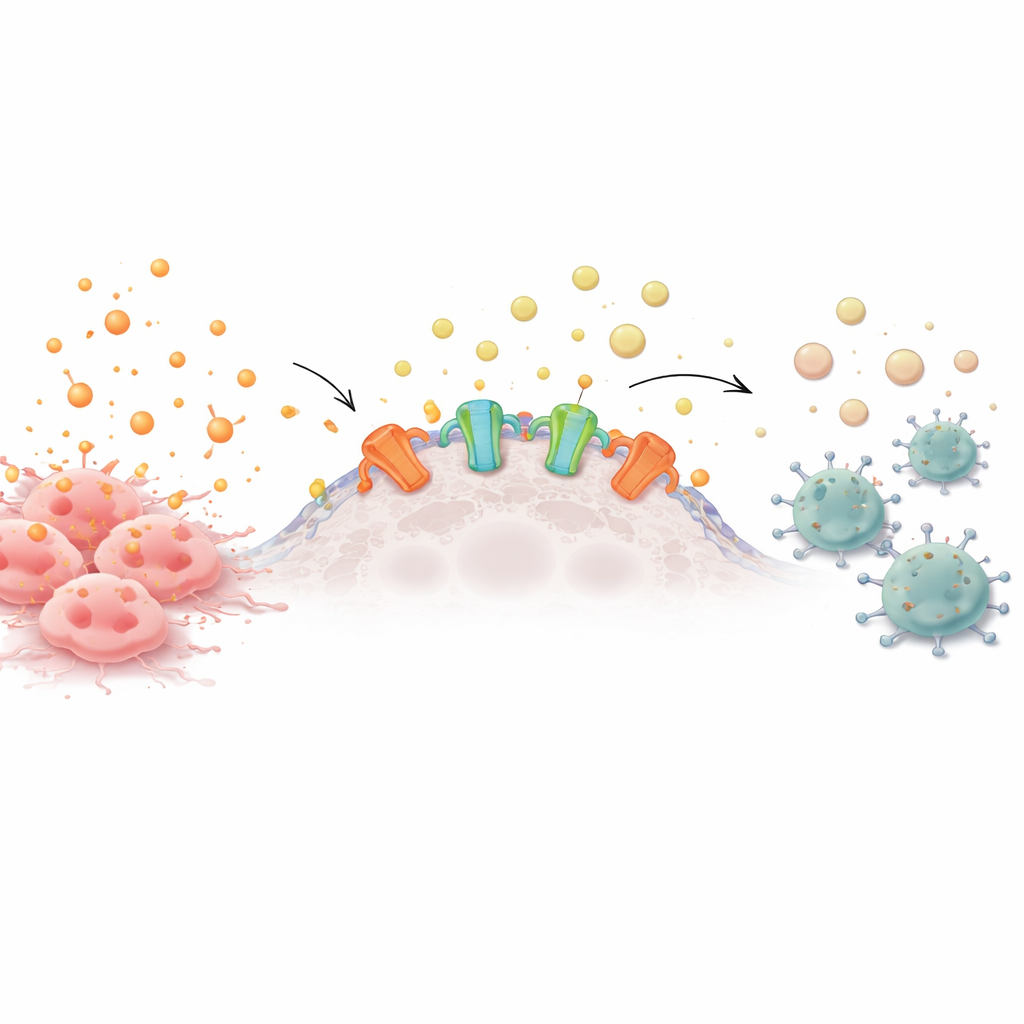
Des sonnettes d’alarme au silence chimique
Les cellules saines et cancéreuses libèrent en permanence des molécules porteuses d’énergie dans leur environnement. Lorsque ces molécules, comme l’ATP, s’accumulent à l’extérieur des cellules, elles jouent le rôle de sonnettes d’alarme, attirant les cellules immunitaires pour enquêter. À la surface de nombreuses cellules tumorales, cependant, se trouvent des enzymes appelées éctonucléotidases qui dégradent progressivement l’ATP en adénosine, un signal calmant qui ordonne aux cellules immunitaires de se calmer. De nombreux cancers agressifs surproduisent ces enzymes, créant un nuage protecteur d’adénosine qui affaiblit les lymphocytes T, les cellules tueuses naturelles et d’autres défenseurs à proximité.
Concevoir de nouveaux bloqueurs chimiques
Les chercheurs se sont attachés à concevoir et synthétiser une série de douze composés apparentés fondés sur un « cœur » quinoline, une structure plate en anneau déjà connue pour interagir avec des cibles biologiques et avoir un potentiel anticancéreux. En greffant différents groupes chimiques sur ce noyau, ils ont créé une petite bibliothèque de dérivés de la quinoline-6-carboxamide. Ces molécules ont été caractérisées avec soin à l’aide d’outils chimiques standard pour confirmer leur structure et leur pureté, puis testées contre plusieurs éctonucléotidases clés, y compris quatre membres traitant l’ATP et des substrats associés, ainsi que deux enzymes réalisant la dernière étape de formation de l’adénosine.
Identifier les inhibiteurs enzymatiques les plus efficaces
Lorsque les nouvelles molécules ont été mises en présence d’enzymes humaines purifiées en laboratoire, plusieurs se sont distinguées comme de puissants bloqueurs. Un composé, désigné 4d, a inhibé de manière puissante deux enzymes traitant l’ATP (h-NTPDase1 et h-NTPDase2) à des concentrations très faibles, le classant comme un inhibiteur prometteur à large spectre. D’autres dérivés ont montré un comportement plus sélectif : le composé 4a bloquait fortement l’ecto-5′-nucléotidase, qui effectue la dernière coupure produisant l’adénosine ; le composé 4k était le meilleur pour bloquer une autre enzyme, ENPP1 ; et les composés 4b et 4g étaient particulièrement efficaces contre différents sous-types de NTPDase. En comparant quelles modifications chimiques amélioraient ou affaiblissaient l’activité, l’équipe a cartographié comment de petits changements de structure peuvent moduler de façon marquée la puissance et la sélectivité de l’inhibition enzymatique.
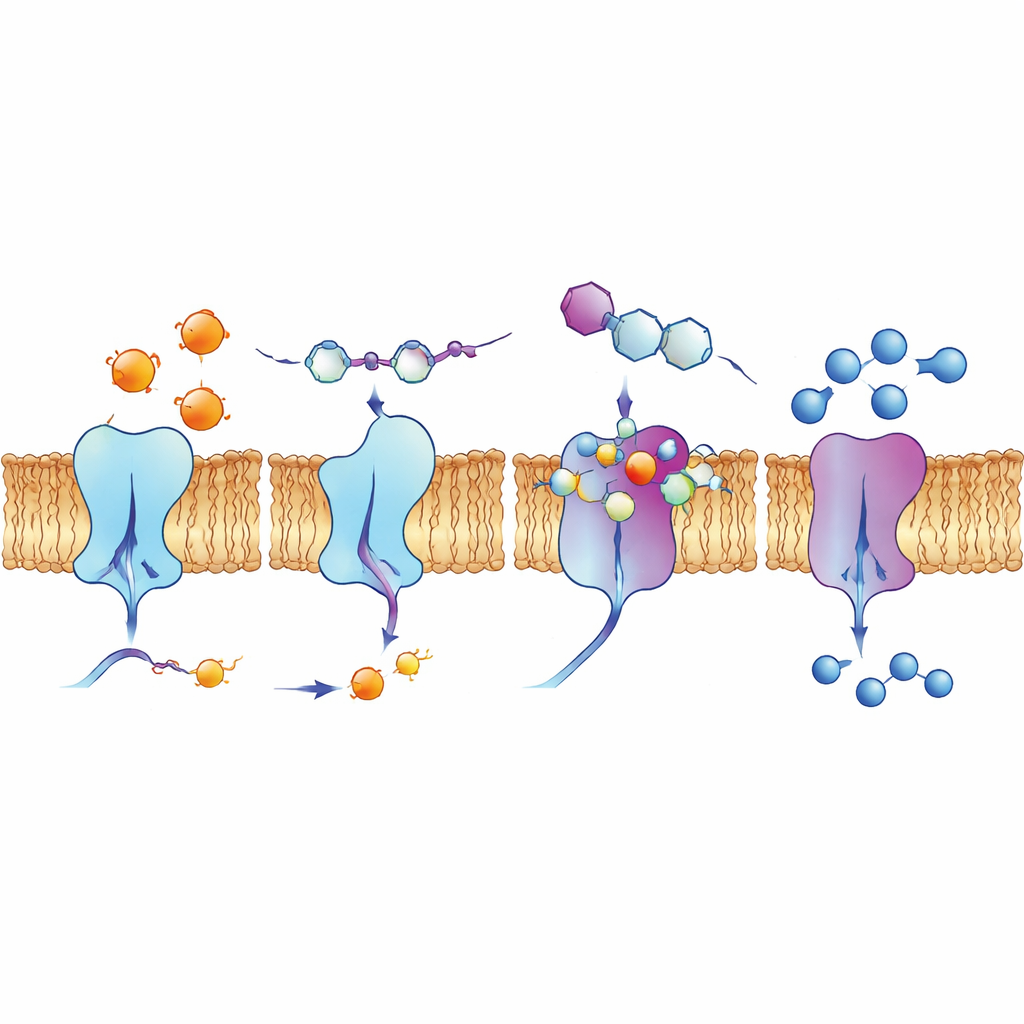
Observer les poches de liaison et les cellules vivantes
Pour comprendre pourquoi certains composés fonctionnaient si bien, les auteurs ont utilisé des simulations de docking informatiques et des calculs de chimie quantique. Ces modèles ont montré comment les molécules à base de quinoline s’insèrent dans des sillons à la surface des enzymes, formant des réseaux de forces attractives, incluant des liaisons hydrogène, des empilements entre anneaux plats et des interactions impliquant des halogènes comme le fluor, le chlore ou l’iode. Les calculs de distribution électronique soutiennent l’idée que les composés les plus actifs présentent le bon équilibre de stabilité et de réactivité pour engager des sites chargés dans les enzymes. L’équipe a également examiné le comportement d’un composé principal, 4d, dans des cellules de cancer du poumon humain en utilisant des méthodes de fluorescence. Il émet naturellement de la lumière sous une certaine excitation, et l’imagerie a révélé qu’il se concentre le long de la membrane cellulaire, lieu même des éctonucléotidases, ce qui suggère qu’il peut atteindre ses cibles prévues dans un contexte biologique réaliste.
Premiers pas vers une action anticancéreuse
Parce qu’un médicament utile doit non seulement atteindre sa cible mais aussi affecter la croissance des cellules cancéreuses, les chercheurs ont évalué comment les nouvelles molécules influencent des cellules de cancer du sein cultivées. Plusieurs dérivés, en particulier 4j et 4k, ont réduit la survie cellulaire et ralenti la division cellulaire au fil du temps, bien que moins efficacement qu’un médicament de chimiothérapie standard. Des évaluations informatiques de l’absorption, de la distribution et des propriétés pharmaceutiques de base suggèrent que la plupart des composés possèdent des caractéristiques compatibles avec une administration orale et peuvent potentiellement atteindre le cerveau, ouvrant la possibilité d’applications futures contre des tumeurs difficiles à traiter.
Ce que cela signifie pour les thérapies anticancéreuses à venir
Globalement, l’étude présente une nouvelle famille de molécules à base de quinoline qui bloquent efficacement les enzymes responsables de la transformation des signaux stimulant l’immunité en adénosine immunosuppressive. Bien que ces composés en soient à un stade précoce et n’aient qu’un effet direct modéré sur la destruction des cellules cancéreuses, ils constituent des outils prometteurs pour reconfigurer le microenvironnement tumoral afin que les cellules immunitaires de l’organisme puissent agir de manière plus efficace. Avec un affinage supplémentaire pour augmenter la puissance et la sélectivité, de tels inhibiteurs d’éctonucléotidases pourraient un jour compléter les immunothérapies existantes, aidant à dissiper le « brouillard » chimique qui protège les tumeurs des attaques.
Citation: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Mots-clés: immunothérapie du cancer, signalisation par l’adénosine, inhibiteurs d’enzyme, composés quinoline, microenvironnement tumoral