Clear Sky Science · es
Derivados del ácido quinolínico como potentes inhibidores de ectonucleotidasas
Por qué importa apaciguar la “señal de peligro” del cáncer
El cáncer no solo crece; también aprende a esconderse. Uno de sus trucos preferidos es convertir una señal natural de peligro liberada por células estresadas en un químico sedante que adormece al sistema inmunitario. Este artículo explora una nueva familia de pequeñas moléculas que pretenden interrumpir esa vía de escape, con el objetivo a largo plazo de ayudar a que las defensas del propio organismo reconozcan y ataquen mejor a los tumores.
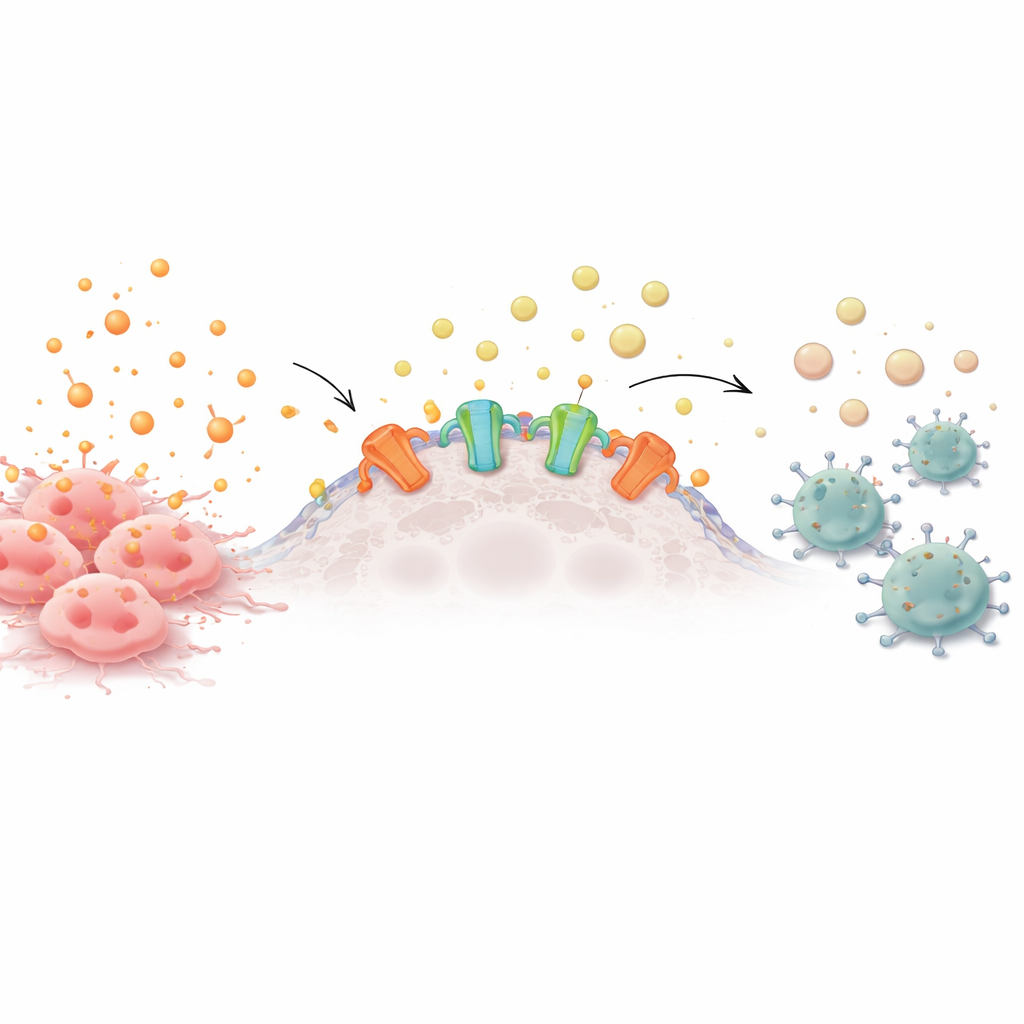
De las alarmas a la calma química
Las células sanas y cancerosas liberan constantemente moléculas transportadoras de energía al entorno. Cuando estas moléculas, como el ATP, se acumulan fuera de las células, actúan como alarmas que atraen a células inmunitarias para investigar problemas. En la superficie de muchas células tumorales, sin embargo, hay enzimas llamadas ectonucleotidasas que degradan el ATP hasta adenosina, una señal calmante que indica a las células inmunitarias que se retiren. Muchos cánceres agresivos sobreproducen estas enzimas, creando una nube protectora de adenosina que debilita a las células T, las células asesinas naturales y otros defensores cercanos.
Diseñando nuevos bloqueadores químicos
Los investigadores se propusieron diseñar y sintetizar un conjunto de doce compuestos relacionados basados en un “núcleo” de quinolina, una estructura plana en forma de anillo ya conocida por interactuar con dianas biológicas y por su potencial anticancerígeno. Al unir diferentes grupos químicos a este núcleo, crearon una pequeña biblioteca de derivados de quinolina-6-carboxamida. Estas moléculas se caracterizaron cuidadosamente con técnicas químicas estándar para confirmar su estructura y pureza, y luego se probaron frente a varias ectonucleotidasas clave, incluyendo cuatro miembros que procesan ATP y sustancias relacionadas, así como dos enzimas que completan el paso final de producción de adenosina.
Encontrando los bloqueadores enzimáticos más eficaces
Al mezclar las nuevas moléculas con enzimas humanas purificadas en el laboratorio, varios compuestos destacaron como potentes inhibidores. Un compuesto, etiquetado como 4d, inhibió con gran potencia dos enzimas que procesan ATP (h-NTPDasa1 y h-NTPDasa2) a concentraciones muy bajas, lo que lo señala como un inhibidor prometedor de acción amplia. Otros derivados mostraron comportamientos más selectivos: el compuesto 4a bloqueó con fuerza la ecto-5′-nucleotidasa, que realiza el último corte que produce adenosina; el compuesto 4k fue el mejor bloqueador de otra enzima, ENPP1; y los compuestos 4b y 4g fueron particularmente efectivos contra distintos subtipos de NTPDasa. Al comparar qué sustituciones químicas mejoraban o debilitaban la actividad, el equipo trazó cómo pequeños cambios en la estructura pueden ajustar de forma drástica la potencia y la selectividad del bloqueo enzimático.
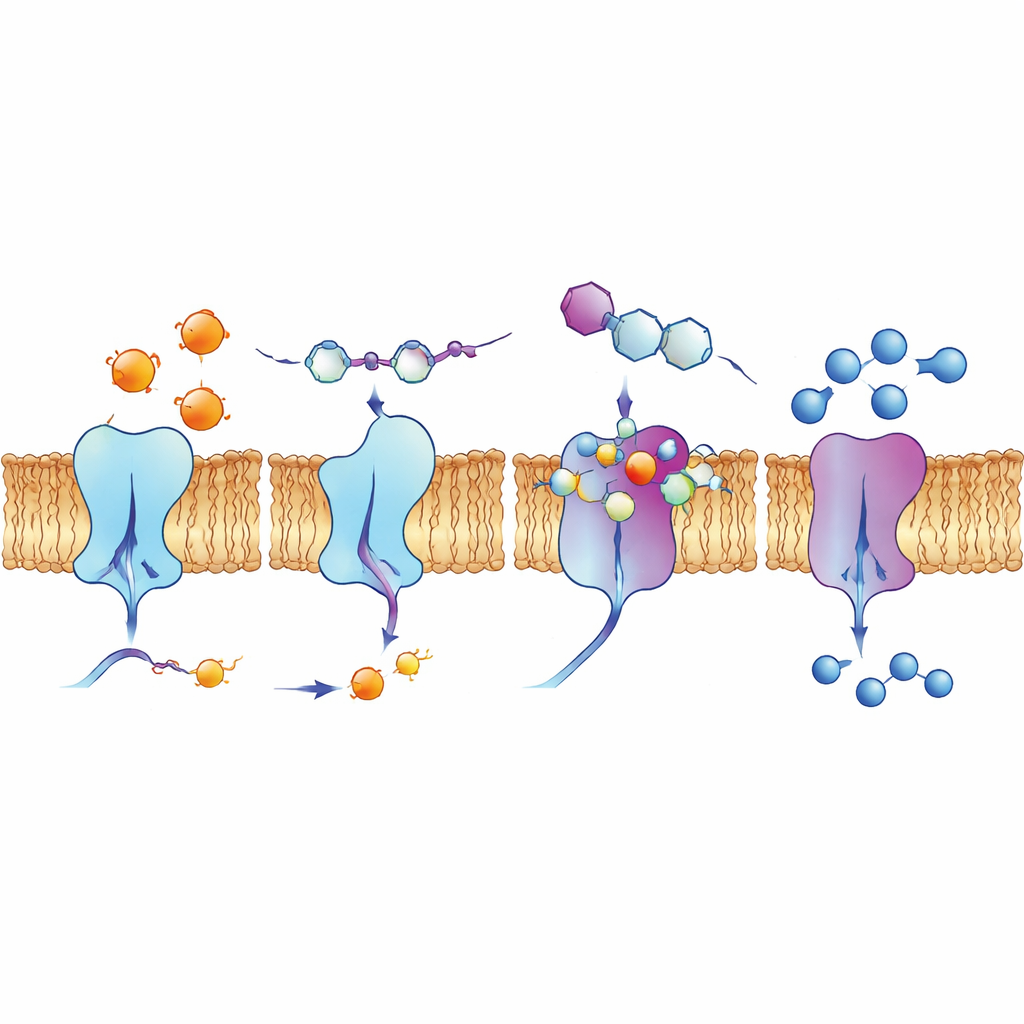
Examinando los sitios de unión y células vivas
Para entender por qué ciertos compuestos funcionaban tan bien, los autores emplearon simulaciones de acoplamiento (docking) por ordenador y cálculos de química cuántica. Estos modelos mostraron cómo las moléculas basadas en quinolina se acomodan en ranuras de las superficies enzimáticas, formando redes de fuerzas atractivas, incluidas interacciones por puente de hidrógeno, apilamientos entre anillos planos e interacciones que involucran halógenos como flúor, cloro o yodo. Los cálculos de distribución electrónica apoyaron la idea de que los compuestos más activos tienen el equilibrio adecuado entre estabilidad y reactividad para interactuar con sitios cargados en las enzimas. El equipo también examinó cómo se comporta un compuesto líder, 4d, en células humanas de cáncer de pulmón utilizando métodos de fluorescencia. Este compuesto emite fluorescencia bajo luz específica, y las imágenes revelaron que se concentra a lo largo de la membrana celular, la misma localización de las ectonucleotidasas, lo que sugiere que puede alcanzar sus dianas previstas en un entorno biológico realista.
Primeros pasos hacia la acción anticancerígena
Puesto que un fármaco útil no solo debe golpear la diana sino también afectar el crecimiento tumoral, los investigadores evaluaron cómo las nuevas moléculas influyen en células de cáncer de mama cultivadas en laboratorio. Varios derivados, especialmente 4j y 4k, redujeron la supervivencia celular y ralentizaron la división celular con el tiempo, aunque no tan intensamente como un fármaco quimioterápico estándar. Comprobaciones computacionales de absorción, distribución y características básicas de “drug-likeness” sugirieron que la mayoría de los compuestos tienen propiedades compatibles con uso oral y pueden, potencialmente, alcanzar el cerebro, lo que abre la posibilidad de futuras aplicaciones en tumores de difícil tratamiento.
Qué significa esto para terapias cancerígenas futuras
En conjunto, el estudio presenta una nueva familia de moléculas basadas en quinolina que bloquean de forma eficaz enzimas responsables de convertir señales que estimulan la inmunidad en adenosina que la apaga. Aunque estos compuestos están en una etapa temprana y muestran solo efectos moderados de citotoxicidad directa, son herramientas prometedoras para remodelar el microambiente tumoral y permitir que las células inmunitarias del propio organismo actúen con mayor eficacia. Con refinamientos adicionales para aumentar potencia y selectividad, tales inhibidores de ectonucleotidasas podrían algún día complementar las inmunoterapias existentes, ayudando a disipar la “niebla” química que protege a los tumores del ataque.
Cita: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Palabras clave: inmunoterapia contra el cáncer, señalización por adenosina, inhibidores enzimáticos, compuestos de quinolina, microambiente tumoral