Clear Sky Science · de
Derivate der Chinolincarbonsäure als potente Ectonukleotidase-Inhibitoren
Warum das Beruhigen des „Alarmsignals“ von Krebs wichtig ist
Krebs wächst nicht nur; er lernt auch, sich zu verbergen. Einer seiner Lieblingstricks besteht darin, ein natürliches Alarmsignal, das von gestressten Zellen freigesetzt wird, in eine beruhigende Chemikalie umzuwandeln, die das Immunsystem in den Schlaf wiegt. Dieser Artikel untersucht eine neue Familie kleiner Moleküle, die diese Fluchtroute unterbrechen sollen, mit dem langfristigen Ziel, die körpereigenen Abwehrkräfte dabei zu unterstützen, Tumore besser zu erkennen und anzugreifen.
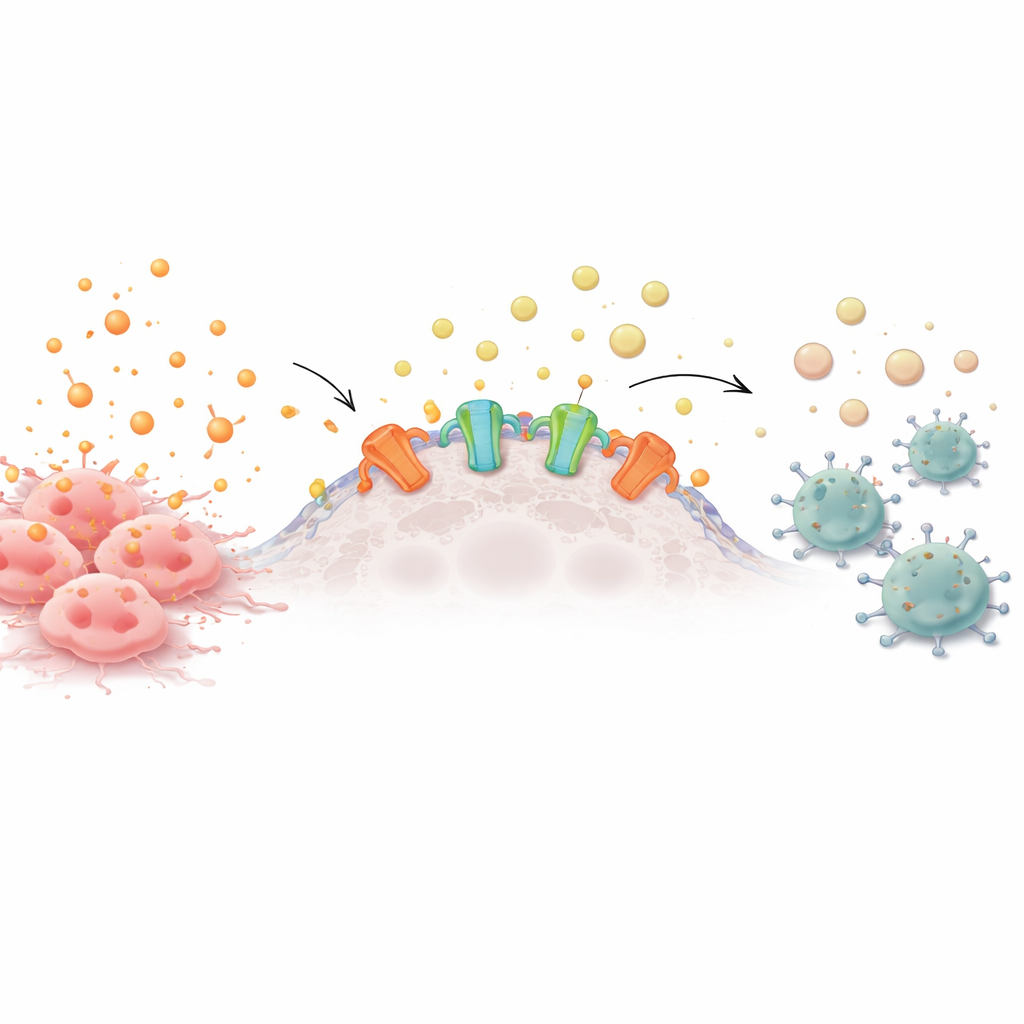
Von Alarmglocken zu chemischer Stille
Gesunde und krebserkrankte Zellen setzen ständig energiereiche Moleküle in ihre Umgebung frei. Wenn sich solche Moleküle, etwa ATP, außerhalb der Zellen ansammeln, wirken sie wie Alarmglocken und locken Immunzellen herbei, um nach der Ursache zu sehen. Auf der Oberfläche vieler Tumorzellen sitzen jedoch Enzyme, sogenannte Ectonukleotidasen, die ATP schrittweise zu Adenosin abbauen — ein beruhigendes Signal, das Immunzellen anweist, sich zurückzuhalten. Viele aggressive Krebsarten produzieren diese Enzyme im Überschuss und schaffen so eine schützende Adenosinwolke, die in der Nähe befindliche T‑Zellen, natürliche Killerzellen und andere Abwehrzellen abschwächt.
Entwurf neuer chemischer Blocker
Die Forschenden machten sich daran, eine Reihe von zwölf verwandten Verbindungen zu entwerfen und zu synthetisieren, die auf einem Chinolin‑„Kern“ basieren — einer flachen, ringförmigen Struktur, die bereits dafür bekannt ist, mit biologischen Zielstrukturen zu interagieren und anticancerales Potenzial zu besitzen. Durch das Anbringen verschiedener chemischer Gruppen an diesem Kern entstand eine kleine Bibliothek von Chinolin‑6‑carboxamid‑Derivaten. Diese Moleküle wurden mit üblichen chemischen Methoden sorgfältig charakterisiert, um Struktur und Reinheit zu bestätigen, und anschließend gegen mehrere wichtige Ectonukleotidasen getestet, darunter vier Mitglieder, die ATP und verwandte Substrate verarbeiten, sowie zwei Enzyme, die den letzten Schritt zur Bildung von Adenosin vollziehen.
Die wirkungsvollsten Enzymblocker finden
Als die neuen Moleküle im Labor mit gereinigten menschlichen Enzymen vermischt wurden, zeichneten sich mehrere als starke Hemmstoffe ab. Eine Verbindung, bezeichnet als 4d, schaltete bei sehr niedrigen Konzentrationen zwei ATP‑verarbeitende Enzyme (h‑NTPDase1 und h‑NTPDase2) wirkungsvoll aus und gilt damit als vielversprechender breit wirkender Inhibitor. Andere Derivate zeigten selektiveres Verhalten: Verbindung 4a hemmte stark die Ecto‑5′‑Nukleotidase, die den letzten Schnitt zur Adenosinbildung vornimmt; 4k war am besten darin, das Enzym ENPP1 zu blockieren; und die Verbindungen 4b und 4g erwiesen sich als besonders effektiv gegen verschiedene NTPDase‑Subtypen. Durch den Vergleich, welche chemischen Modifikationen die Aktivität verbesserten oder abschwächten, kartierte das Team, wie kleine Strukturänderungen die Hemmwirkung und Selektivität der Enzyme drastisch beeinflussen können.
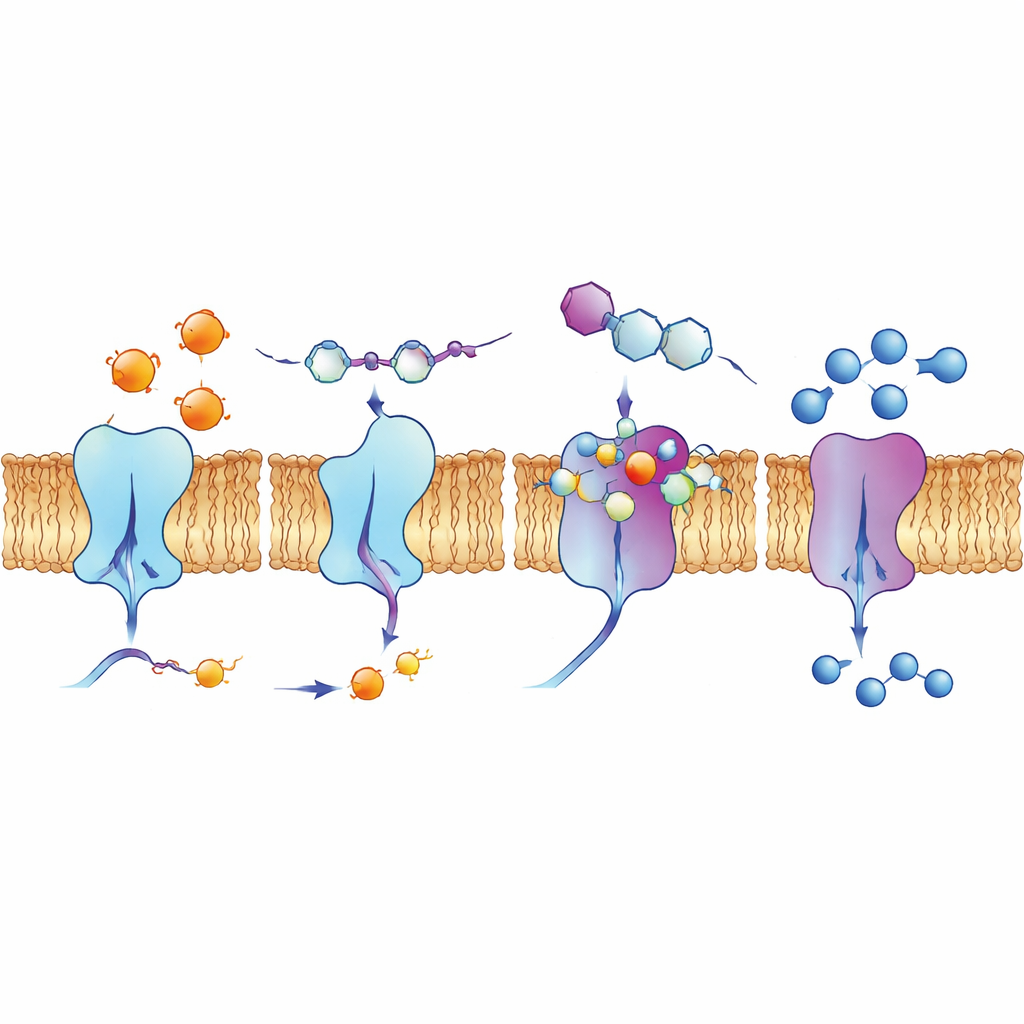
Ein Blick in Bindungstaschen und lebende Zellen
Um zu verstehen, warum bestimmte Verbindungen so gut wirkten, nutzten die Autorinnen und Autoren computerbasierte Docking‑Simulationen und Quantenchemie‑Berechnungen. Diese Modelle zeigten, wie sich die chinolinbasierten Moleküle in Nischen auf den Enzymoberflächen einlagern und Netzwerke attraktiver Kräfte ausbilden, darunter Wasserstoffbrücken, Stapelwechselwirkungen zwischen flachen Ringen und Wechselwirkungen mit Halogenen wie Fluor, Chlor oder Jod. Berechnungen zur Elektronenverteilung stützten die Idee, dass die aktivsten Verbindungen das richtige Gleichgewicht aus Stabilität und Reaktivität besitzen, um auf geladene Stellen in den Enzymen einzuwirken. Das Team untersuchte außerdem, wie sich eine Leitverbindung, 4d, in humanen Lungenkrebszellen verhält, mithilfe von Fluoreszenzmethoden. Sie fluoresziert unter bestimmten Lichtbedingungen und die Bildgebung zeigte, dass sie sich entlang der Zellmembran anreichert — genau dort, wo Ectonukleotidase‑Enzyme lokalisiert sind — was darauf hindeutet, dass sie ihre vorgesehenen Ziele in einem realistischen biologischen Umfeld erreichen kann.
Frühe Schritte in Richtung antitumoraler Wirkung
Da ein nützliches Medikament nicht nur sein Ziel treffen, sondern auch das Wachstum von Krebszellen beeinflussen muss, prüften die Forschenden, wie die neuen Moleküle Brustkrebszellen in Kultur beeinflussen. Mehrere Derivate, insbesondere 4j und 4k, verringerten das Überleben der Zellen und verlangsamten die Zellteilung im Laufe der Zeit, wenn auch nicht so stark wie ein Standard‑Chemotherapeutikum. Computergestützte Bewertungen von Absorption, Verteilung und grundlegender Arzneimittelähnlichkeit deuteten darauf hin, dass die meisten Verbindungen Eigenschaften aufweisen, die mit oraler Anwendung vereinbar sind und potenziell das Gehirn erreichen können, was Möglichkeiten für künftige Anwendungen bei schwer behandelbaren Tumoren eröffnet.
Was das für künftige Krebsbehandlungen bedeutet
Insgesamt stellt die Studie eine neue Familie chinolinbasierter Moleküle vor, die Enzyme effizient blockieren, welche immunstimulierende Signale in immundämpfendes Adenosin umwandeln. Obwohl diese Verbindungen sich noch in einem frühen Stadium befinden und nur mäßige direkte krebsabtötende Effekte zeigen, sind sie vielversprechende Werkzeuge, um die Tumorumgebung so umzubauen, dass die körpereigenen Immunzellen effektiver arbeiten können. Mit weiterer Optimierung zur Steigerung von Potenz und Selektivität könnten solche Ectonukleotidase‑Inhibitoren eines Tages bestehende Immuntherapien ergänzen und helfen, den chemischen „Nebel“ zu lüften, der Tumore vor Angriffen schützt.
Zitation: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Schlüsselwörter: Krebsimmuntherapie, Adenosin-Signalgebung, Enzymhemmer, Chinolin-Verbindungen, Tumormikroumgebung