Clear Sky Science · tr
Güçlü ektonükleotidaz inhibitörleri olarak kinolin karboksilik asit türevleri
Kanserin “tehlike sinyali”ni yatıştırmasının önemi
Kanser sadece büyümez; aynı zamanda saklanmayı da öğrenir. En sevdiği numaralardan biri, stres altındaki hücrelerin saldığı doğal bir tehlike sinyalini bağışlayıcı bir kimyasala dönüştürüp bağışıklık sistemini uyutmaktır. Bu makale, o kaçış yolunu bozmayı amaçlayan yeni bir küçük molekül ailesini inceliyor; nihai hedef, vücudun kendi savunmasının tümörleri daha iyi tanıyıp saldırmasına yardımcı olmak.
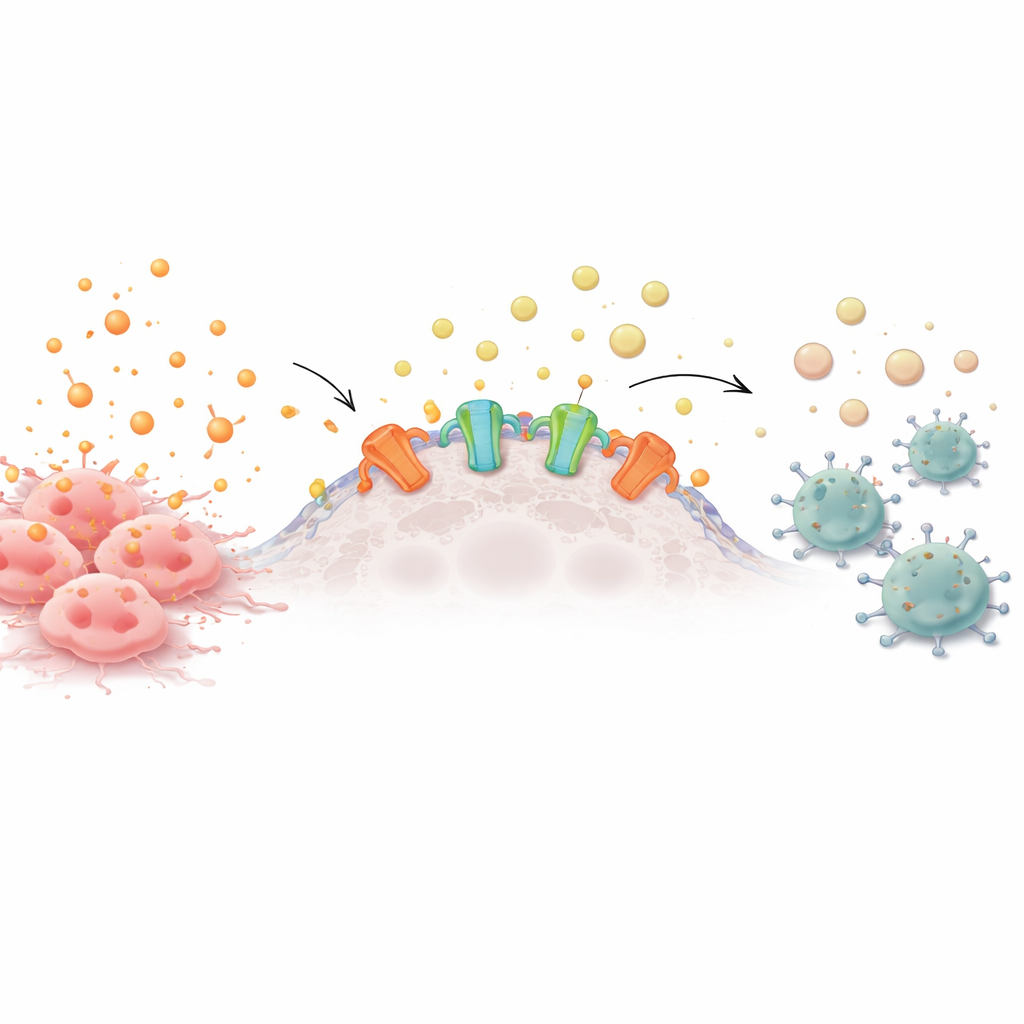
Alarm zillerinden kimyasal sessizliğe
Sağlıklı ve kanserli hücreler çevrelerine sürekli enerji taşıyan moleküller salar. Bu moleküller, örneğin ATP, hücre dışına biriktiğinde alarm zilleri gibi çalışır ve bağışıklık hücrelerini olası bir sorunu incelemeye çeker. Ancak birçok tümör hücresi yüzeyinde, ATP’yi sürekli olarak adenozi̇ne parçalayan ektonükleotidaz adı verilen enzimler bulunur; adenozi̇n, bağışıklık hücrelerine geri çekilmelerini söyleyen yatıştırıcı bir sinyaldir. Birçok agresif kanser bu enzimleri aşırı üretir ve çevresindeki T hücreleri, doğal öldürücü hücreler ve diğer savunucuları zayıflatan koruyucu bir adenozi̇n bulutu oluşturur.
Yeni kimyasal engelleyiciler tasarlamak
Araştırmacılar, biyolojik hedeflerle etkileştiği ve antikanser potansiyeli olduğu bilinen düz, halka şeklinde bir yapı olan kinolin “çekirdeği” üzerine kurulmuş on iki ilişkili bileşik tasarlayıp sentezlemeye koyuldular. Bu çekirdeğe farklı kimyasal gruplar ekleyerek kinolin-6-karboksamid türevlerinden küçük bir kütüphane oluşturdular. Bu moleküller, yapı ve saflıklarını doğrulamak için standart kimya araçlarıyla dikkatle karakterize edildi ve ardından ATP ve ilişkili maddeleri işleyen dört üye de dahil olmak üzere birkaç ana ektonükleotidaz ile ve adenozi̇n üretiminin son adımını tamamlayan iki enzim karşısında test edildi.
En etkili enzim durdurucuları bulmak
Yeni moleküller saflaştırılmış insan enzimleriyle laboratuvarda karıştırıldığında, birkaç tanesi güçlü engelleyiciler olarak öne çıktı. 4d etiketli bir bileşik, çok düşük konsantrasyonlarda iki ATP-işleyen enzimi (h-NTPDase1 ve h-NTPDase2) etkili bir şekilde devre dışı bırakarak umut verici bir geniş etkili inhibitör olarak öne çıktı. Diğer türevler daha seçici davranış sergiledi: 4a bileşiği adenozi̇n üreten son kesimi gerçekleştiren ekto-5′-nükleotidazı güçlü biçimde engelledi; 4k bileşiği başka bir enzim olan ENPP1’i en iyi engelleyen oldu; 4b ve 4g ise farklı NTPDase alt tiplerine karşı özellikle etkiliydi. Hangi kimyasal süslemelerin aktiviteyi artırıp azaltacağını karşılaştırarak ekip, yapıda yapılan küçük değişikliklerin enzim engelleme gücünü ve seçiciliğini nasıl dramatik şekilde ayarlayabildiğini haritaladı.
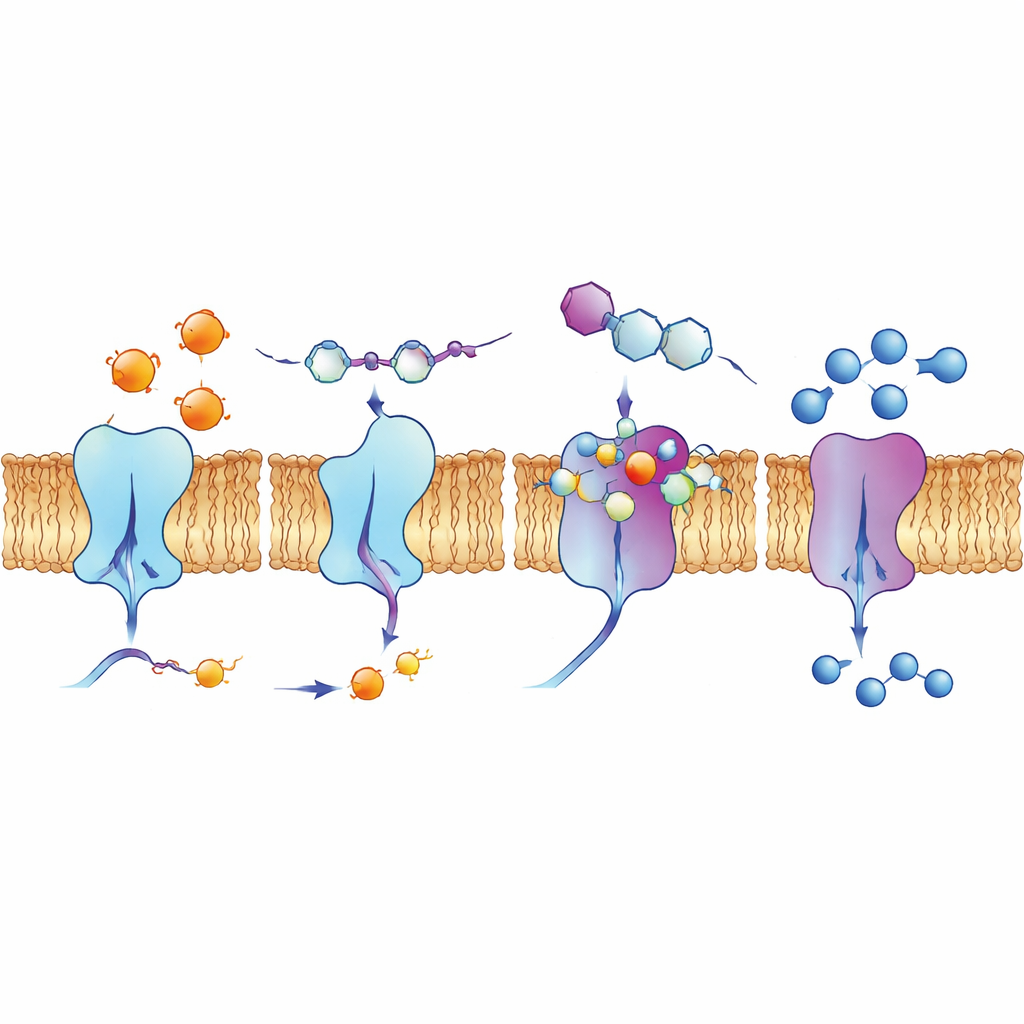
Bağlanma cepleri ve canlı hücrelere bakış
Bazı bileşiklerin neden bu kadar iyi çalıştığını anlamak için yazarlar bilgisayar tabanlı yerleştirme (docking) simülasyonları ve kuantum kimya hesaplamaları kullandılar. Bu modeller, kinolin bazlı moleküllerin enzim yüzeylerindeki oyuklara nasıl yerleştiğini, hidrojen bağları, düz halkalar arasındaki yığılma etkileşimleri ve flor, klor veya iyot gibi halojenleri içeren etkileşimler dahil olmak üzere cazip kuvvet ağları oluşturduğunu gösterdi. Elektron dağılımı hesaplamaları, en aktif bileşiklerin enzimlerdeki yüklü bölgelerle etkileşmeye uygun dengeye sahip olacak şekilde kararlılık ve reaktivite bakımından uygun oldukları fikrini destekledi. Ekip ayrıca lider bileşiklerden biri olan 4d’nin insan akciğer kanseri hücrelerindeki davranışını floresan yöntemlerle inceledi. Belirli ışık altında doğal olarak parlıyor ve görüntüleme, onun ektonükleotidaz enzimlerinin bulunduğu hücre zarında yoğunlaştığını ortaya koydu; bu da hedeflerine gerçekçi bir biyolojik ortamda ulaşabildiğini düşündürüyor.
Antikanser etkinliğe doğru erken adımlar
Yararlı bir ilacın yalnızca hedefine bağlanmaması, aynı zamanda kanser hücresi büyümesini etkilemesi gerektiği için araştırmacılar yeni moleküllerin kültürde yetiştirilen meme kanseri hücreleri üzerindeki etkilerini değerlendirdiler. Özellikle 4j ve 4k olmak üzere birkaç türev hücre hayatta kalmasını azalttı ve zamanla hücre bölünmesini yavaşlattı, ancak standart bir kemoterapi ilacı kadar güçlü değildi. Emilim, dağılım ve temel ilaç-uygunluğu açısından yapılan hesaplamalı kontroller, bileşiklerin çoğunun oral kullanım ile uyumlu özelliklere sahip olduğunu ve potansiyel olarak beyne ulaşabileceğini gösterdi; bu da tedavisi zor tümörlerde gelecekteki uygulamalar olasılığını gündeme getiriyor.
Gelecekteki kanser tedavileri için anlamı
Genel olarak, çalışma bağışıklık uyaran sinyalleri bağışıklığı baskılayan adenozi̇ne dönüştüren enzimleri etkili şekilde engelleyen kinolin bazlı yeni bir molekül ailesini tanıtıyor. Bu bileşikler erken aşamada olup doğrudan kanser öldürücü etkileri ılımlı olsa da, tümör ortamını yeniden şekillendirerek vücudun kendi bağışıklık hücrelerinin daha etkili çalışmasına olanak veren umut verici araçlardır. Güç ve seçiciliği artırmak için daha fazla iyileştirme ile bu tür ektonükleotidaz inhibitörleri bir gün mevcut immünoterapilere tamamlayıcı olabilir ve tümörleri koruyan kimyasal “sis”i kaldırmaya yardımcı olabilir.
Atıf: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Anahtar kelimeler: kanser immünoterapisi, adenozin sinyali, enzim inhibitörleri, kinolin bileşikleri, tümör mikroçevresi