Clear Sky Science · ar
مشتقات حمض الكينولين الكربوكسيلي كمثبطات قوية للِإكتونوكليوتيدازات
لماذا يهم تهدئة «إشارة الخطر» في السرطان
السرطان لا يكتفي بالنمو فحسب؛ بل يتعلّم أيضاً كيف يختبئ. إحدى حيلته المفضلة هي تحويل إشارة خطر طبيعية تُفرَز من الخلايا المضغوطة إلى مركب مهدئ يُنعِم جهاز المناعة ويجعله أقل يقظة. تستكشف هذه الورقة عائلة جديدة من الجزيئات الصغيرة تهدف إلى تعطيل هذا طريق الهروب، مع الهدف الطويل الأمد لمساعدة دفاعات الجسم على التعرف على الأورام ومهاجمتها بشكل أفضل.
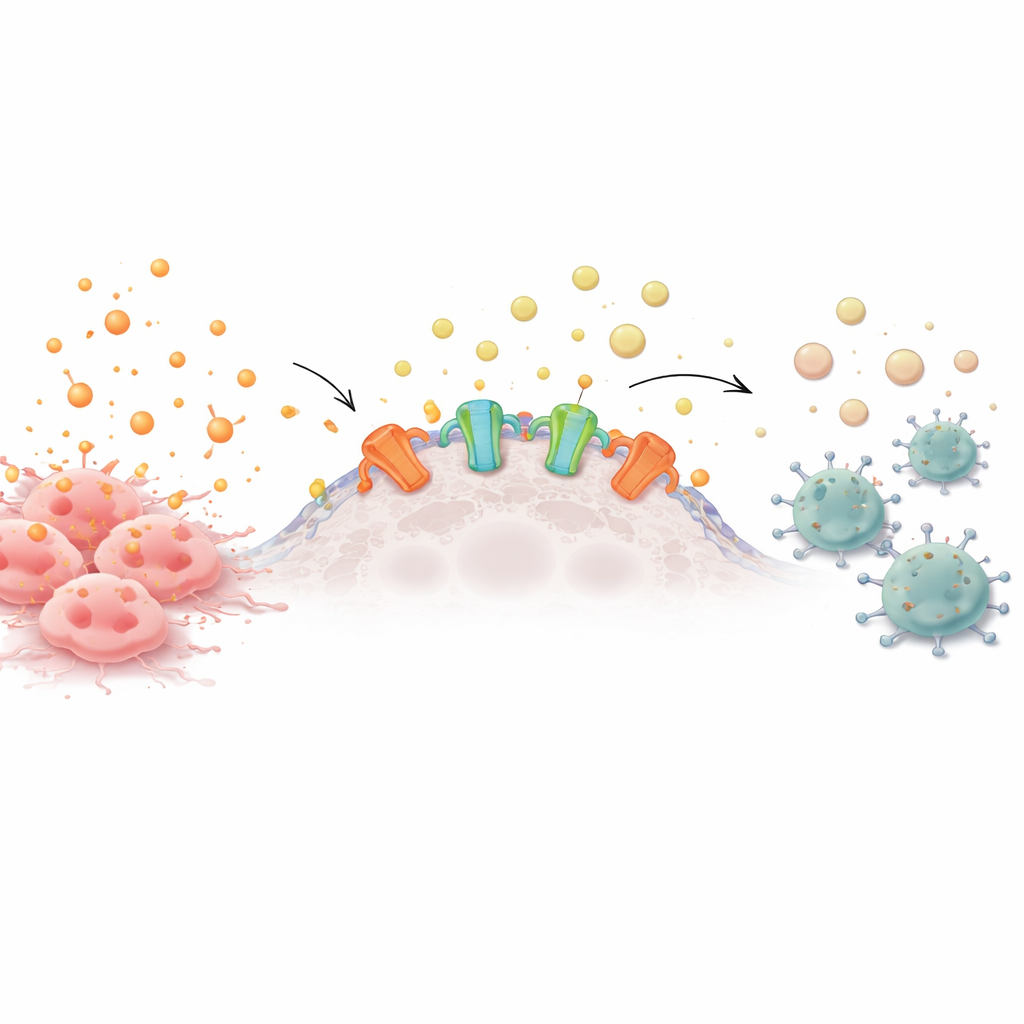
من أجراس الإنذار إلى الصمت الكيميائي
الخلايا السليمة والخلايا السرطانية تفرز باستمرار جزيئات حاملة للطاقة إلى محيطها. عندما تتراكم هذه الجزيئات، مثل أدينوسين ثلاثي الفوسفات (ATP)، خارج الخلايا، تعمل كأجراس إنذار تستدعي خلايا الجهاز المناعي للتحقق من وجود مشكلة. على سطح العديد من الخلايا الورمية، مع ذلك، توجد إنزيمات تُدعى إكتونوكليوتيدازات تقوم بتقطيع ATP تدريجياً إلى أدينوسين، إشارة مهدئة تأمر خلايا المناعة بالتراجع. العديد من أنواع السرطان العدوانية تُفرط في إنتاج هذه الإنزيمات، مكونة سحابة واقية من الأدينوسين تضعف الخلايا التائية والخلايا القاتلة الطبيعية ودفاعات أخرى قريبة.
تصميم حاصرات كيميائية جديدة
سعى الباحثون إلى تصميم وتخليق مجموعة مكونة من اثني عشر مركباً مرتبطاً مبنية حول «لب» الكينولين، بنية حلقيّة مسطحة معروفة بتفاعلها مع أهداف بيولوجية وبإمكانها امتلاك نشاط مضاد للسرطان. عبر إرفاق مجموعات كيميائية مختلفة بهذا اللب، أنشأوا مكتبة صغيرة من مشتقات كينولين-6-كاربوكساميد. خُصّصت هذه الجزيئات وتمييزها بعناية باستخدام أدوات التحليل الكيميائي القياسية للتأكد من بنيتها ونقائها، ثم اختُبرت ضد عدة إكتونوكليوتيدازات أساسية، بما في ذلك أربعة أعضاء تعالج ATP والمواد المرتبطة به، وكذلك إنزيمان يكملان الخطوة النهائية لتكوين الأدينوسين.
العثور على أقوى مثبطات الإنزيم
عند خلط الجزيئات الجديدة مع إنزيمات بشرية مُنقّاة في المختبر، تميّز عدد منها كمثبطات قوية. مركب واحد، المسمى 4d، أوقف بقوة اثنين من إنزيمات معالجة ATP (h-NTPDase1 و h-NTPDase2) عند تراكيز منخفضة جداً، مما يجعله مثبطاً واعداً واسع المدى. أظهرت مشتقات أخرى سلوكاً أكثر انتقائية: المركب 4a حجب بشكل قوي إكتو-5′-نوكليوتيداز، الذي يؤدي القطع النهائي لإنتاج الأدينوسين؛ كان المركب 4k الأفضل في حجب إنزيم آخر، ENPP1؛ وكانت المركبات 4b و4g فعّالة بشكل خاص ضد سواغات فرعية مختلفة من NTPDase. من خلال مقارنة أي التعديلات الكيميائية حسّنت أو أضعفت النشاط، رسم الفريق خريطة توضح كيف يمكن للتغييرات الطفيفة في البنية أن تضبط بشكل كبير قوة وانتقائية حجب الإنزيم.
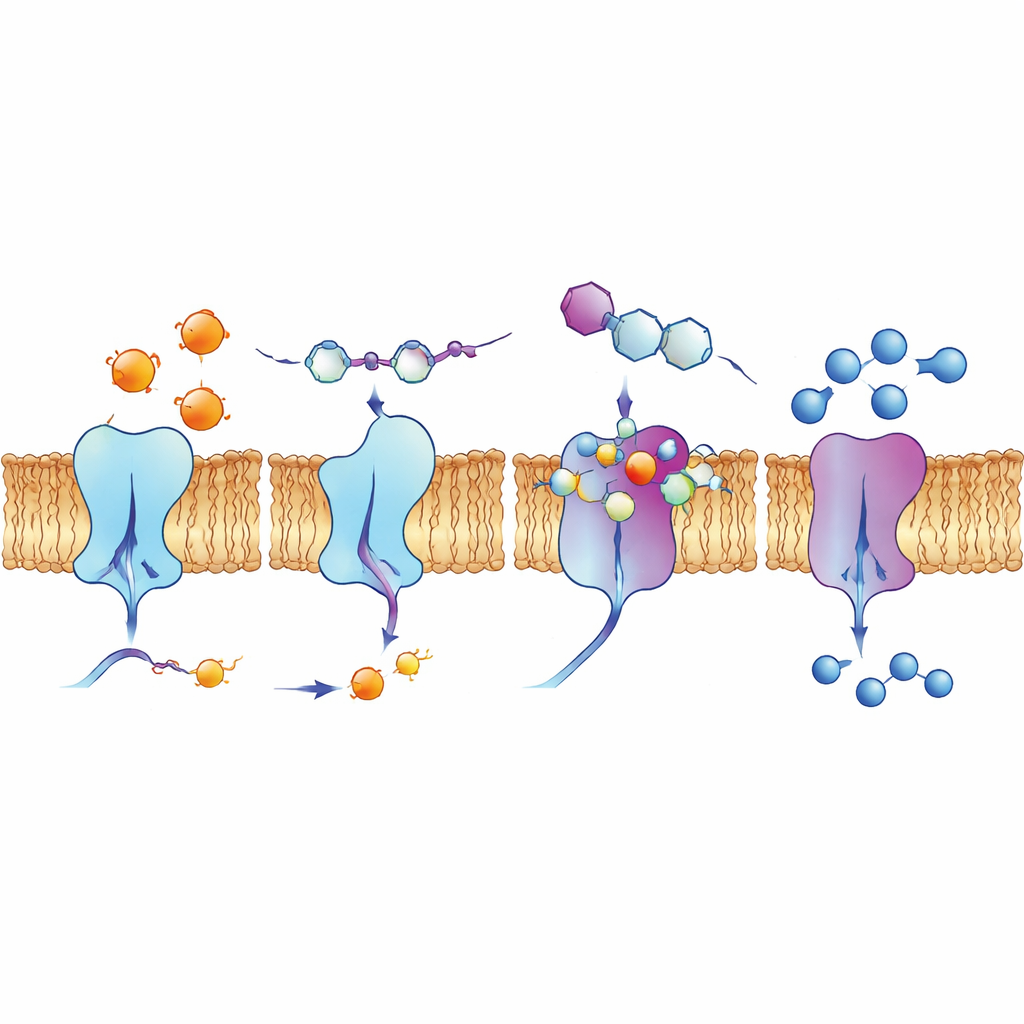
نظرة إلى جيوب الارتباط والخلايا الحية
لفهم سبب فعالية بعض المركبات، استخدم المؤلفون محاكاة ربط حاسوبية وحسابات كيمياء كمية. أظهرت هذه النماذج كيف تتداخل جزيئات الكينولين داخل أخاديد على أسطح الإنزيمات، مكونة شبكات من قوى جذب، بما في ذلك روابط الهيدروجين، وتراكم الحلقات المسطحة، وتفاعلات تتضمن هالوجينات مثل الفلور والكلور أو اليود. دعمت حسابات توزيع الإلكترون الفكرة القائلة بأن المركبات الأكثر نشاطاً تمتلك التوازن الصحيح بين الاستقرار والنشاط الكيميائي للتفاعل مع مواقع مشحونة في الإنزيمات. كما فحص الفريق سلوك مركب رائد واحد، 4d، في خلايا سرطان الرئة البشرية باستخدام طرق التألق. هذا المركب يتألق طبيعياً تحت ضوء معين، وكشفت الصور أنه يتركز على غشاء الخلية، وهو الموقع الفعلي للإكتونوكليوتيدازات، مما يشير إلى أنه قادر على الوصول إلى أهدافه في بيئة بيولوجية واقعية.
خطوات مبكرة نحو الفعل المضاد للسرطان
بما أن الدواء المفيد يجب ألا يستهدف الهدف فقط بل يؤثر أيضاً في نمو الخلايا السرطانية، قيّم الباحثون كيف تؤثر الجزيئات الجديدة على خلايا سرطان الثدي المزروعة في المختبر. قللت عدة مشتقات، خاصة 4j و4k، من بقاء الخلايا وأبطأت انقسامها مع مرور الوقت، وإن لم تكن بقوة أدوية العلاج الكيميائي القياسية. أشارت الفحوصات الحاسوبية لامتصاص وتوزيع ومواصفات الشبه دوائية الأساسية إلى أن معظم هذه المركبات لديها خصائص متوافقة مع الاستخدام الفموي وقد يكون باستطاعتها الوصول إلى الدماغ، مما يفتح إمكانية تطبيقات مستقبلية في الأورام صعبة العلاج.
ماذا يعني هذا لعلاجات السرطان المستقبلية
بشكل عام، تقدّم الدراسة عائلة جديدة من الجزيئات القائمة على الكينولين التي تحجب بكفاءة الإنزيمات المسؤولة عن تحويل الإشارات المحفزة للمناعة إلى أدينوسين مثبط للمناعة. وبينما هذه المركبات في مرحلة مبكرة وتظهر تأثيرات مباشرة معتدلة على قتل السرطان، فهي أدوات واعدة لإعادة تشكيل بيئة الورم بحيث تعمل خلايا الجهاز المناعي للجسم بفعالية أكبر. مع مزيد من التكرير لرفع الفعالية والانتقائية، قد تكمل مثل هذه المثبطات للإكتونوكليوتيدازات يوماً ما العلاجات المناعية القائمة، مساعدةً على رفع «ضباب» كيميائي يحمي الأورام من الهجوم.
الاستشهاد: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
الكلمات المفتاحية: العلاج المناعي للسرطان, إشارة الأدينوسين, مثبطات الإنزيم, مركبات الكينولين, البيئة الميكروية للورم