Clear Sky Science · pl
pochodne chinolinokarboksylowych jako silne inhibitory ektonukleotydaz
Dlaczego ugaszenie „sygnału niebezpieczeństwa” raka ma znaczenie
Nowotwór nie tylko rośnie; uczy się też ukrywać. Jednym z jego ulubionych trików jest przekształcanie naturalnego sygnału niebezpieczeństwa uwalnianego przez zestresowane komórki w ukojenie chemiczne, które usypia układ odpornościowy. Artykuł opisuje nową rodzinę małych cząsteczek mających na celu przerwanie tej drogi ucieczki, z długofalowym celem pomocy własnym mechanizmom obronnym organizmu w lepszym rozpoznawaniu i atakowaniu guzów.
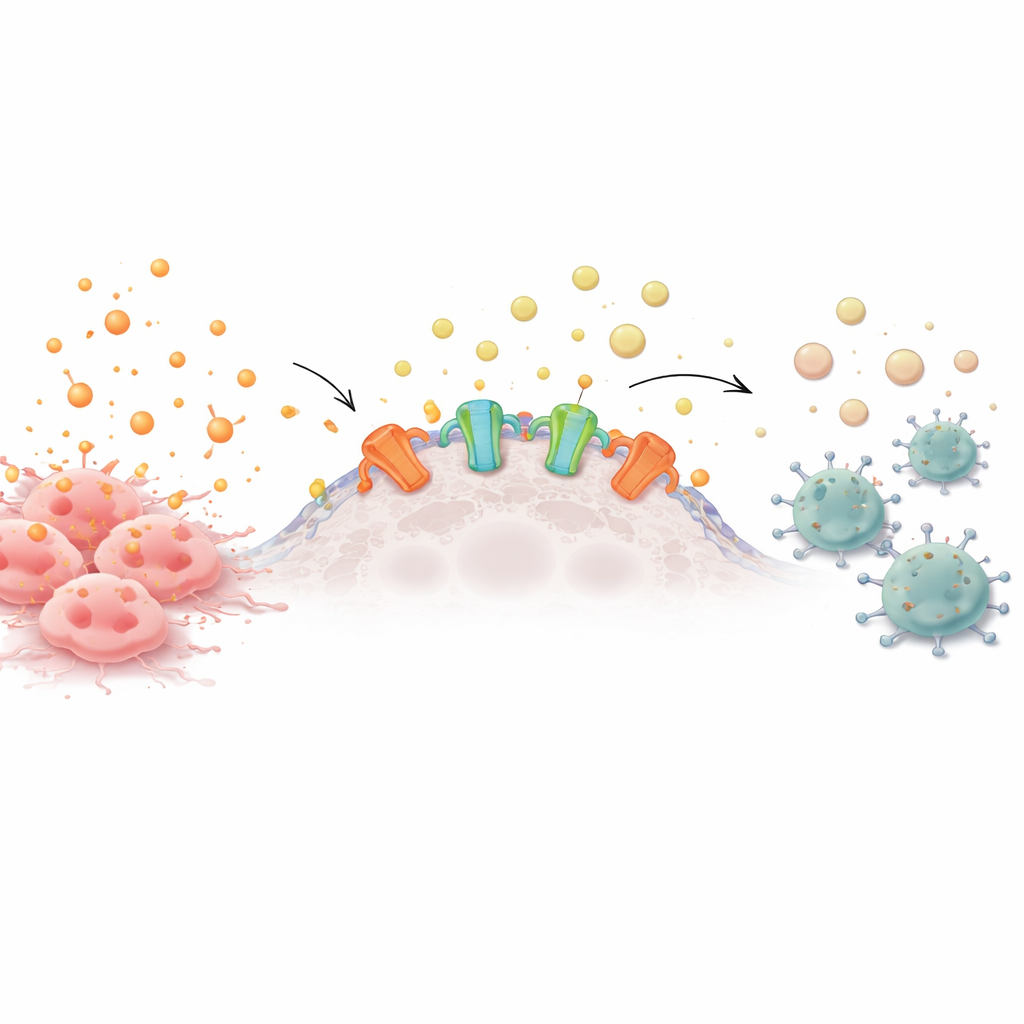
Z alarmów do chemicznej ciszy
Zdrowe i nowotworowe komórki stale uwalniają do otoczenia cząsteczki przenoszące energię. Gdy takie substancje, jak ATP, gromadzą się poza komórkami, pełnią rolę alarmów, przyciągając komórki odpornościowe do zbadania zagrożenia. Na powierzchni wielu komórek nowotworowych znajdują się jednak enzymy zwane ektonukleotydazami, które stopniowo rozkładają ATP do adenozyny — sygnału kojącego, który nakazuje komórkom odpornościowym wycofać się. Wiele agresywnych nowotworów nadprodukuje te enzymy, tworząc ochronną chmurę adenozyny osłabiającą pobliskie limfocyty T, komórki NK i inne defensywne komórki.
Projektowanie nowych blokujących związków
Badacze postanowili zaprojektować i zsyntetyzować zestaw dwunastu spokrewnionych związków opartych na rdzeniu chinolinowym — płaskiej, pierścieniowej strukturze znanej z interakcji z celami biologicznymi i mającej potencjał przeciwnowotworowy. Poprzez przyłączanie różnych grup chemicznych do tego rdzenia stworzyli małą bibliotekę pochodnych chinolino-6-karboksyamidu. Związki te zostały starannie scharakteryzowane przy użyciu standardowych narzędzi chemicznych w celu potwierdzenia struktur i czystości, a następnie przetestowane przeciw kilku kluczowym ektonukleotydazom, w tym czterem enzymom przetwarzającym ATP i pokrewne substraty oraz dwóm enzymom dokonującym ostatniego kroku w tworzeniu adenozyny.
Wyszukiwanie najskuteczniejszych hamulców enzymatycznych
Gdy nowe cząsteczki wymieszano z oczyszczonymi ludzkimi enzymami in vitro, kilka z nich wyróżniło się jako silne inhibitory. Jeden związek, oznaczony jako 4d, efektywnie zablokował dwie enzymy przetwarzające ATP (h-NTPDase1 i h-NTPDase2) przy bardzo niskich stężeniach, co czyni go obiecującym inhibitorem o szerokim spektrum działania. Inne pochodne wykazywały bardziej selektywne działanie: związek 4a silnie hamował ecto-5′-nukleotydazę, która wykonuje ostatnie cięcie prowadzące do powstania adenozyny; związek 4k był najlepszy w blokowaniu enzymu ENPP1; natomiast związki 4b i 4g były szczególnie skuteczne wobec różnych podtypów NTPDaz. Porównując, które modyfikacje chemiczne wzmacniały lub osłabiały aktywność, zespół odwzorował, jak drobne zmiany strukturalne mogą istotnie regulować siłę i wybiórczość blokowania enzymów.
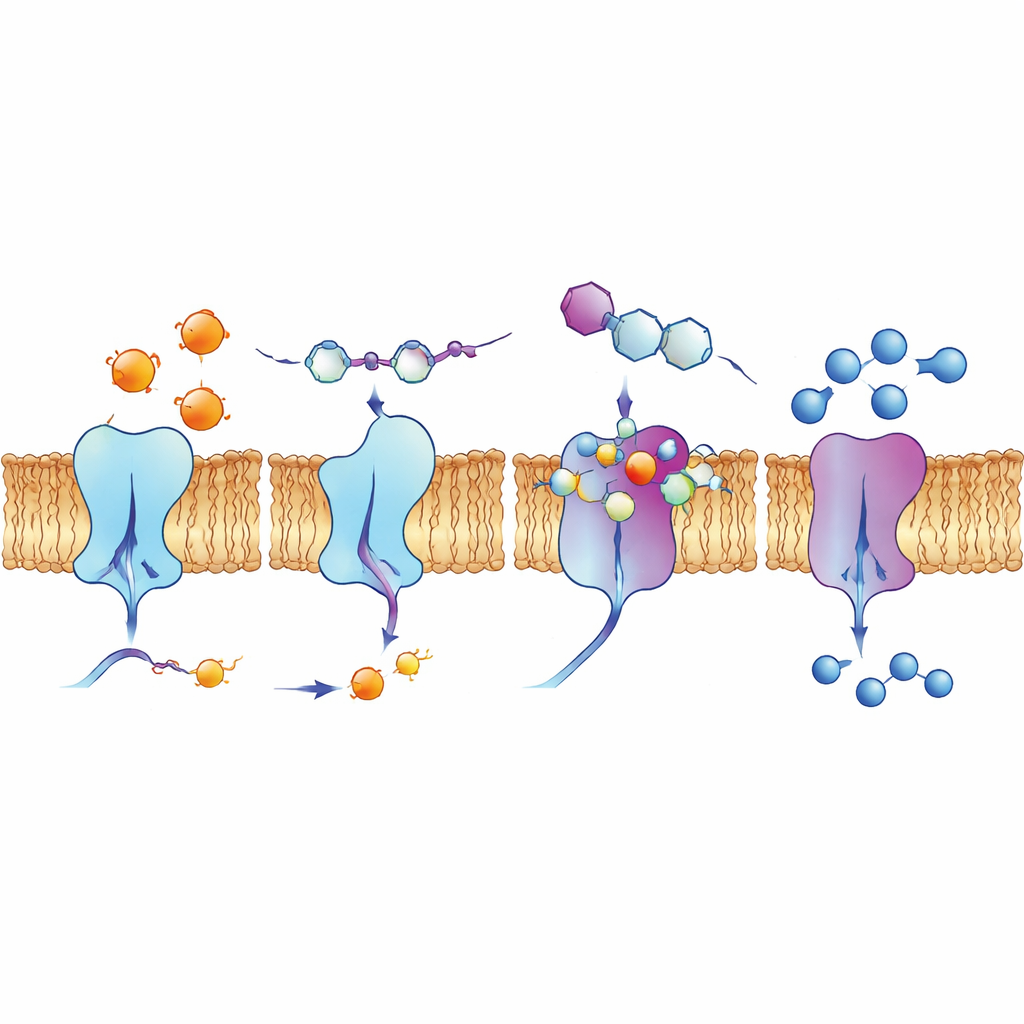
Zaglądanie w kieszenie wiążące i do żywych komórek
Aby zrozumieć, dlaczego niektóre związki działały tak dobrze, autorzy użyli symulacji dokowania komputerowego oraz obliczeń chemii kwantowej. Modele pokazały, jak cząsteczki oparte na chinolinie wpasowują się w szczeliny na powierzchniach enzymów, tworząc sieci oddziaływań przyciągających, w tym wiązań wodorowych, oddziaływań stakujących pomiędzy płaskimi pierścieniami oraz interakcji z halogenami takimi jak fluor, chlor czy jod. Obliczenia rozkładu elektronów wspierały tezę, że najbardziej aktywne związki mają odpowiednią równowagę stabilności i reaktywności, by angażować naładowane miejsca w enzymach. Zespół zbadał też zachowanie jednego związku wiodącego, 4d, w komórkach ludzkiego raka płuca metodami fluorescencyjnymi. Związek naturalnie świeci pod określonym światłem, a obrazy wykazały jego kumulację wzdłuż błony komórkowej — właśnie tam, gdzie znajdują się ektonukleotydazy — sugerując, że może on docierać do zamierzonych celów w realistycznym środowisku biologicznym.
Pierwsze kroki w kierunku działania przeciwnowotworowego
Ponieważ użyteczny lek musi nie tylko trafiać w cel, lecz także wpływać na wzrost komórek nowotworowych, badacze ocenili, jak nowe związki oddziałują z hodowanymi komórkami raka piersi. Kilka pochodnych, zwłaszcza 4j i 4k, zmniejszało przeżywalność komórek i spowalniało ich podziały w czasie, chociaż nie tak silnie jak standardowy lek chemioterapeutyczny. Obliczeniowe przeglądy właściwości wchłaniania, rozprowadzania i podstawowej „lekopodobności” sugerowały, że większość związków ma właściwości zgodne z podawaniem doustnym i potencjalnie może przenikać do mózgu, co stwarza możliwość przyszłych zastosowań w trudno leczonych guzach.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Podsumowując, badanie przedstawia nową rodzinę molekuł opartych na chinolinie, które skutecznie blokują enzymy odpowiedzialne za przekształcanie sygnałów pobudzających układ odpornościowy w tłumiącą adenozynę. Chociaż związki te są na wczesnym etapie i wykazują jedynie umiarkowany bezpośredni efekt cytotoksyczny, stanowią obiecujące narzędzia do przekształcania mikrośrodowiska guza, tak by własne komórki odpornościowe organizmu mogły działać skuteczniej. Przy dalszym dopracowaniu w celu zwiększenia mocy i wybiórczości, takie inhibitory ektonukleotydaz mogłyby w przyszłości uzupełniać istniejące immunoterapie, pomagając rozwiać chemiczną „mgłę” chroniącą guzy przed atakiem.
Cytowanie: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Słowa kluczowe: immunoterapia nowotworów, sygnalizacja adenozynowa, inhibitory enzymów, związki chinolinowe, mikrośrodowisko guza