Clear Sky Science · he
נגזרות חומצה קינולינית-קרבוקסילית כמעכבים עוצמתיים של אקטונוקלאוטידאזות
מדוע חשוב להרגיע את "אות הסכנה" של הסרטן
הסרטן לא רק גדל; הוא גם לומד להסתתר. אחת מהתרמיות המועדפות עליו היא להמיר אות סכנה טבעי שמשתחרר מתאים תחת לחץ לכימיקל מרגיע שמרדיד את המערכת החיסונית. מאמר זה חוקר משפחה חדשה של מולקולות קטנות שמטרתן לקטוע את מסלול המילוט הזה, עם מטרה ארוכת טווח לסייע למערכת ההגנה של הגוף לזהות ולתוקף טוב יותר את הגידולים.
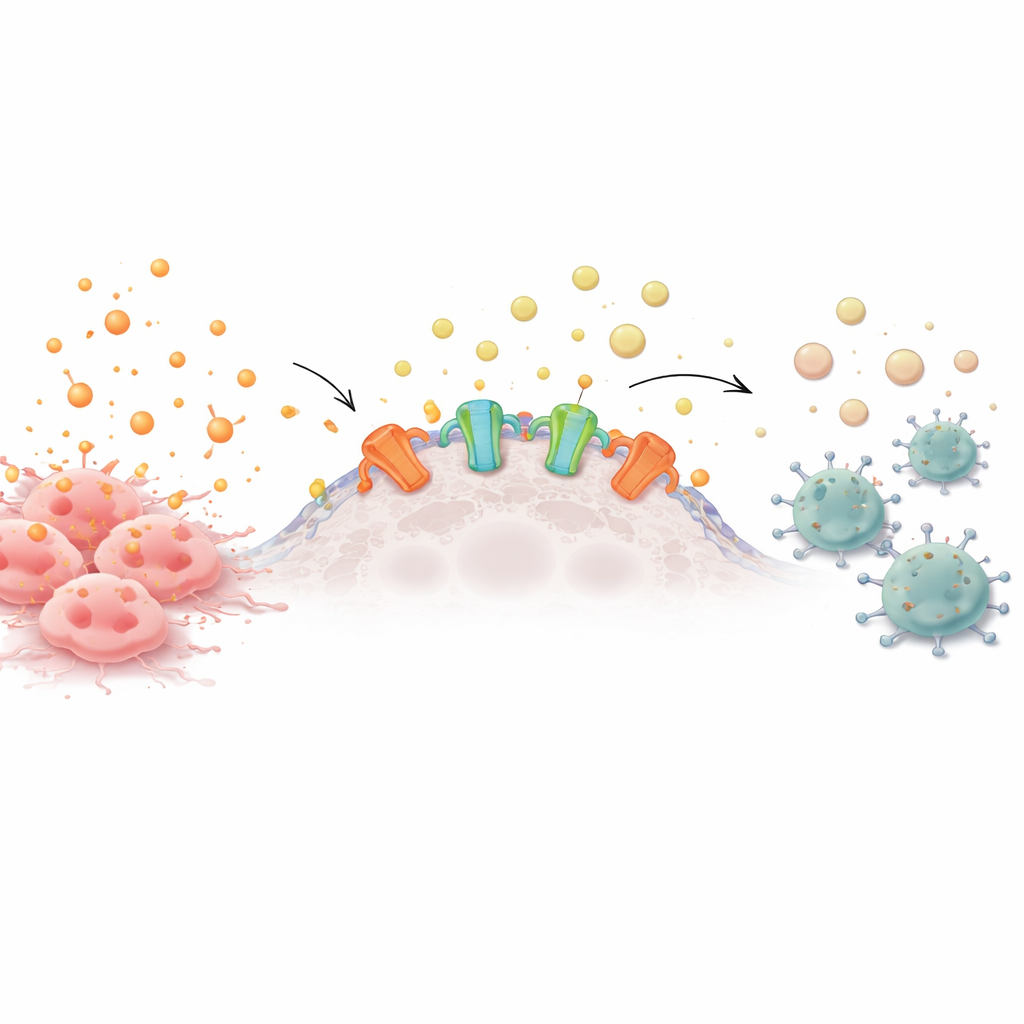
מצופרי אזעקה להשתקה כימית
תאים בריאים וסרטניים משחררים בהתמדה מולקולות נושאות אנרגיה לסביבתם. כאשר מולקולות אלה, כגון ATP, מצטברות מחוץ לתאים, הן פועלות כמו צופרי אזעקה שמושכים תאי חיסון לחקור את הבעיה. על פני השטח של תאים סרטניים רבים, עם זאת, מצויים אנזימים הקרויים אקטונוקלאוטידאזות, הקוצצות בעקביות את ה‑ATP לאדנוזין — אות המרגיע שאומר לתאי החיסון להפסיק לפעול. סרטנים אגרסיביים רבים מייצרים יותר מדי אנזימים אלה, ויוצרים ענן מגן של אדנוזין שמחליש תאי T הסמוכים, תאי ה‑NK ומגינים אחרים.
עיצוב חוסמים כימיים חדשים
החוקרים יצאו לעצב ולסנתז ערכה של שתים-עשרה תרכובות קרובות, המבוססות על ליבת קינולין — מבנה שטוח בעל טבעת שכבר ידוע כאינטראקטיבי עם מטרות ביולוגיות ובעל פוטנציאל אנטי־סרטני. על ידי חיבור קבוצות כימיות שונות לליבה זו, הם יצרו ספרייה קטנה של נגזרות קינולין‑6‑קרבוקסאמיד. מולקולות אלה עברו תיאור קפדני בעזרת כלים כימיים סטנדרטיים לאימות המבנה והטוהר, ולאחר מכן נבדקו מול מספר אקטונוקלאוטידאזות מפתח, כולל ארבעה חברים המעבדים ATP וחומרים קשורים, וכן שני אנזימים הממלאים את הצעד הסופי ביצירת אדנוזין.
איתור החוסמים היעילים ביותר של אנזימים
כאשר המולקולות החדשות תווספו לאנזימים אנושיים מזוקים במעבדה, כמה מהן בלטו כחוסמות חזקות. תרכובת אחת, המסומנת 4d, השתקה בעוצמה שני אנזימים מעבדי ATP (h‑NTPDase1 ו‑h‑NTPDase2) בריכוזים נמוכים מאוד, מה שמציבה אותה כמועמד מבטיח כמעכב רחב־פעולה. נגזרות אחרות הציגו התנהגות סלקטיבית יותר: תרכובת 4a חסמה בעוצמה את אקטו‑5′‑נוקלאוטידאז, המבצע את הקיצוץ האחרון שמייצר אדנוזין; 4k הייתה הטובה ביותר בחסימת האנזים ENPP1; ו‑4b ו‑4g היו יעילות במיוחד נגד תת‑סוגים שונים של NTPDase. בהשוואת קישוטים כימיים שהגבימו או החלישו את הפעילות, הצוות מיפוי כיצד שינויים זעירים במבנה יכולים לכוונן באופן דרמטי את עוצמת וסלקטיביות החסימה.
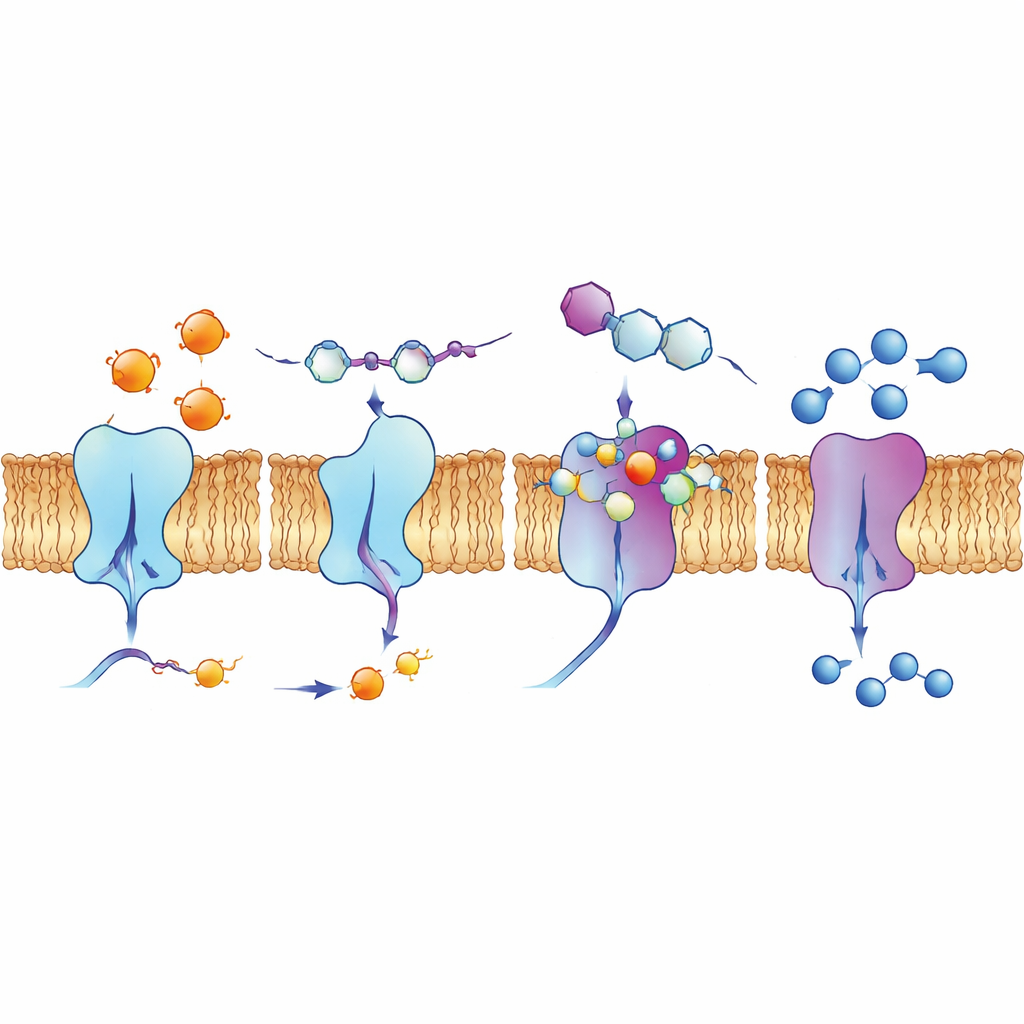
צפייה בכיסי קשירה ובתאים חיים
כדי להבין מדוע תרכובות מסוימות עבדו כל כך טוב, המחברים השתמשו בהדמיות דוקינג ממוחשבות ובחישובי כימיה קוונטית. מודלים אלה הראו כיצד המולקולות מבוססות הקינולין מתמקמות בשקעים על פני שטח האנזימים, יוצרות רשתות של כוחות אטרקטיביים, כולל קשרי מימן, שכבות סטאקינג בין טבעות שטוחות ואינטראקציות הקשורות להלוגנים כגון פלואור, כלור או יוד. חישובים של התפלגות אלקטרונים תמכו ברעיון שהתרכובות הפעילות ביותר מאוזנות נכון מבחינת יציבות וריאקטיביות כדי לקשור את האתרים המטענים באנזימים. הצוות גם בחן כיצד מולקולה מובילה אחת, 4d, מתנהגת בתאי ריאה סרטניים אנושיים באמצעות שיטות פלואורסנציה. היא זוהרת באופן טבעי באור מסוים, והדמיה הראתה שהיא מרוכזת לאורך ממברנת התא — המיקום שבו נמצאים האנזימים אקטונוקלאוטידאז — מה שמרמז שהיא יכולה להגיע למטרותיה בסביבה ביולוגית ריאליסטית.
צעדים ראשונים לכיוון פעולה אנטי־סרטנית
מאחר שתרופה שימושית חייבת לא רק לפגוע במטרה אלא גם להשפיע על גדילת תאי הסרטן, החוקרים בדקו כיצד המולקולות החדשות משפיעות על תאי סרטן השד הגודלים בתרבית. כמה נגזרות, במיוחד 4j ו‑4k, הפחיתו הישרדות תאים והאטו חלוקה תאית לאורך זמן, אם כי לא בעוצמה של כדור כימותרפי סטנדרטי. בדיקות חישוביות של ספיגה, התפוצה ותכונות בסיסיות של דמיון לתרופה הציעו שלרוב התרכובות יש תכונות התואמות לשימוש פומי ויכולת פוטנציאלית להגיע למוח, מה שמעלה אפשרות ליישומים עתידיים בגידולים שקשה לטפל בהם.
מה משמעות הדבר עבור טיפולים עתידיים בסרטן
בסך הכל, המחקר מציג משפחה חדשה של מולקולות מבוססות קינולין היכולות לחסום ביעילות אנזימים שאחראים להפיכת אותות מעוררי חיסון לאדנוזין המדכא את המערכת. אמנם התרכובות הללו נמצאות בשלבים ראשוניים ומראות רק השפעות ישירות מתונות על הריגת תאים, הן מהוות כלי מבטיח לעיצוב מחדש של מיקרו־סביבת הגידול כדי שתאי החיסון של הגוף יוכלו לפעול ביעילות רבה יותר. עם שיפור נוסף להגברת החוזקה והסלקטיביות, מעכבים כאלה של אקטונוקלאוטידאזות עשויים בעתיד להשלים אימונותרפיות קיימות ולסייע בהרמת ה"ערפל" הכימי שמגן על הגידולים מפני התקפה.
ציטוט: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
מילות מפתח: אימונותרפיה של סרטן, אותות אדנוזין, מעכבי אנזימים, תרכובות קינולין, מיקרו־סביבת הגידול