Clear Sky Science · pt
Derivados do ácido quinolínico como inibidores potentes de ectonucleotidases
Por que acalmar o “sinal de perigo” do câncer importa
O câncer não apenas cresce; ele também aprende a se esconder. Um de seus truques favoritos é converter um sinal natural de perigo liberado por células estressadas em um composto calmante que embota o sistema imunológico. Este artigo explora uma nova família de pequenas moléculas que visam interromper essa rota de escape, com o objetivo de longo prazo de ajudar as defesas do próprio corpo a reconhecer e atacar melhor os tumores.
De alarmes a silêncio químico
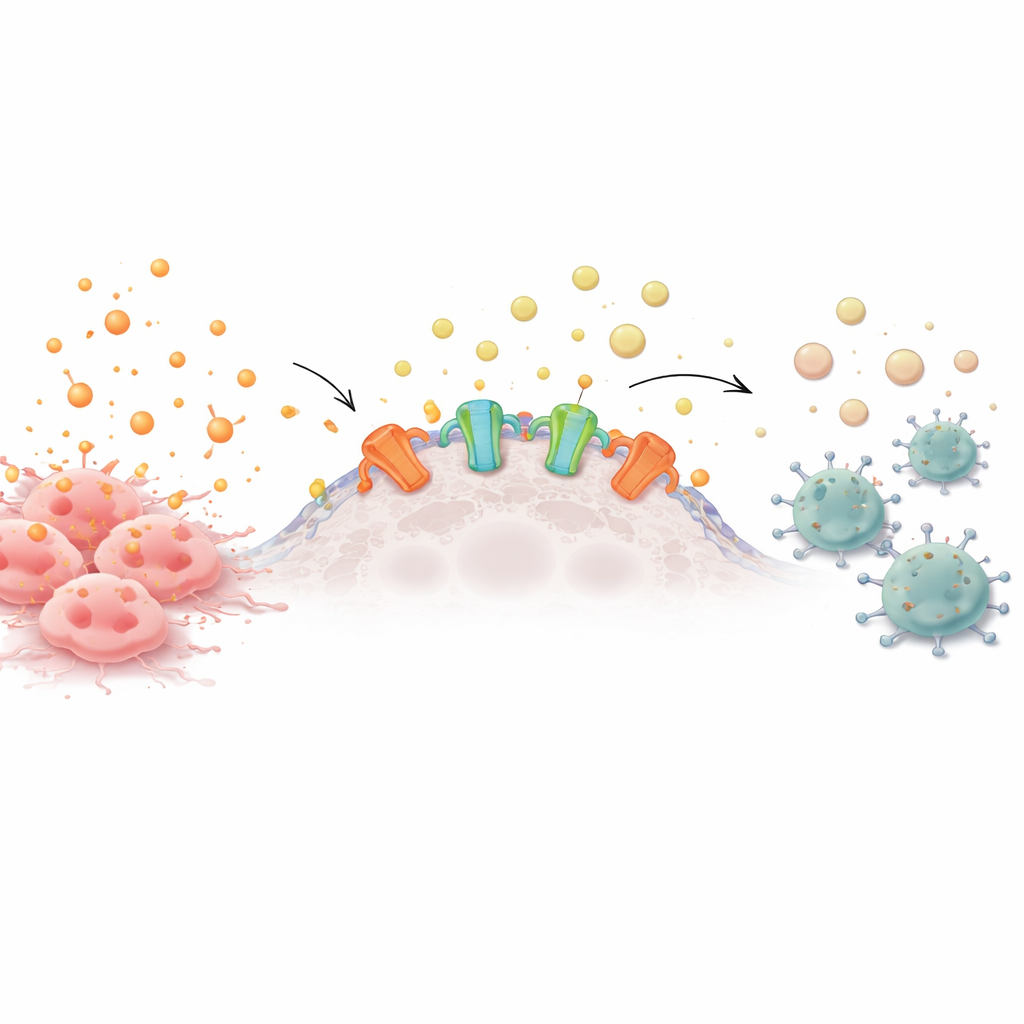
Células saudáveis e cancerosas liberam continuamente moléculas carregadoras de energia para o ambiente. Quando essas moléculas, como o ATP, se acumulam fora das células, atuam como alarmes, atraindo células imunes para investigar problemas. Na superfície de muitas células tumorais, porém, existem enzimas chamadas ectonucleotidases que gradualmente degradam o ATP em adenosina, um sinal calmante que manda as células imunes recuarem. Muitos cânceres agressivos superproduzem essas enzimas, criando uma nuvem protetora de adenosina que enfraquece células T próximas, células natural killer e outros defensores.
Projetando novos bloqueadores químicos
Os pesquisadores procuraram projetar e sintetizar um conjunto de doze compostos relacionados construídos sobre um “núcleo” de quinolina, uma estrutura plana em forma de anel já conhecida por interagir com alvos biológicos e por ter potencial anticâncer. Ao ligar diferentes grupos químicos a esse núcleo, criaram uma pequena biblioteca de derivados de quinolina-6-carboxamida. Essas moléculas foram caracterizadas com cuidado usando ferramentas químicas padrão para confirmar suas estruturas e pureza, e então testadas contra várias ectonucleotidases-chave, incluindo quatro membros que processam ATP e substâncias relacionadas, bem como duas enzimas que realizam o passo final da formação de adenosina.
Encontrando os inibidores enzimáticos mais eficazes
Quando as novas moléculas foram misturadas com enzimas humanas purificadas em laboratório, várias se destacaram como bloqueadores potentes. Um composto, rotulado 4d, inibiu com potência duas enzimas que processam ATP (h-NTPDase1 e h-NTPDase2) em concentrações muito baixas, marcando-o como um promissor inibidor de ação ampla. Outros derivados exibiram comportamento mais seletivo: o composto 4a bloqueou fortemente a ecto-5'-nucleotidase, que realiza o corte final que produz adenosina; o composto 4k foi o melhor em bloquear outra enzima, ENPP1; e os compostos 4b e 4g foram particularmente eficazes contra diferentes subtipos de NTPDase. Ao comparar que modificações químicas melhoraram ou enfraqueceram a atividade, a equipe mapeou como pequenas mudanças na estrutura podem ajustar dramaticamente a força e a seletividade da inibição enzimática.
Observando bolsões de ligação e células vivas
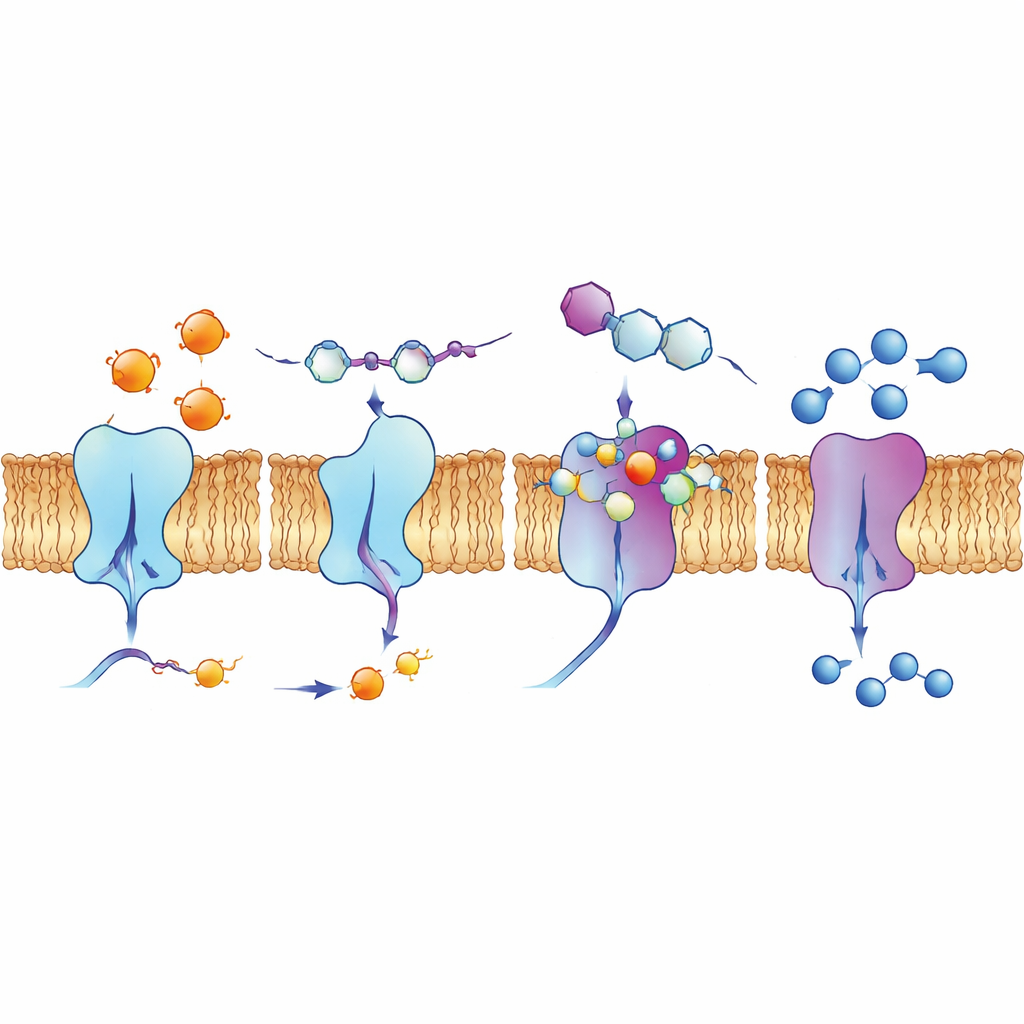
Para entender por que certos compostos funcionaram tão bem, os autores usaram simulações de docking por computador e cálculos de química quântica. Esses modelos mostraram como as moléculas à base de quinolina se alojam em ranhuras nas superfícies enzimáticas, formando redes de forças atrativas, incluindo ligações de hidrogênio, empilhamento entre anéis planos e interações envolvendo halogênios como flúor, cloro ou iodo. Cálculos da distribuição eletrônica sustentaram a ideia de que os compostos mais ativos têm o equilíbrio certo de estabilidade e reatividade para engajar sítios carregados nas enzimas. A equipe também examinou como um composto líder, 4d, se comporta em células humanas de câncer de pulmão usando métodos de fluorescência. Ele apresenta fluorescência natural sob luz específica, e a imagem revelou que se concentra ao longo da membrana celular, o próprio local das ectonucleotidases, sugerindo que pode alcançar seus alvos pretendidos em um contexto biológico realista.
Passos iniciais rumo à ação anticâncer
Como um fármaco útil deve não apenas atingir seu alvo, mas também afetar o crescimento das células cancerosas, os pesquisadores avaliaram como as novas moléculas influenciam células de câncer de mama cultivadas em laboratório. Vários derivados, especialmente 4j e 4k, reduziram a sobrevivência celular e retardaram a divisão celular ao longo do tempo, embora não tão fortemente quanto um quimioterápico padrão. Verificações computacionais de absorção, distribuição e semelhança a fármacos básicas sugeriram que a maioria dos compostos possui propriedades compatíveis com uso oral e potencialmente pode alcançar o cérebro, levantando a possibilidade de aplicações futuras em tumores de difícil tratamento.
O que isso significa para terapias futuras contra o câncer
No geral, o estudo introduz uma nova família de moléculas à base de quinolina que bloqueiam de forma eficiente enzimas responsáveis por transformar sinais que estimulam o sistema imune em adenosina que os reprime. Embora esses compostos estejam em estágio inicial e exibam efeitos diretos de combate ao câncer apenas moderados, eles são ferramentas promissoras para remodelar o microambiente tumoral de modo que as próprias células imunes do corpo possam agir com maior eficácia. Com refinamento adicional para aumentar potência e seletividade, tais inibidores de ectonucleotidases poderiam um dia complementar imunoterapias existentes, ajudando a dissipar a “névoa” química que protege os tumores do ataque.
Citação: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Palavras-chave: imunoterapia contra o câncer, sinalização por adenosina, inibidores de enzimas, compostos de quinolina, microambiente tumoral