Clear Sky Science · sv
Kinolin-karboxylsyraderivat som potenta ectonukleotidasinhibitorer
Varför det spelar roll att dämpa cancerns "fara-signal"
Cancer växer inte bara; den lär sig också att gömma sig. Ett av dess vanligaste trick är att omvandla en naturlig fara-signal som släpps ut av stressade celler till en lugnande kemikalie som får immunsystemet att somna. Denna artikel undersöker en ny familj småmolekyler som syftar till att störa den flyktvägen, med det långsiktiga målet att hjälpa kroppens egna försvar att bättre känna igen och angripa tumörer.
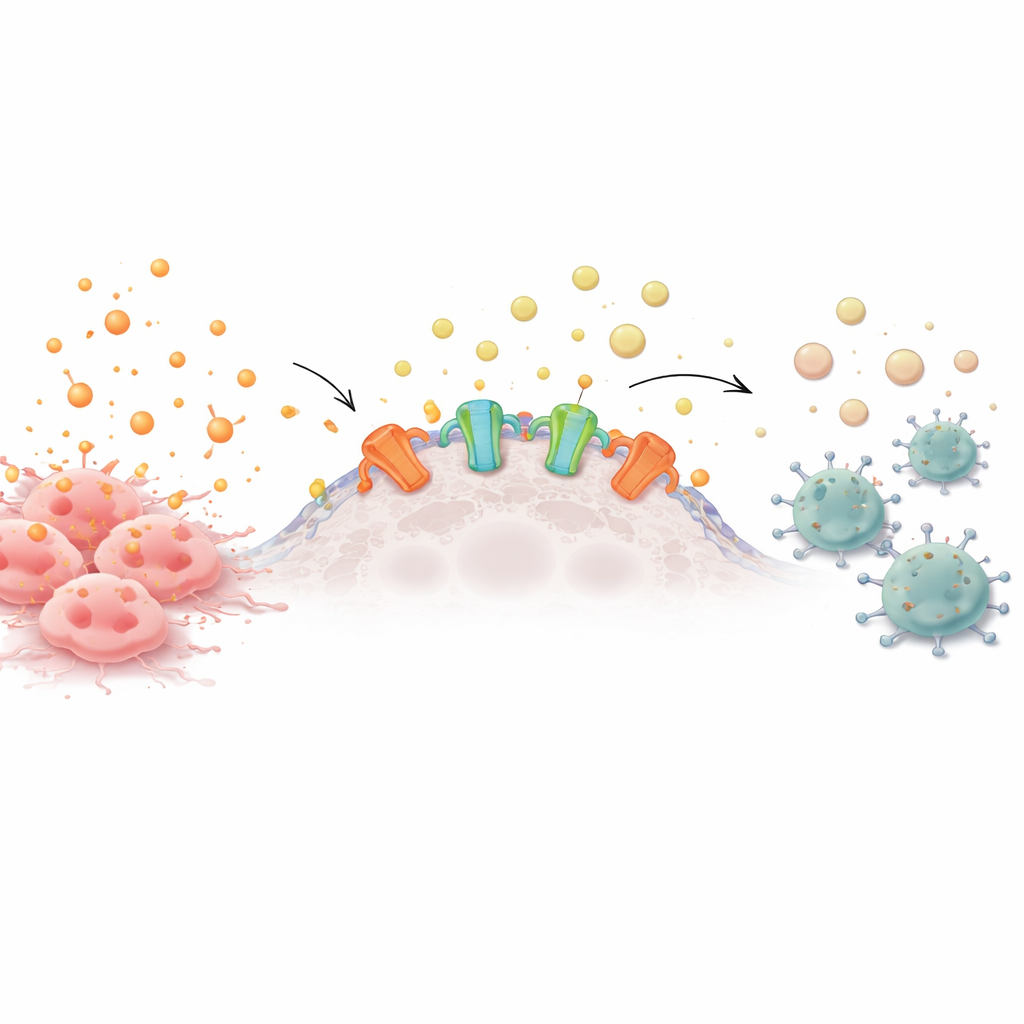
Från alarmklockor till kemisk tystnad
Friska och cancerösa celler släpper ständigt energibärande molekyler ut i sin omgivning. När dessa molekyler, som ATP, byggs upp utanför cellerna fungerar de som alarmklockor och drar till sig immunceller för att undersöka problem. På ytan av många tumörceller finns dock enzymer kallade ectonukleotidaser som stadigt klyver ATP till adenosin, en lugnande signal som säger åt immunceller att avstå. Många aggressiva cancerformer överproducerar dessa enzymer och skapar ett skyddande moln av adenosin som försvagar närliggande T‑celler, naturliga mördarceller och andra försvarsceller.
Design av nya kemiska blockare
Forskarna satte upp för att designa och syntetisera en uppsättning tolv närbesläktade föreningar byggda på en kinolin-"kärna", en platt, ringformad struktur som redan är känd för att interagera med biologiska mål och ha anticancereffekter. Genom att fästa olika kemiska grupper på denna kärna skapade de ett litet bibliotek av kinolin-6-karboxamid-derivat. Dessa molekyler karaktäriserades noggrant med standardkemiska verktyg för att bekräfta struktur och renhet, och testades sedan mot flera viktiga ectonukleotidaser, inklusive fyra medlemmar som bearbetar ATP och närbesläktade substanser, samt två enzymer som utför det sista steget i bildandet av adenosin.
Att hitta de mest effektiva enzymstopparna
När de nya molekylerna blandades med renade mänskliga enzymer i laboratoriet framträdde flera som starka hämmare. En förening, betecknad 4d, stängde effektivt ner två ATP‑bearbetande enzymer (h‑NTPDase1 och h‑NTPDase2) vid mycket låga koncentrationer, vilket gör den till en lovande bredverkande hämmare. Andra derivat visade mer selektivt beteende: förening 4a blockerade starkt ecto‑5′‑nukleotidas, som utför den sista klyvningen som bildar adenosin; förening 4k var bäst på att blockera ett annat enzym, ENPP1; och föreningarna 4b och 4g var särskilt effektiva mot olika NTPDase‑subtyper. Genom att jämföra vilka kemiska modifieringar som förbättrade eller försvagade aktiviteten kartlade teamet hur små förändringar i struktur dramatiskt kan ställa in enzymhämmningsstyrka och selektivitet.
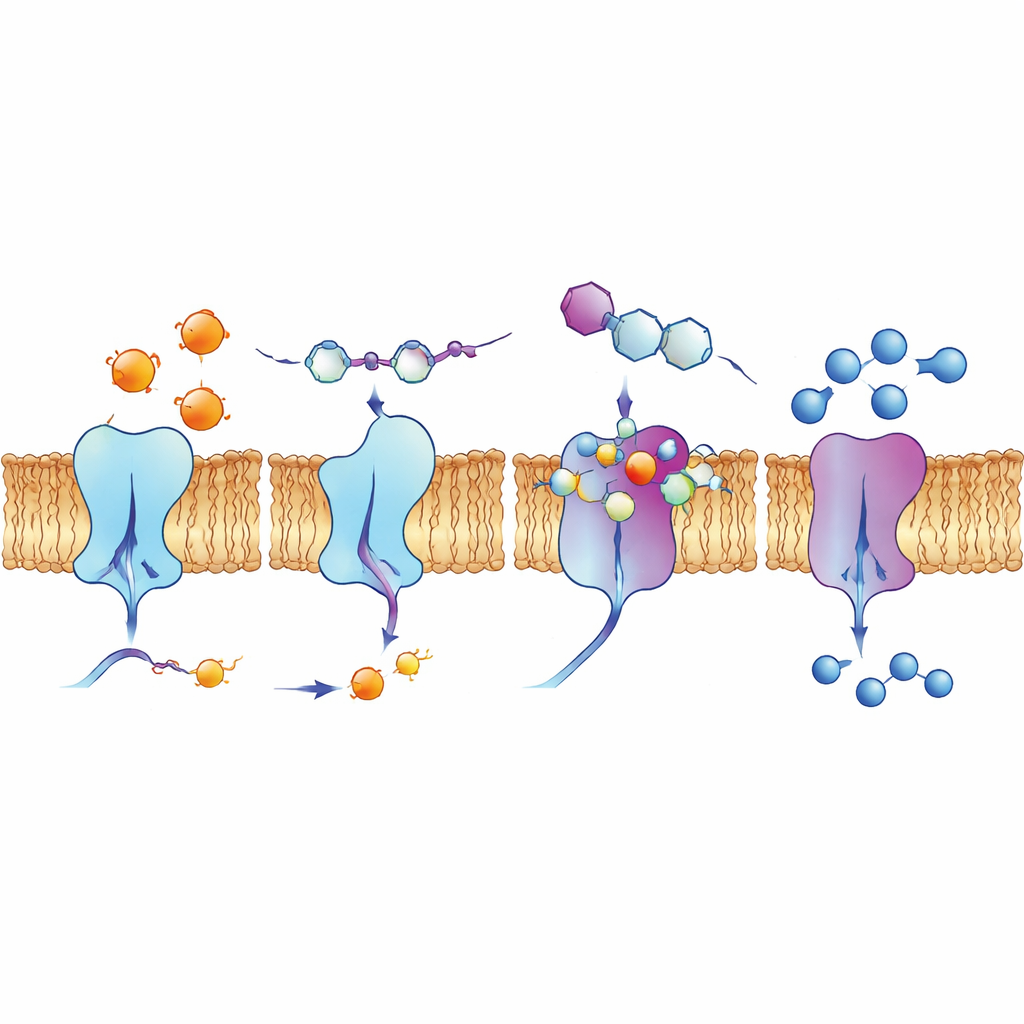
Insyn i bindningsfickor och levande celler
För att förstå varför vissa föreningar fungerade så bra använde författarna datorbaserade dockningssakkon och kvantkemiska beräkningar. Dessa modeller visade hur kinolinbaserade molekyler vilar i fåror på enzymens ytor och bildar nätverk av attraktiva krafter, inklusive vätebindningar, stapling mellan platta ringar och interaktioner som involverar halogener såsom fluor, klor eller jod. Beräkningar av elektrondistribution stödde idén att de mest aktiva föreningarna har rätt balans mellan stabilitet och reaktivitet för att engagera laddade platser i enzymerna. Teamet undersökte också hur en ledande förening, 4d, beter sig i mänskliga lungcancerceller med hjälp av fluorescensmetoder. Den fluorescerar naturligt under specifikt ljus, och avbildning visade att den koncentreras längs cellmembranet — just där ectonukleotidaserna sitter — vilket tyder på att den kan nå sina avsedda mål i en realistisk biologisk miljö.
Tidiga steg mot anticancerverkan
Ett användbart läkemedel måste inte bara slå mot sitt mål utan även påverka cancercells tillväxt, så forskarna bedömde hur de nya molekylerna påverkar bröstcancerceller odlade i kultur. Flera derivat, särskilt 4j och 4k, minskade cellöverlevnad och bromsade celldelning över tid, om än inte lika kraftfullt som ett standardkemoterapeutikum. Beräkningar av absorption, distribution och grundläggande läkemedelsliknande egenskaper antydde att de flesta föreningar har egenskaper förenliga med oral användning och potentiellt kan nå hjärnan, vilket öppnar möjligheten för framtida tillämpningar i svårbehandlade tumörer.
Vad detta betyder för framtida cancerbehandlingar
Sammanfattningsvis introducerar studien en ny familj kinolinbaserade molekyler som effektivt blockerar enzymer ansvariga för att omvandla immunstimulerande signaler till immundämpande adenosin. Även om dessa föreningar befinner sig i ett tidigt skede och endast uppvisar måttliga direkta cancerdödande effekter, är de lovande verktyg för att omforma tumörmiljön så att kroppens egna immunceller kan verka mer effektivt. Med vidare förfining för att öka potens och selektivitet skulle sådana ectonukleotidasinhibitorer en dag kunna komplettera befintliga immunoterapier och hjälpa till att lyfta den kemiska "dimma" som skyddar tumörer från angrepp.
Citering: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Nyckelord: cancerimmunterapi, adenosinsignalering, enzymhämmare, kinolinföreningar, tumörmikromiljö