Clear Sky Science · it
Derivati dell'acido chinolinicarbossilico come potenti inibitori delle ectonucleotidasi
Perché è importante attenuare il “segnale di pericolo” del cancro
Il cancro non si limita a proliferare; impara anche a nascondersi. Uno dei suoi trucchi preferiti è trasformare un segnale di pericolo naturale rilasciato da cellule sotto stress in una sostanza chimica tranquillizzante che assopisce il sistema immunitario. Questo articolo esplora una nuova famiglia di piccole molecole che mirano a interrompere quella via di fuga, con l'obiettivo a lungo termine di aiutare le difese dell'organismo a riconoscere e attaccare meglio i tumori.
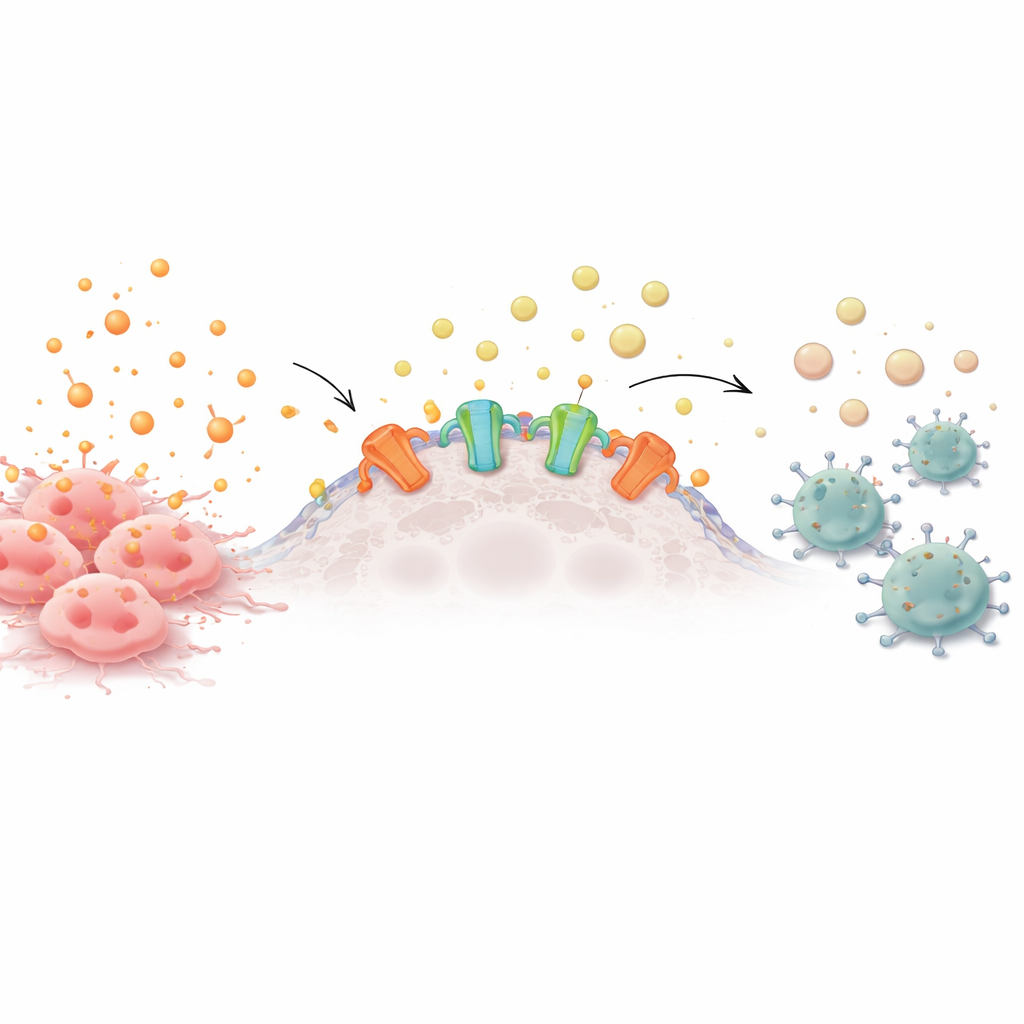
Dai campanelli d'allarme al silenzio chimico
Cellule sane e tumorali rilasciano costantemente molecole che trasportano energia nel loro intorno. Quando queste molecole, come l'ATP, si accumulano all'esterno delle cellule, funzionano da campanelli d'allarme che richiamano cellule immunitarie per investigare il problema. Sulla superficie di molte cellule tumorali, però, sono presenti enzimi chiamati ectonucleotidasi che degradano gradualmente l'ATP in adenosina, un segnale calmante che dice alle cellule immunitarie di abbassare la guardia. Molti tumori aggressivi sovrapproducono questi enzimi, creando una nube protettiva di adenosina che indebolisce le cellule T, le cellule natural killer e altri difensori nelle vicinanze.
Progettare nuovi bloccanti chimici
I ricercatori si sono prefissati di progettare e sintetizzare una serie di dodici composti correlati basati su un “nucleo” chinolinico, una struttura piatta a forma di anello già nota per interagire con bersagli biologici e per il suo potenziale antitumorale. Attaccando diversi gruppi chimici a questo nucleo, hanno creato una piccola libreria di derivati della chinolina-6-carbossamide. Queste molecole sono state accuratamente caratterizzate con strumenti chimici standard per confermarne struttura e purezza, quindi testate contro diverse ectonucleotidasi chiave, inclusi quattro membri che processano ATP e sostanze correlate, oltre a due enzimi che completano l'ultimo passo nella produzione di adenosina.
Trovare i bloccanti enzimatici più efficaci
Quando le nuove molecole sono state mescolate con enzimi umani purificati in laboratorio, diverse sono emerse come forti inibitori. Un composto, etichettato 4d, ha spento con potenza due enzimi che processano ATP (h-NTPDase1 e h-NTPDase2) a concentrazioni molto basse, segnalando il suo potenziale come inibitore ad ampio spettro. Altri derivati hanno mostrato un comportamento più selettivo: il composto 4a ha bloccato con forza l'ecto-5′-nucleotidasi, che esegue l'ultima scissione che produce adenosina; il composto 4k è stato il migliore nel bloccare un altro enzima, ENPP1; e i composti 4b e 4g sono stati particolarmente efficaci contro diversi sottotipi di NTPDase. Confrontando quali modifiche chimiche miglioravano o indebolivano l'attività, il gruppo ha mappato come piccoli cambiamenti strutturali possano modulare in modo deciso potenza e selettività dell'inibizione enzimatica.
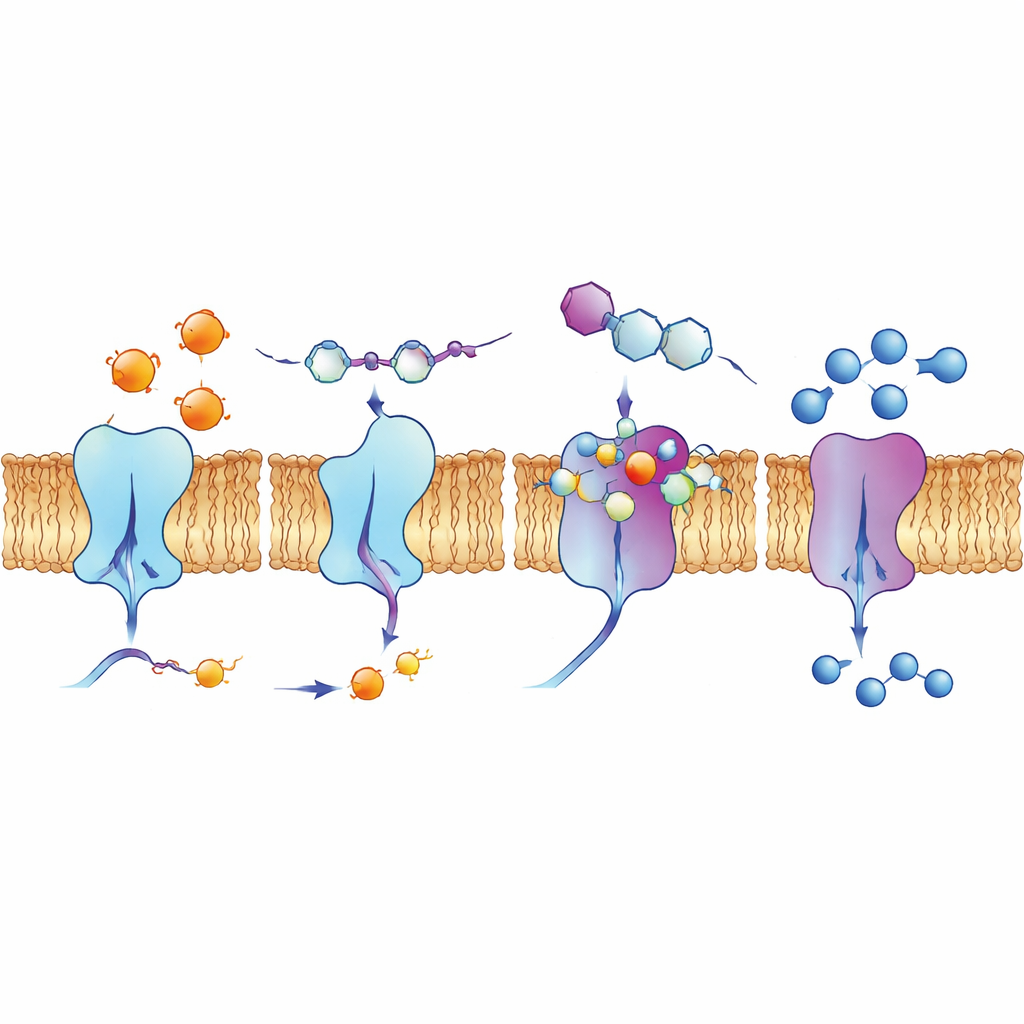
Uno sguardo nelle tasche di legame e nelle cellule vive
Per capire perché alcuni composti funzionassero così bene, gli autori hanno usato simulazioni di docking al computer e calcoli di chimica quantistica. Questi modelli hanno mostrato come le molecole a base di chinolina si incastrino nelle scanalature delle superfici enzimatiche, formando reti di forze attrattive, inclusi legami a idrogeno, stacking tra anelli piatti e interazioni che coinvolgono alogeni come fluoro, cloro o iodio. I calcoli della distribuzione elettronica hanno supportato l'idea che i composti più attivi abbiano il giusto equilibrio di stabilità e reattività per impegnarsi con siti caricati negli enzimi. Il team ha anche esaminato il comportamento di un composto guida, 4d, in cellule di carcinoma polmonare umano usando metodi di fluorescenza. Il composto emette naturalmente fluorescenza sotto luce specifica, e le immagini hanno rivelato che si concentra lungo la membrana cellulare, proprio dove si trovano le ectonucleotidasi, suggerendo che può raggiungere i bersagli previsti in un contesto biologico realistico.
Primi passi verso un'azione antitumorale
Poiché un farmaco utile deve non solo colpire il bersaglio ma anche influenzare la crescita delle cellule tumorali, i ricercatori hanno valutato come le nuove molecole influenzino cellule di carcinoma mammario coltivate in vitro. Diversi derivati, in particolare 4j e 4k, hanno ridotto la sopravvivenza cellulare e rallentato la divisione nel tempo, sebbene non con la stessa intensità di un chemioterapico standard. Controlli computazionali sull'assorbimento, distribuzione e le proprietà fondamentali di drug-likeness hanno suggerito che la maggior parte dei composti possiede caratteristiche compatibili con l'uso per via orale e può potenzialmente raggiungere il cervello, aprendo la possibilità di applicazioni future in tumori difficili da trattare.
Cosa significa per le terapie oncologiche future
Nel complesso, lo studio introduce una nuova famiglia di molecole a base di chinolina che bloccano in modo efficiente gli enzimi responsabili della trasformazione di segnali immunostimolanti in adenosina immunosopprimente. Pur trovandosi a uno stadio iniziale e mostrando solo effetti diretti moderati sulla uccisione delle cellule tumorali, queste molecole sono strumenti promettenti per rimodellare il microambiente tumorale in modo che le cellule immunitarie dell'organismo possano operare con maggiore efficacia. Con ulteriori perfezionamenti per aumentare potenza e selettività, tali inibitori delle ectonucleotidasi potrebbero un giorno affiancare le immunoterapie esistenti, contribuendo a dissolvere la “nebbia” chimica che protegge i tumori dall'attacco.
Citazione: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Parole chiave: immunoterapia oncologica, segnalazione dell'adenosina, inibitori enzimatici, composti chinolinici, microambiente tumorale