Clear Sky Science · ru
Производные хинолинкарбоновой кислоты как мощные ингибиторы экто-нуклеотидаз
Почему важно усмирить «сигнал опасности» рака
Рак не только растет; он также учится прятаться. Один из его любимых трюков — превращать естественный сигнал опасности, выделяемый стрессированными клетками, в успокаивающее химическое вещество, которое усыпляет иммунную систему. В этой статье рассматривается новая семья малых молекул, нацеленных на разрушение этого пути уклонения, с долговременной целью помочь собственным защитным силам организма лучше распознавать и атаковать опухоли.
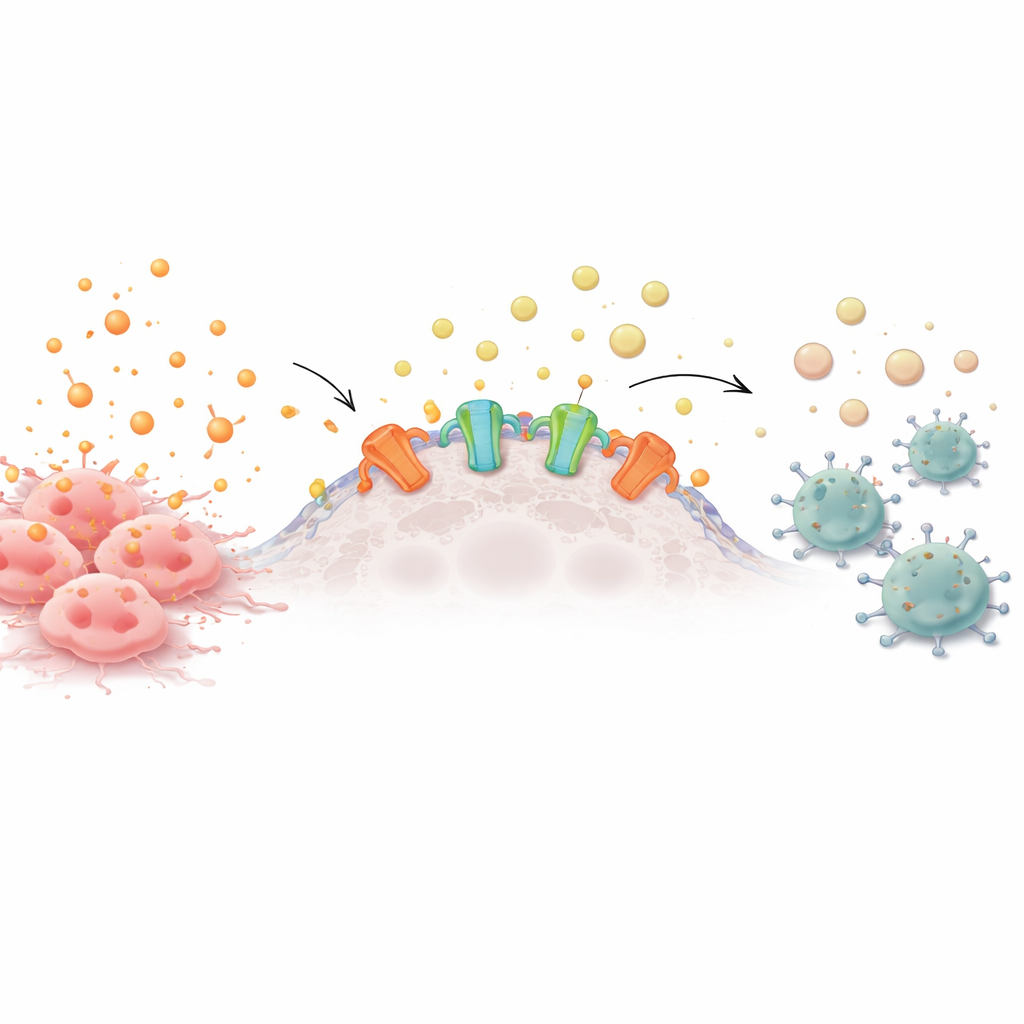
От тревожных сигналов к химической тишине
Здоровые и раковые клетки постоянно выбрасывают в окружение молекулы, несущие энергию. Когда эти молекулы, такие как АТФ, накапливаются вне клеток, они действуют как тревожные звонки, привлекая иммунные клетки для проверки проблемы. Однако на поверхности многих опухолевых клеток находятся ферменты, называемые эктону-клеотидазами, которые постепенно расщепляют АТФ до аденозина — успокаивающего сигнала, приказывающего иммунным клеткам отступить. Многие агрессивные виды рака перепроизводят эти ферменты, создавая защитное облако аденозина, которое ослабляет близлежащие Т‑клетки, естественные киллеры и других защитников.
Проектирование новых химических блокаторов
Исследователи поставили задачу спроектировать и синтезировать набор из двенадцати родственных соединений на основе хинолинового «каркаса» — плоской циклической структуры, уже известной взаимодействием с биологическими мишенями и обладающей противораковым потенциалом. При присоединении различных химических групп к этому ядру они получили небольшую библиотеку производных хинолин-6-карбоксамида. Эти молекулы тщательно характеризовали стандартными методами химии, чтобы подтвердить их строение и чистоту, а затем тестировали против нескольких ключевых эктону-клеотидаз, включая четыре фермента, перерабатывающие АТФ и родственные вещества, а также два фермента, завершающих последний шаг образования аденозина.
Поиск наиболее эффективных тормозов ферментов
Когда новые молекулы смешивали с очищенными человеческими ферментами в лаборатории, несколько из них выделялись как сильные ингибиторы. Одно соединение, обозначенное как 4d, мощно блокировало два фермента, перерабатывающих АТФ (h‑NTPDase1 и h‑NTPDase2), при очень низких концентрациях, что выделяет его как перспективный широкодейственный ингибитор. Другие производные проявили более селективное поведение: соединение 4a сильно блокировало экто‑5′‑нуклеотидазу, выполняющую последний разрез, приводящий к образованию аденозина; соединение 4k оказалось лучшим в блокировании фермента ENPP1; а соединения 4b и 4g были особенно эффективны против разных подтипов NTPDase. Сравнивая, какие химические «украшения» усиливали или ослабляли активность, команда построила карту того, как небольшие изменения в структуре могут существенно регулировать силу и селективность блокирования ферментов.
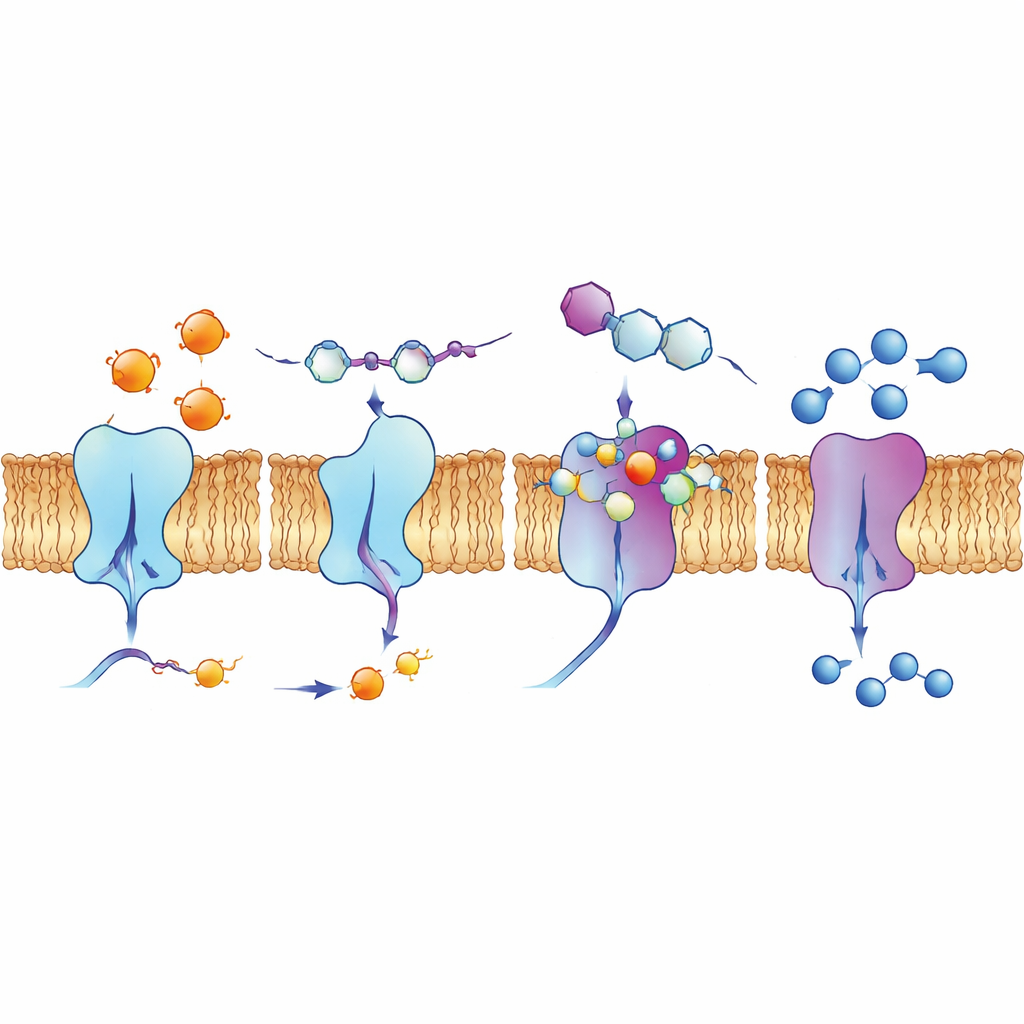
Заглядывая в карманы связывания и в живые клетки
Чтобы понять, почему некоторые соединения работали так хорошо, авторы использовали компьютерное докирование и расчеты квантовой химии. Эти модели показали, как хинолиновые молекулы располагаются в бороздках на поверхности ферментов, формируя сети привлекательных взаимодействий, включая водородные связи, стаккинг между плоскими кольцами и взаимодействия с галогенами, такими как фтор, хлор или йод. Расчеты распределения электронов поддержали идею о том, что наиболее активные соединения имеют правильный баланс стабильности и реакционной способности для взаимодействия с заряженными участками ферментов. Команда также исследовала поведение одного лидирующего соединения, 4d, в клетках рака легкого человека с помощью флуоресцентных методов. Оно естественным образом флюоресцирует при определенном свете, и визуализация показала его концентрацию вдоль клеточной мембраны — именно там находятся эктону-клеотидазы — что указывает на способность достигать целевых участков в реалистичных биологических условиях.
Ранние шаги к противораковой активности
Поскольку полезное лекарство должно не только попадать в мишень, но и влиять на рост раковых клеток, исследователи оценили, как новые молекулы влияют на клетки рака молочной железы в культуре. Несколько производных, особенно 4j и 4k, снижали выживаемость клеток и замедляли их деление со временем, хотя и не так сильно, как стандартный химиотерапевтический препарат. Компьютерные проверки абсорбции, распределения и базовой «лекарственной подобности» показали, что большинство соединений обладают свойствами, совместимыми с пероральным применением, и потенциально могут проникать в мозг, что открывает возможность будущего использования против трудноизлечимых опухолей.
Что это значит для будущих терапий рака
В целом исследование представляет новую семью хинолиновых молекул, которые эффективно блокируют ферменты, превращающие иммуноподдерживающие сигналы в иммуноподавляющий аденозин. Хотя эти соединения находятся на ранней стадии и демонстрируют лишь умеренные прямые цитотоксические эффекты, они представляют собой многообещающие инструменты для изменения микроокружения опухоли, чтобы собственные иммунные клетки организма работали эффективнее. При дальнейшем совершенствовании для повышения мощности и селективности такие ингибиторы эктону-клеотидаз могли бы в будущем дополнять существующие иммунотерапии, помогая рассеять химический «туман», который скрывает опухоли от атаки.
Цитирование: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Ключевые слова: иммунотерапия рака, аденозиновая сигнализация, ингибиторы ферментов, хинолиновые соединения, микроокружение опухоли