Clear Sky Science · nl
Derivaten van kinoline-carboxylzuur als krachtige ectonucleotidase-remmers
Waarom het dempen van het kankers ‘gevaarsein’ ertoe doet
Kanker groeit niet alleen; het leert zich ook verbergen. Een van zijn favoriete trucs is een natuurlijk gevaarsein dat door gestreste cellen wordt vrijgegeven omzetten in een kalmerend chemisch middel dat het immuunsysteem in slaap sust. Dit artikel onderzoekt een nieuwe familie van kleine moleculen die dat ontsnappingspad willen verstoren, met als langetermijndoel de eigen afweer van het lichaam beter tumoren te laten herkennen en aanvallen.
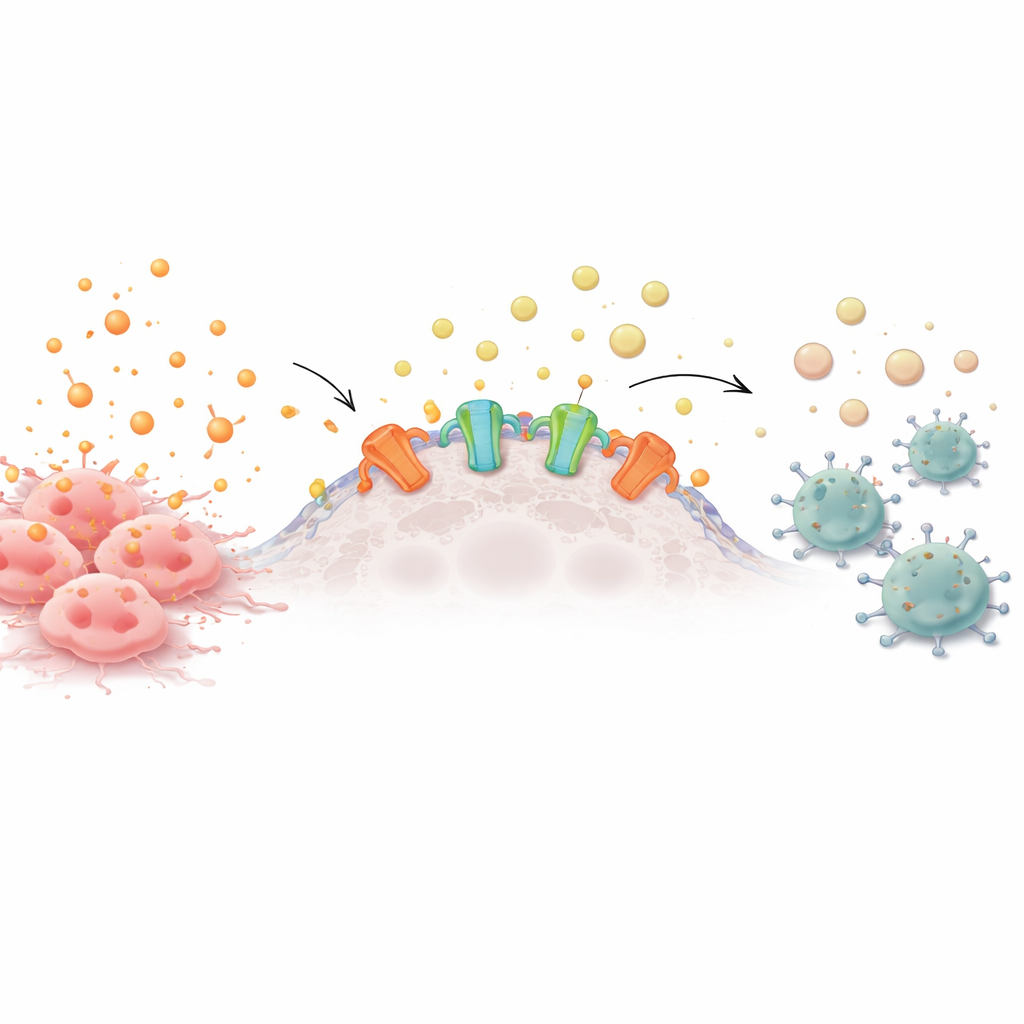
Van alarmbellen naar chemische stilte
Gezonde en kankercellen geven voortdurend energiedragende moleculen aan hun omgeving af. Wanneer deze moleculen, zoals ATP, buitencellig ophopen, fungeren ze als alarmbellen die immuuncellen aantrekken om onderzoek te doen. Op het oppervlak van veel tumorcellen bevinden zich echter enzymen die ectonucleotidases heten en die ATP gestaag afbreken tot adenosine, een kalmerend signaal dat immuuncellen opdraagt zich terug te trekken. Veel agressieve kankers produceren deze enzymen in overmaat en creëren zo een beschermende wolk van adenosine die nabijgelegen T-cellen, natural killer-cellen en andere verdedigers verzwakt.
Ontwerpen van nieuwe chemische blokkeringen
De onderzoekers wilden een reeks van twaalf verwante verbindingen ontwerpen en synthetiseren, gebaseerd op een kinoline “kern”, een platte, ringvormige structuur die al bekendstaat om interactie met biologische doelen en potentie tegen kanker. Door verschillende chemische groepen aan deze kern te koppelen creëerden ze een kleine bibliotheek van kinoline-6-carboxamide-derivaten. Deze moleculen werden zorgvuldig gekarakteriseerd met standaard chemische technieken om hun structuur en zuiverheid te bevestigen, en vervolgens getest tegen meerdere sleutel-ectonucleotidases, waaronder vier leden die ATP en aanverwante stoffen verwerken, en twee enzymen die de laatste stap naar adenosine voltooien.
Het vinden van de meest effectieve enzymblokkers
Toen de nieuwe moleculen in het laboratorium werden gemengd met gezuiverde menselijke enzymen, vielen er meerdere op als sterke blokkeringen. Eén verbinding, aangeduid als 4d, schakelde krachtig twee ATP-verwerkende enzymen uit (h-NTPDase1 en h-NTPDase2) bij zeer lage concentraties, wat het markeert als een veelbelovende breedwerkende remmer. Andere derivaten vertoonden meer selectief gedrag: verbinding 4a blokkeerde sterk ecto-5′-nucleotidase, dat de laatste knip uitvoert die adenosine produceert; verbinding 4k was het beste in het blokkeren van een ander enzym, ENPP1; en verbindingen 4b en 4g waren bijzonder effectief tegen verschillende NTPDase-subtypen. Door te vergelijken welke chemische toevoegingen de activiteit verbeterden of verzwakten, bracht het team in kaart hoe kleine structurele veranderingen de kracht en selectiviteit van enzymremming drastisch kunnen afstemmen.
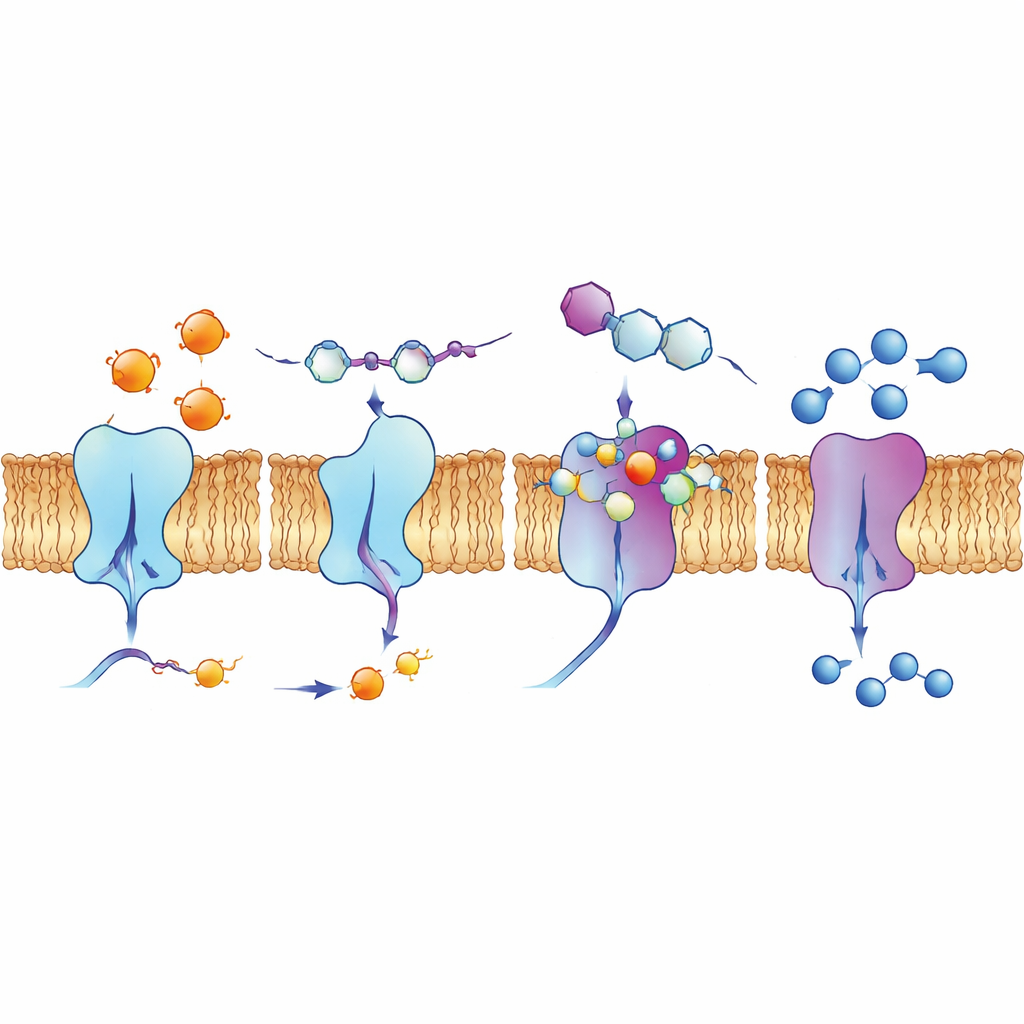
In de bindingsgaten en levende cellen kijken
Om te begrijpen waarom bepaalde verbindingen zo goed werkten, gebruikten de auteurs computergestuurde docking-simulaties en kwantumchemische berekeningen. Deze modellen toonden hoe de op kinoline gebaseerde moleculen in groeven op de enzymoppervlakken passen en netwerken van aantrekkingskrachten vormen, waaronder waterstofbruggen, stapeling tussen platte ringen en interacties met halogenen zoals fluor, chloor of jodium. Berekeningen van elektronenverdeling ondersteunden het idee dat de meest actieve verbindingen de juiste balans van stabiliteit en reactiviteit hebben om geladen plaatsen in de enzymen aan te pakken. Het team onderzocht ook hoe één leidende verbinding, 4d, zich gedraagt in menselijke longkankercellen met behulp van fluorescentiemethoden. Het fluoresceert onder bepaald licht, en beeldvorming toonde dat het zich concentreert langs het celmembraan, juist de plaats van ectonucleotidase-enzymen, wat suggereert dat het zijn beoogde doelen in een realistische biologische omgeving kan bereiken.
Vroege stappen richting antikankergraad
Aangezien een bruikbaar geneesmiddel niet alleen zijn doelwit moet raken maar ook de groei van kankercellen moet beïnvloeden, evalueerden de onderzoekers hoe de nieuwe moleculen borstkankercellen in kweek beïnvloeden. Verschillende derivaten, met name 4j en 4k, verminderden de overleving van cellen en vertraagden de celdeling in de loop van de tijd, zij het niet zo sterk als een standaard chemotherapeuticum. Computationele controles van absorptie, distributie en basale geneesmiddelgelijkheid suggereerden dat de meeste verbindingen eigenschappen hebben die compatibel zijn met orale toediening en mogelijk de hersenen kunnen bereiken, wat de mogelijkheid opent voor toekomstige toepassingen bij moeilijk te behandelen tumoren.
Wat dit betekent voor toekomstige kankertherapieën
Al met al introduceert de studie een nieuwe familie van kinoline-gebaseerde moleculen die efficiënt enzymen blokkeren die immuunstimulerende signalen omzetten in immuunverzwakkend adenosine. Hoewel deze verbindingen zich nog in een vroeg stadium bevinden en slechts matige directe kankerdodende effecten laten zien, zijn ze veelbelovende instrumenten om de tumormicro-omgeving te hervormen zodat de eigen immuuncellen van het lichaam effectiever kunnen werken. Met verdere verfijning om potentie en selectiviteit te vergroten, zouden dergelijke ectonucleotidase-remmers op termijn bestaande immunotherapieën kunnen aanvullen en helpen de chemische ‘nevel’ op te tillen die tumoren voor aanval beschermt.
Bronvermelding: Ishaq, A., Nawaz, I., Qadir, J. et al. Quinoline carboxylic acid derivatives as potent ectonucleotidase inhibitors. Sci Rep 16, 10127 (2026). https://doi.org/10.1038/s41598-026-36994-1
Trefwoorden: kankerimmunotherapie, adenosinesignalering, enzymremmers, kinolineverbindingen, tumormicro-omgeving