Clear Sky Science · zh
用感应代谢物的受体对NK细胞和T细胞进行工程改造以靶向实体瘤
将肿瘤化学特征转化为导向信号
当今许多最有前景的癌症疗法依赖于激活免疫系统,然而实体瘤常常像设有城墙的要塞:本应摧毁它们的免疫细胞往往无法到达足够的数量。该研究探讨了一种新方法,将肿瘤自身的化学代谢产物转变为能够主动吸引杀伤性免疫细胞进入肿瘤的灯塔,从而有望使下一代细胞治疗在对抗乳腺癌和卵巢癌等难治性实体瘤时更为有效。
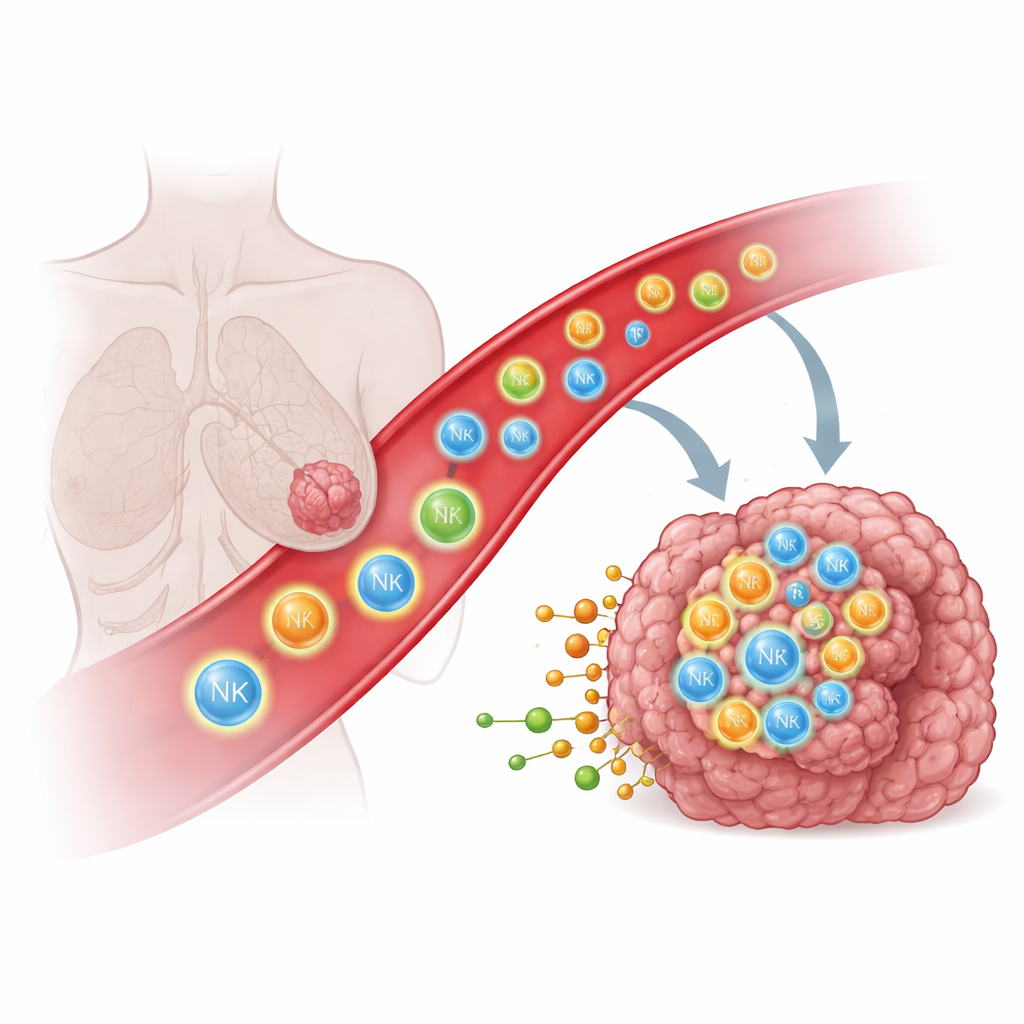
为何免疫细胞难以到达实体瘤
像自然杀伤(NK)细胞和T细胞这样的免疫细胞可以识别并清除癌细胞,但前提是它们能实际进入肿瘤。在许多患者体内,这些细胞要么根本到达不了肿瘤,要么被滞留在诸如肺等邻近组织中,从而限制了包括工程化CAR T和CAR NK细胞在内的强效疗法的作用。传统上,科学家尝试使用基于蛋白质的线索,如趋化因子和粘附分子,来引导免疫细胞,这些分子类似于分子路标。然而,即便具备这类知识,将免疫细胞深度导入实体瘤仍然异常困难,提示可能还有其他类型的信号在起作用。
发现对肿瘤代谢物的隐性“嗅觉受体”
为寻找新的引导系统,研究人员在NK细胞中进行了大规模基因筛选,开启数千个基因以观察哪些能帮助这些细胞迁移入小鼠的乳腺和卵巢肿瘤。他们反复发现一小类受体——属于G蛋白偶联受体(GPCR)家族——对蛋白质并不敏感,而是响应源自脂肪和胆固醇的小型生物活性分子。突出的受体GPR183及其若干同类通常仅出现在特定免疫细胞类型中。当这些受体被人工加入到NK或T细胞时,它们像新的“嗅觉受体”一样,感应癌细胞释放的代谢物并驱动工程化细胞朝肿瘤方向迁移。
肿瘤副产物如何形成化学踪迹
团队接着探究肿瘤具体产生了哪些物质会吸引携带GPR183的细胞。他们聚焦于氧化胆固醇(oxysterols)——胆固醇的氧化形式,由在侵袭性乳腺癌细胞中活跃的酶生成,尤其是在这些细胞暴露于炎性信号时。通过在癌细胞中敲除关键酶,研究人员表明,去除合成特定氧化胆固醇的能力会显著降低GPR183表达的NK细胞对肿瘤条件培养基的迁移。进一步实验显示,这些配体不仅创建了化学踪迹,还以配体依赖的方式重塑了NK细胞的基因活动,增强了与运动和膜组织相关的程序,同时下调了某些代谢通路。
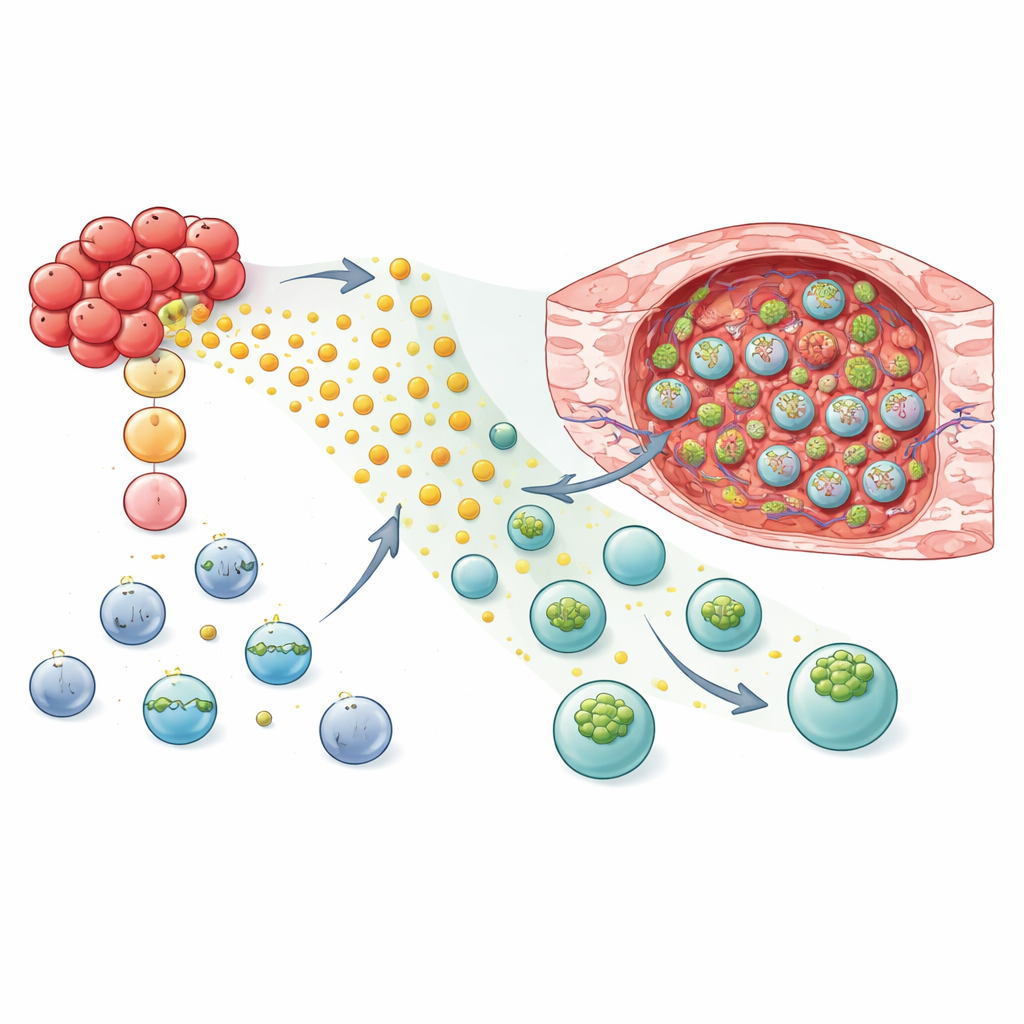
重新编程NK和T细胞以定位并攻击肿瘤
掌握了这一机制性见解后,研究人员测试了添加GPR183是否能使活体疗法成为更有效的肿瘤追踪者。在乳腺癌小鼠模型中,带有GPR183的NK-92细胞和来源于人体的原代NK细胞表现出强烈且优先的向肿瘤组织迁移,而非健康肺组织。当这些被编辑的NK细胞——或被设计为识别肿瘤表面标志的CAR NK细胞——被移植到小鼠体内时,肿瘤生长比接受普通细胞的动物更慢。这一策略对T细胞也同样有效:无论是常规的CD8 T细胞还是带GPR183的肿瘤靶向CAR T细胞,都在肿瘤内部的累积量更高,而在肺和脾中的分布相似。在免疫健全的小鼠模型中,携带小鼠版本GPR183的T细胞更有效地控制了乳腺肿瘤,并增加了完全清除肿瘤的动物比例。
这对未来癌症治疗可能意味着什么
对非专业读者来说,核心信息是作者找到了重接线免疫细胞的方法,使其追随肿瘤自身代谢发出的“嗅觉”信号。通过为NK和T细胞配备像GPR183这样的代谢物感应受体,他们将分散的免疫力量转变为在最需要处积聚的定向“搜寻者”。这项工作表明,与其与肿瘤化学环境对抗,不如劫持这种环境——利用癌细胞自然产生的分子作为工程细胞疗法的归巢线索。如果能安全地转化到临床,这种方法或能帮助克服治疗实体瘤的最大障碍之一:将足够多的强效免疫细胞在恰当时间输送到恰当位置。
引用: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
关键词: 免疫疗法, 细胞工程, 实体瘤, 趋化性, GPCRs