Clear Sky Science · nl
NK- en T-cellen ontwerpen met metaboliet‑gevoelige receptoren om vaste tumoren te richten
De tumorchemie als richtingssignaal
Veel van de meest veelbelovende kankerbehandelingen van vandaag zetten het immuunsysteem vrij, maar vaste tumoren gedragen zich vaak als ommuurde vestingen: de cellen die ze moeten vernietigen arriveren zelden in voldoende aantallen. Deze studie onderzoekt een nieuwe manier om de chemische bijproducten van de tumor zelf om te zetten in bakens die dodelijke immuuncellen actief naar binnen trekken, waardoor de volgende generatie celtherapieën mogelijk veel effectiever wordt tegen moeilijk te behandelen kankers zoals borst- en eierstokkanker.
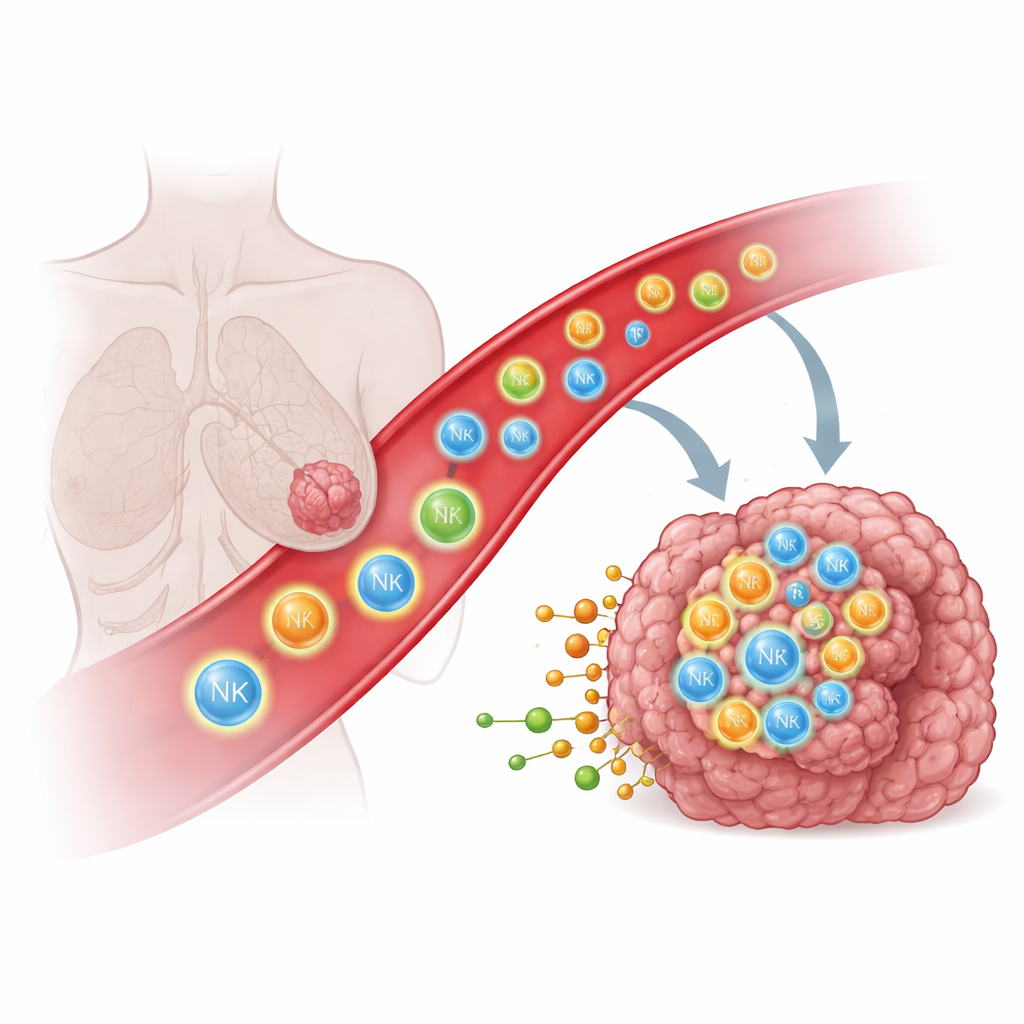
Waarom immuuncellen moeite hebben vaste tumoren te bereiken
Immuuncellen zoals natural killer (NK)-cellen en T-cellen kunnen kankercellen herkennen en vernietigen, maar alleen als ze de tumor fysiek binnenkomen. Bij veel patiënten bereiken deze cellen de tumor nooit of blijven ze vastzitten in nabijgelegen weefsels zoals de longen, wat de impact van krachtige therapieën, waaronder geengineerde CAR T- en CAR NK-cellen, beperkt. Traditioneel proberen wetenschappers immuuncellen te leiden met eiwitgebaseerde signalen, zoals chemokinen en adhesiemoleculen, die fungeren als moleculaire verkeersborden. Toch blijft het opmerkelijk moeilijk om immuuncellen diep in vaste tumoren te dirigeren, wat erop wijst dat ook andere soorten signalen een rol spelen.
Verborgen “neusreceptoren” voor tumormetabolieten ontdekken
Om nieuwe geleidingssystemen te vinden, gebruikten de onderzoekers grootschalige genetische screens in NK-cellen, waarbij duizenden genen werden aangezet om te zien welke hielpen bij migratie naar borst- en eierstokkanker in muismodellen. Ze vonden herhaaldelijk een kleine groep receptoren — leden van de familie van G-eiwitgekoppelde receptoren (GPCR) — die niet op eiwitten reageren maar op kleine, bioactieve moleculen afgeleid van vetten en cholesterol. De opvallende receptor, GPR183, samen met enkele verwanten, komt normaal gesproken alleen in geselecteerde immuunceltypen voor. Wanneer deze receptoren kunstmatig aan NK- of T-cellen werden toegevoegd, fungeerden ze als nieuwe “neusreceptoren” die metabolieten die door kankercellen worden vrijgegeven detecteerden en de geengineerde cellen richting de tumoren dreven.
Hoe tumorbijdproducten een chemisch spoor vormen
Het team onderzocht vervolgens precies wat de tumoren produceerden dat GPR183-uitgeruste cellen aantrok. Ze concentreerden zich op oxysterolen — geoxideerde vormen van cholesterol — gemaakt door enzymen die actief zijn in invasieve borstkankercellen, vooral wanneer die cellen worden blootgesteld aan ontstekingssignalen. Door sleutelenzymen in kankercellen uit te schakelen, toonden de onderzoekers aan dat het verwijderen van het vermogen om specifieke oxysterolen te maken de migratie van GPR183-expressieve NK-cellen naar tumor-geconditioneerd medium sterk verminderde. Aanvullende experimenten lieten zien dat deze liganden niet alleen een chemisch spoor creëerden, maar ook de genactiviteit van NK-cellen ligand-afhankelijk hervormden, waarbij programma’s gerelateerd aan beweging en membraanorganisatie werden versterkt en bepaalde metabole paden werden gedempt.
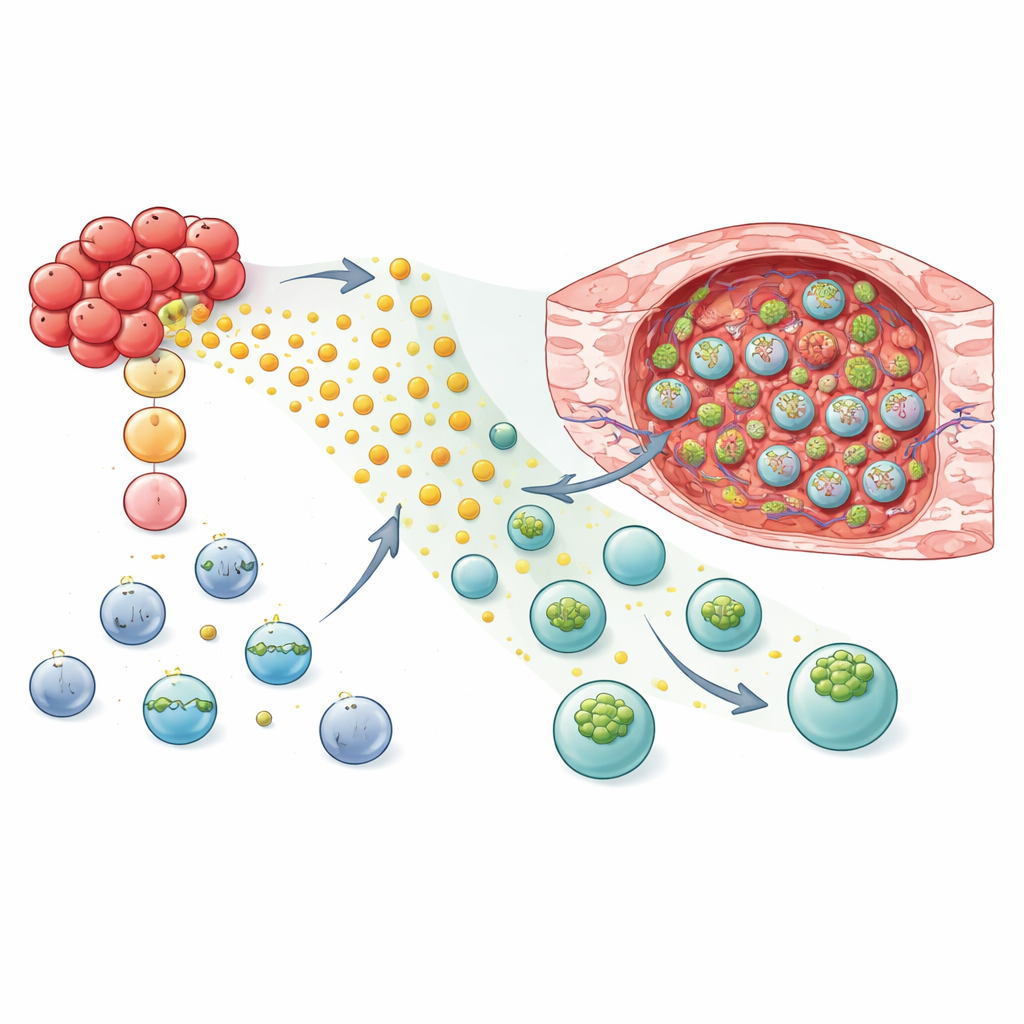
NK- en T-cellen herprogrammeren om gericht aan te vallen
Gewapend met dit mechanistische inzicht testten de onderzoekers of toevoeging van GPR183 levende therapieën betere tumorfinders kon maken. In muismodellen van borstkanker toonden NK-92-cellen en primaire menselijke NK-cellen die met GPR183 waren geengineerd sterke, preferentiële migratie naar tumorweefsel boven gezond longweefsel. Wanneer deze gewijzigde NK-cellen — of CAR NK-cellen die zijn ontworpen om een tumoroppervlakmarker te herkennen — in muizen werden overgedragen, groeiden tumoren trager dan bij dieren die standaardcellen ontvingen. De strategie werkte ook voor T-cellen: zowel conventionele CD8 T-cellen als tumorgerichte CAR T-cellen met GPR183 stapelden zich in hogere aantallen in tumoren op, terwijl ze vergelijkbaar bleven in long en milt. In een immunocompetent muismodel controleerden T-cellen met de muisvariant van GPR183 borstkankers effectiever en nam het aandeel dieren met volledige tumoruitroei toe.
Wat dit kan betekenen voor toekomstige kankerbehandelingen
Voor niet‑specialisten is de kernboodschap dat de auteurs een manier hebben gevonden om immuuncellen zo te herbedraden dat ze het chemische "geurspoor" van de tumormetabolisme volgen. Door NK- en T-cellen uit te rusten met metaboliet‑gevoelige receptoren zoals GPR183, veranderden ze verspreide immuunmacht in gerichte zoekers die zich ophopen waar ze het meest nodig zijn. Het werk suggereert dat we, in plaats van te vechten tegen tumorchemie, deze kunnen kapen — door de moleculen die kankercellen van nature produceren te gebruiken als richtsignalen voor geengineerde celtherapieën. Indien veilig naar de kliniek vertaald, zou deze benadering kunnen helpen een van de grootste obstakels bij de behandeling van vaste tumoren te overwinnen: het op het juiste moment op de juiste plaats krijgen van voldoende krachtige immuuncellen.
Bronvermelding: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
Trefwoorden: immunotherapie, celengineering, vaste tumoren, chemotaxis, GPCRs