Clear Sky Science · tr
Tümörleri Hedeflemek İçin Metabolit Algılayan Reseptörlerle NK ve T hücrelerini Mühendislik Etme
Tümör Kimyasını Bir Yön Bulma Sinyaline Dönüştürmek
Günümüzün en umut verici kanser tedavilerinin çoğu bağışıklık sistemini serbest bırakmaya dayanıyor; ancak solid tümörler sıklıkla surlarla çevrili kaleler gibi duruyor: onları yok etmesi gereken hücreler yeterli sayıda asla ulaşamıyor. Bu çalışma, tümörün kendi kimyasal yan ürünlerini, katil bağışıklık hücrelerini içeri doğru aktif şekilde çeken işaret fişeğine dönüştürmenin yeni bir yolunu araştırıyor; böylece meme ve over gibi zor tedavi edilen kanserlere karşı yeni nesil hücre tedavilerini çok daha etkili kılma potansiyeli doğuyor.
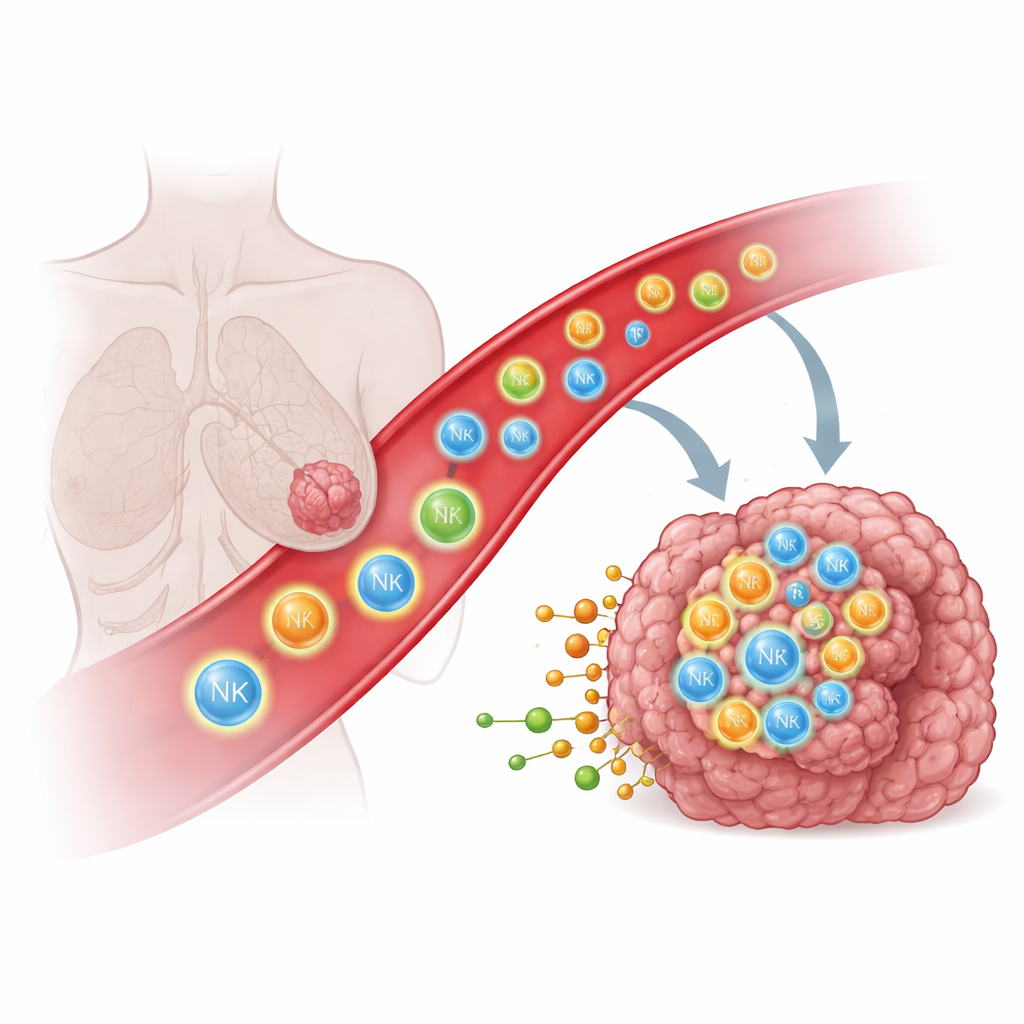
Bağışıklık Hücrelerinin Solid Tümörlere Ulaşmakta Neden Zorlandığı
Doğal öldürücü (NK) hücreler ve T hücreleri gibi bağışıklık hücreleri kanser hücrelerini tanıyıp yok edebilir, ancak bunun için fiziksel olarak tümörün içine girmeleri gerekir. Birçok hastada bu hücreler ya tümöre hiç ulaşmaz ya da akciğer gibi yakın dokularda takılıp kalır; bu da CAR T ve CAR NK hücreleri dahil güçlü tedavilerin etkisini sınırlar. Geleneksel olarak bilim insanları, moleküler sokak tabelaları gibi davranan kemokinler ve adezyon molekülleri gibi protein bazlı işaretlerle bağışıklık hücrelerini yönlendirmeye çalıştı. Yine de bu bilgilerle bile bağışıklık hücrelerini solid tümörlerin derinliklerine yönlendirmek şaşırtıcı derecede zor kaldı; bu da başka tür sinyallerin rol oynayabileceğini düşündürüyor.
Tümör Metabolitleri İçin Gizli “Koku Reseptörlerini” Keşfetmek
Yeni yönlendirme sistemlerini ortaya çıkarmak için araştırmacılar, binlerce geni açarak hangi genlerin NK hücrelerinin farelerde meme ve over tümörlerine göç etmesine yardımcı olduğunu görmek üzere geniş ölçekli genetik taramalar kullandılar. Tekrarlanan şekilde, proteinlere değil yağ ve kolesterolden türeyen küçük, biyoaktif moleküllere yanıt veren G-protein-eşlikli reseptör (GPCR) ailesinden küçük bir reseptör grubu bulundu. Öne çıkan reseptör GPR183 ve birkaç akrabası genelde yalnızca seçkin bağışıklık hücresi tiplerinde ortaya çıkar. Bu reseptörler yapay olarak NK veya T hücrelerine eklendiğinde, kanser hücreleri tarafından salınan metabolitleri algılayan yeni “koku reseptörleri” gibi davranarak tasarlanmış hücreleri tümörlere doğru sürükledi.
Tümör Yan Ürünleri Nasıl Kimyasal Bir İz Oluşturur
Araştırma ekibi sonra GPR183 donanımlı hücreleri çeken şeyin tam olarak tümörlerin ne ürettiğini sordu. İncelemelerini, özellikle inflamatuar sinyallere maruz kalan invaziv meme kanseri hücrelerinde aktif olan enzimlerin ürettiği oksisteroller—yani oksitlenmiş kolesterol formları—üzerine odakladılar. Kanser hücrelerindeki kritik enzimleri yok ederek, araştırmacılar belirli oksisterolleri yapma yeteneğini kaldırmanın GPR183 eksprese eden NK hücrelerinin tümör koşullandırılmış ortama göçünü keskin şekilde azalttığını gösterdiler. Ek deneyler bu ligandların yalnızca kimyasal bir iz oluşturmakla kalmadığını, aynı zamanda ligand-bağımlı olarak NK hücrelerinin gen aktivitesini yeniden şekillendirerek hareket ve zar organizasyonu ile ilişkili programları artırdığını ve bazı metabolik yolları azaltığını ortaya koydu.
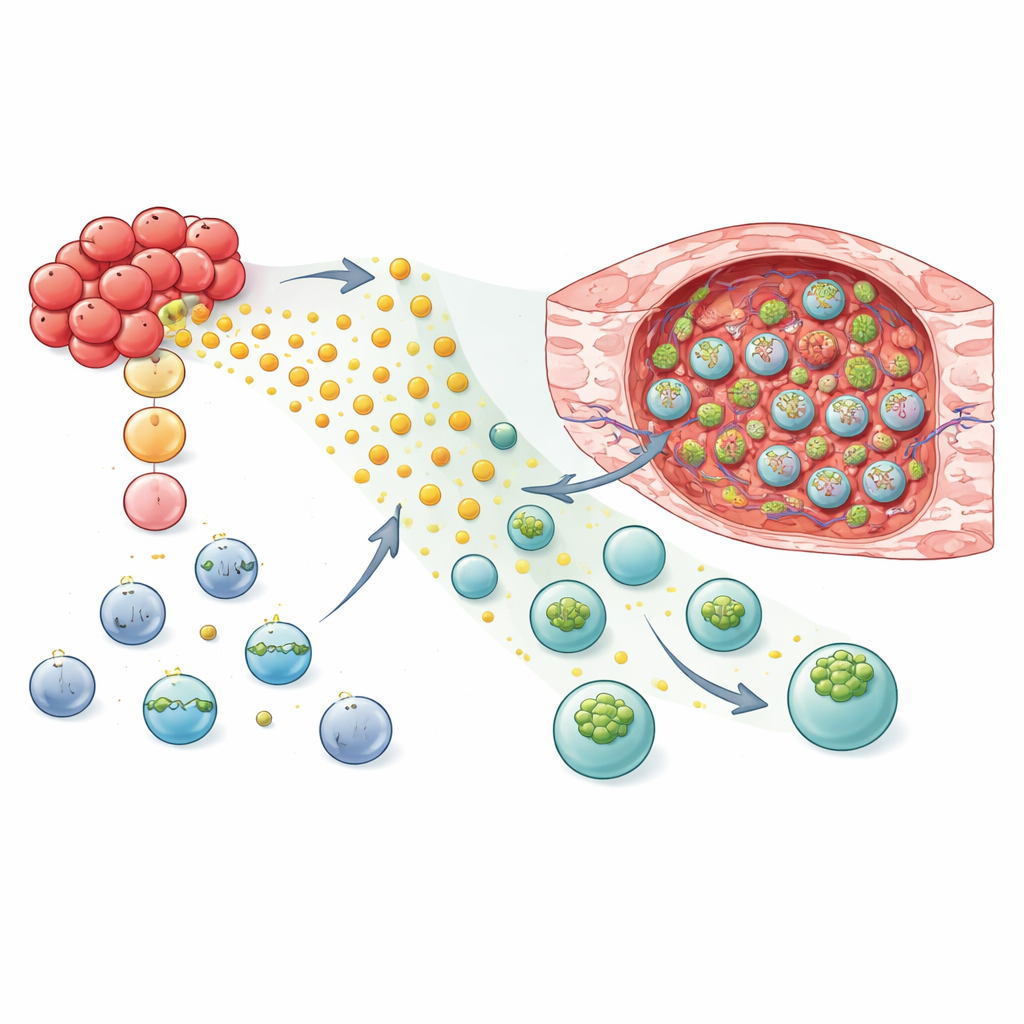
Homing Yeteneğini ve Saldırıyı Sağlamak İçin NK ve T Hücrelerini Yeniden Programlama
Bu mekanistik içgörüyle donanan araştırmacılar, GPR183 eklemenin canlı terapileri daha iyi tümör avcıları yapıp yapamayacağını test ettiler. Meme kanseri fare modellerinde GPR183 ile mühendislik edilmiş NK-92 hücreleri ve birincil insan NK hücreleri, sağlıklı akciğer dokusuna kıyasla tümör dokusuna güçlü ve tercihli bir göç gösterdi. Bu düzenlenmiş NK hücreleri—veya tümör yüzey belirteci tanımak üzere tasarlanmış CAR NK hücreleri—farelere aktarıldığında, tümörler standart hücreleri alan hayvanlara göre daha yavaş büyüdü. Bu strateji T hücreleri için de işe yaradı: hem konvansiyonel CD8 T hücreleri hem de tümör hedefli CAR T hücreleri GPR183 ile donatıldığında akciğer ve dalakla benzer seviyelerde kalırken tümör içinde daha yüksek düzeylerde birikim gösterdi. İmmün yetenekli bir fare modelinde, fare versiyonlu GPR183 taşıyan T hücreleri meme tümörlerini daha etkili kontrol etti ve tam tümör temizliği görülen hayvanların oranını artırdı.
Gelecekteki Kanser Tedavileri İçin Olası Anlamı
Bir uzman olmayan için temel mesaj, yazarların bağışıklık hücrelerini bir tümörün kendi metabolizmasının kimyasal “kokusunu” takip edecek şekilde yeniden kablolamanın bir yolunu bulduğudur. NK ve T hücrelerini GPR183 gibi metabolit algılayan reseptörlerle donatarak, dağınık bağışıklık güçlerini en çok ihtiyaç duyulan yerde biriken hedefe yönelik arayıcılara dönüştürdüler. Çalışma, tümör kimyasıyla savaşmak yerine onu kaçırabileceğimizi—kanser hücrelerinin doğal olarak ürettiği molekülleri mühendislik hücre terapileri için yön bulma işaretleri olarak kullanabileceğimizi öne sürüyor. Klinik uygulamaya güvenli bir şekilde çevrilirse, bu yaklaşım solid tümörleri tedavi etmede en büyük engellerden biri olan: yeterli sayıda güçlü bağışıklık hücresini doğru zamanda doğru yere ulaştırma sorununu aşmaya yardımcı olabilir.
Atıf: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
Anahtar kelimeler: immünoterapi, hücre mühendisliği, solid tümörler, kemotaksi, GPCRler