Clear Sky Science · pt
Engenharia de células NK e T com receptores sensíveis a metabólitos para direcionar tumores sólidos
Transformando a química tumoral em um sinal de orientação
Muitos dos tratamentos contra o câncer mais promissores hoje dependem de liberar o sistema imunológico, porém tumores sólidos frequentemente se comportam como fortalezas isoladas: as próprias células destinadas a destruí-los raramente chegam em números suficientes. Este estudo explora uma nova maneira de transformar os subprodutos químicos do tumor em faróis que atraem ativamente células imunes assassinas para o seu interior, potencialmente tornando as terapias celulares de próxima geração muito mais eficazes contra cânceres de difícil tratamento, como tumores de mama e ovário.
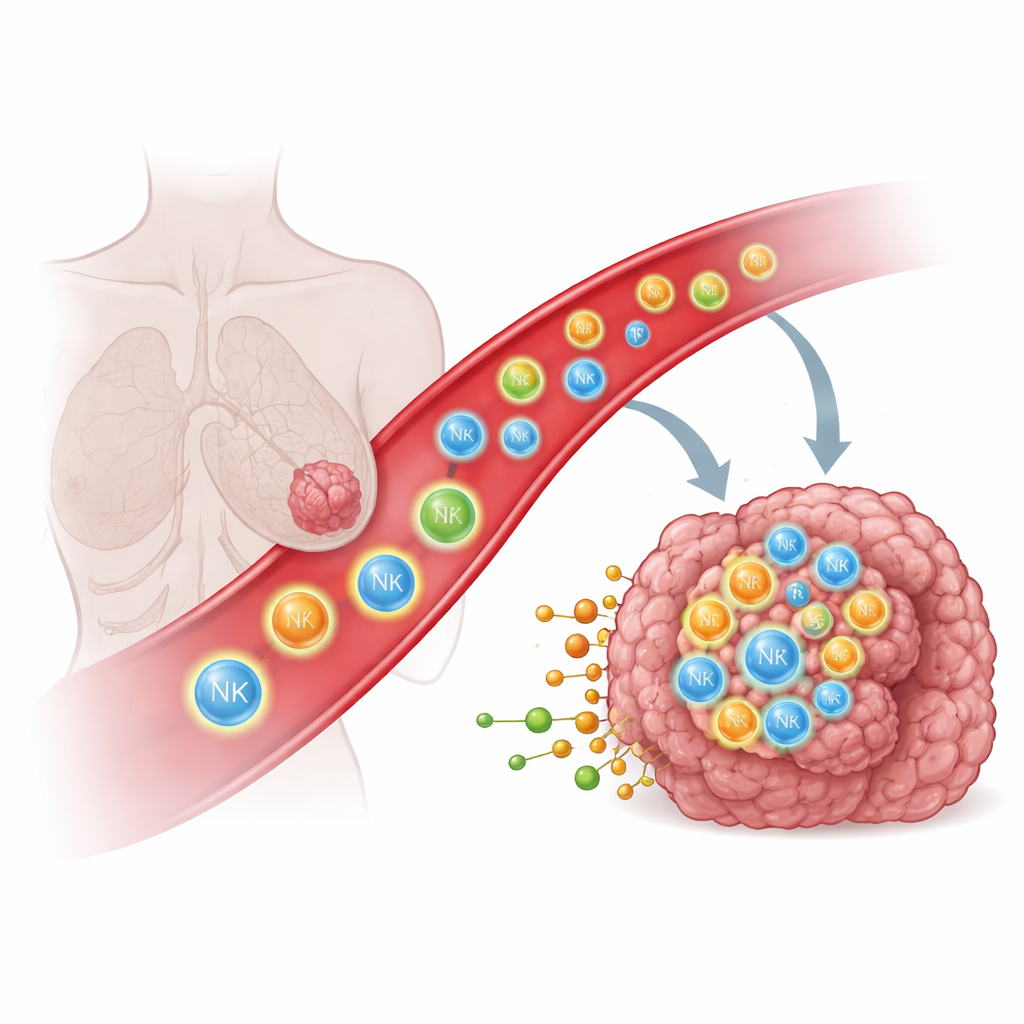
Por que as células imunes têm dificuldade em alcançar tumores sólidos
Células imunes como células natural killer (NK) e células T podem reconhecer e destruir células cancerosas, mas somente se elas entrarem fisicamente no tumor. Em muitos pacientes, essas células ou nunca alcançam o tumor ou ficam retidas em tecidos próximos, como os pulmões, limitando o impacto de terapias potentes, incluindo células CAR T e CAR NK modificadas. Tradicionalmente, os cientistas tentaram guiar células imunes usando sinais proteicos, como quimiocinas e moléculas de adesão, que atuam como placas de sinalização molecular. Ainda assim, mesmo com esse conhecimento, direcionar células imunes profundamente para tumores sólidos tem se mostrado surpreendentemente difícil, indicando que outros tipos de sinais podem estar em jogo.
Descobrindo “receptores olfativos” ocultos para metabólitos tumorais
Para revelar novos sistemas de orientação, os pesquisadores usaram triagens genéticas em larga escala em células NK, ativando milhares de genes para ver quais ajudavam essas células a migrar para tumores de mama e ovário em camundongos. Eles encontraram repetidamente um pequeno grupo de receptores — membros da família dos receptores acoplados à proteína G (GPCR) — que respondem não a proteínas, mas a pequenas moléculas bioativas derivadas de gorduras e colesterol. O receptor de destaque, chamado GPR183, junto com vários parentes, normalmente aparece apenas em tipos seletos de células imunes. Quando adicionados artificialmente a células NK ou T, esses receptores atuaram como novos “receptores olfativos” que sensorizavam metabólitos liberados por células cancerosas e direcionavam as células modificadas rumo aos tumores.
Como os subprodutos tumorais viram uma trilha química
Em seguida, a equipe investigou exatamente o que os tumores produziam que atraía células equipadas com GPR183. Eles se concentraram em oxisteróis — formas oxidadas do colesterol — produzidos por enzimas ativas em células de câncer de mama invasivo, especialmente quando essas células são expostas a sinais inflamatórios. Ao desligar enzimas-chave nas células cancerosas, os pesquisadores mostraram que remover a capacidade de fabricar oxisteróis específicos reduzia drasticamente a migração de células NK expressando GPR183 em direção ao meio condicionado por tumor. Experimentos adicionais revelaram que esses ligantes não apenas criavam uma trilha química, mas também remodelavam a atividade gênica das células NK de forma dependente do ligante, estimulando programas associados ao movimento e à organização da membrana enquanto rebaixavam certas vias metabólicas.
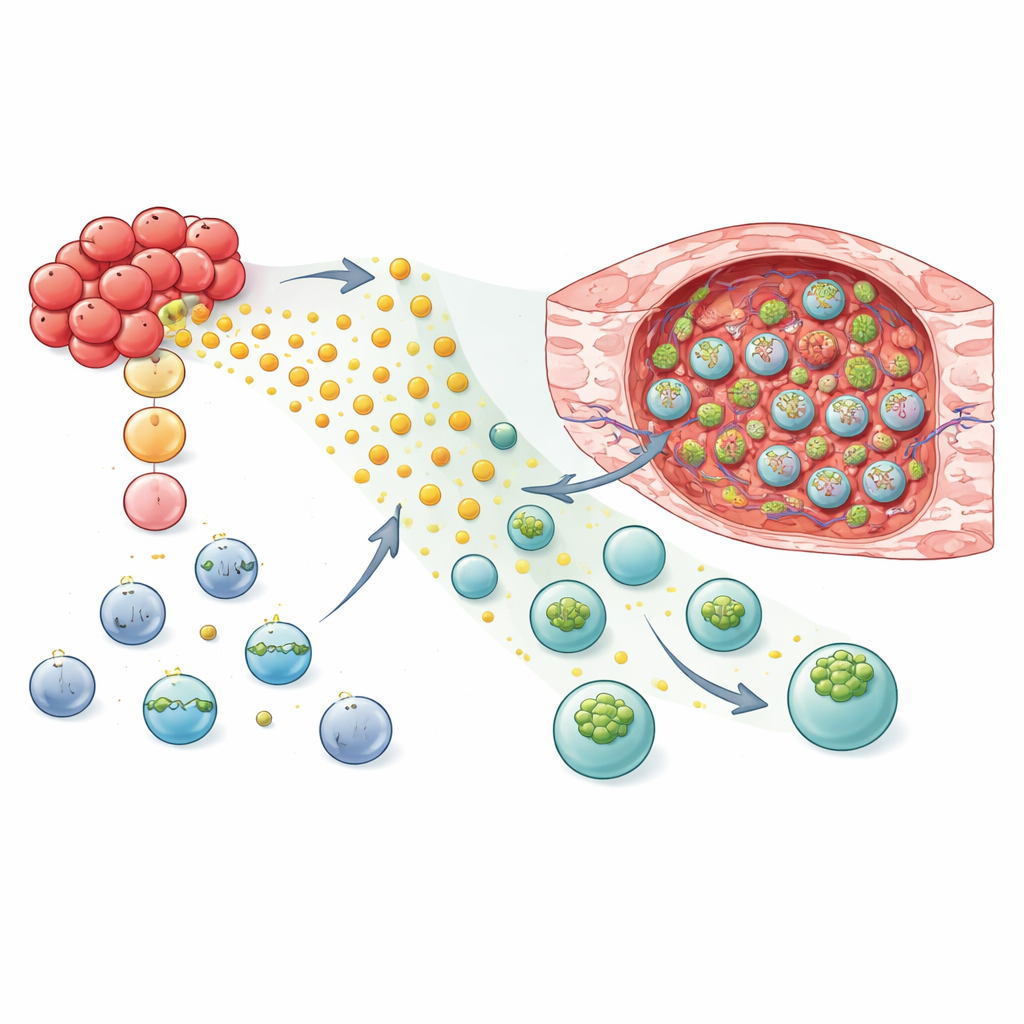
Reprogramando células NK e T para localizar e atacar
Munidos desse insight mecanístico, os pesquisadores testaram se adicionar GPR183 poderia tornar terapias vivas melhores caçadoras de tumor. Em modelos de camundongo de câncer de mama, células NK-92 e células NK humanas primárias modificadas com GPR183 mostraram forte migração preferencial para tecido tumoral em relação ao tecido pulmonar saudável. Quando essas células NK editadas — ou células CAR NK projetadas para reconhecer um marcador de superfície tumoral — foram transferidas para camundongos, os tumores cresceram mais lentamente do que em animais que receberam células padrão. A estratégia também funcionou para células T: tanto células T CD8 convencionais quanto células CAR T direcionadas a tumor com GPR183 se acumularam em níveis mais altos dentro dos tumores, permanecendo semelhantes no pulmão e no baço. Em um modelo de camundongo imunocompetente, células T portadoras da versão murina de GPR183 controlaram tumores de mama com mais eficácia e aumentaram a fração de animais com eliminação completa do tumor.
O que isso pode significar para tratamentos futuros do câncer
Para um não especialista, a mensagem central é que os autores descobriram uma maneira de reprogramar células imunes para que sigam o “cheiro” químico do próprio metabolismo do tumor. Ao equipar células NK e T com receptores sensíveis a metabólitos como GPR183, eles transformaram forças imunes dispersas em buscadores direcionados que se acumulam onde são mais necessários. O trabalho sugere que, em vez de combater a química tumoral, podemos usá-la a nosso favor — utilizando as moléculas que as células cancerosas produzem naturalmente como sinais de orientação para terapias celulares modificadas. Se traduzida de forma segura para a clínica, essa abordagem pode ajudar a superar um dos maiores obstáculos no tratamento de tumores sólidos: levar células imunes potentes em quantidade suficiente ao local certo e no momento certo.
Citação: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
Palavras-chave: imunoterapia, engenharia celular, tumores sólidos, quimiotaxia, GPCRs