Clear Sky Science · pl
Inżynieria komórek NK i T z receptorami wyczuwającymi metabolity w celu celowania w guzy lity
Przekształcanie chemii guza w sygnał przyciągający
Wiele z najbardziej obiecujących obecnie terapii przeciwnowotworowych opiera się na uwolnieniu układu odpornościowego, jednak guzy lite często funkcjonują jak oblężone twierdze: komórki, które mają je zniszczyć, nie docierają tam w wystarczającej liczbie. W badaniu tym zbadano nowe podejście polegające na przekształceniu chemicznych produktów ubocznych guza w sygnały, które aktywnie ściągają zabójcze komórki odpornościowe do wnętrza guza, co może sprawić, że nowej generacji terapie komórkowe będą znacznie skuteczniejsze wobec trudno leczonych nowotworów, takich jak rak piersi i jajnika.
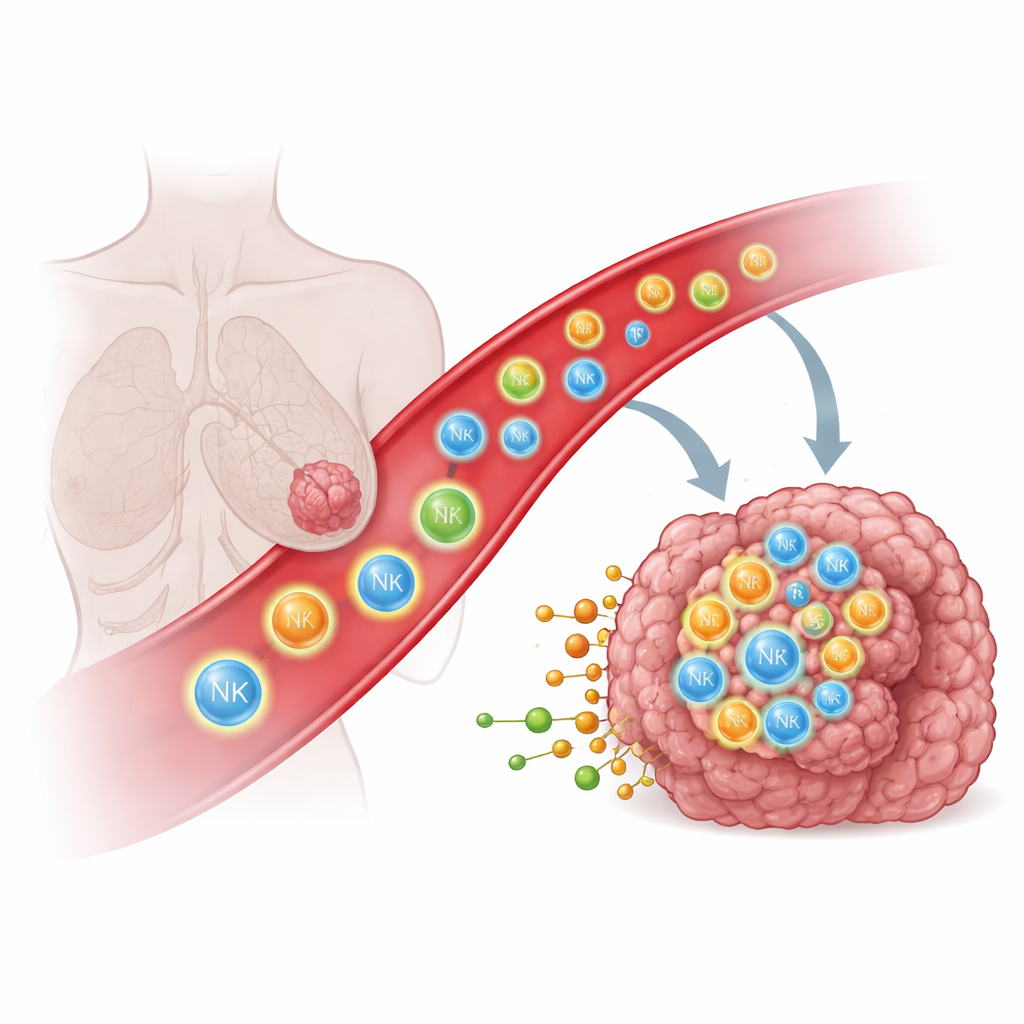
Dlaczego komórkom odpornościowym trudno dotrzeć do guzów litych
Komórki odpornościowe, takie jak naturalne komórki zabójcze (NK) i limfocyty T, potrafią rozpoznawać i niszczyć komórki nowotworowe, ale tylko wtedy, gdy fizycznie wkroczą do guza. U wielu pacjentów komórki te albo w ogóle nie docierają do guza, albo zatrzymują się w pobliskich tkankach, np. w płucach, co ogranicza skuteczność potężnych terapii, w tym inżynierowanych komórek CAR T i CAR NK. Tradycyjnie naukowcy próbowali kierować komórkami odpornościowymi za pomocą białkowych sygnałów, takich jak chemokiny i cząsteczki adhezyjne, działających jak molekularne znaki drogowe. Nawet przy tej wiedzy, skierowanie komórek odpornościowych głęboko do guzów litych pozostaje zaskakująco trudne, co sugeruje, że mogą działać inne rodzaje sygnałów.
Odkrycie ukrytych „receptorów węchowych” na metabolity guza
Aby ujawnić nowe systemy nawigacji, badacze zastosowali szeroko zakrojone przesiewy genetyczne w komórkach NK, aktywując tysiące genów, by zobaczyć, które z nich ułatwiają migrację tych komórek do guzów piersi i jajnika u myszy. W powtarzalny sposób odkrywali niewielką grupę receptorów — członków rodziny receptorów sprzężonych z białkiem G (GPCR) — które reagują nie na białka, lecz na małe bioaktywne cząsteczki pochodzące z lipidów i cholesterolu. Receptorem wyróżniającym się był GPR183, wraz z kilkoma pokrewnymi, które zwykle występują tylko w wybranych typach komórek odpornościowych. Po sztucznym dodaniu tych receptorów do komórek NK lub T, działały one jak nowe „receptory węchowe”, wykrywając metabolity uwalniane przez komórki nowotworowe i kierując zmodyfikowane komórki w stronę guza.
Jak produkty uboczne guza stają się chemicznym tropem
Zespół zapytał potem, co dokładnie guzy wytwarzają, że przyciąga komórki z GPR183. Skoncentrowali się na oksysterolach — zoxidowanych formach cholesterolu — wytwarzanych przez enzymy aktywne w inwazyjnych komórkach raka piersi, zwłaszcza gdy komórki te są wystawione na sygnały zapalne. Poprzez wyeliminowanie kluczowych enzymów w komórkach nowotworowych badacze wykazali, że utrata zdolności do wytwarzania konkretnych oksysteroli wyraźnie zmniejszała migrację komórek NK ekspresujących GPR183 w kierunku pożywki warunkowanej przez guz. Dodatkowe eksperymenty wykazały, że te ligandy nie tylko tworzyły chemiczny trop, ale także przekształcały aktywność genów w komórkach NK w sposób zależny od liganda, wzmacniając programy związane z ruchem i organizacją błony, jednocześnie osłabiając określone szlaki metaboliczne.
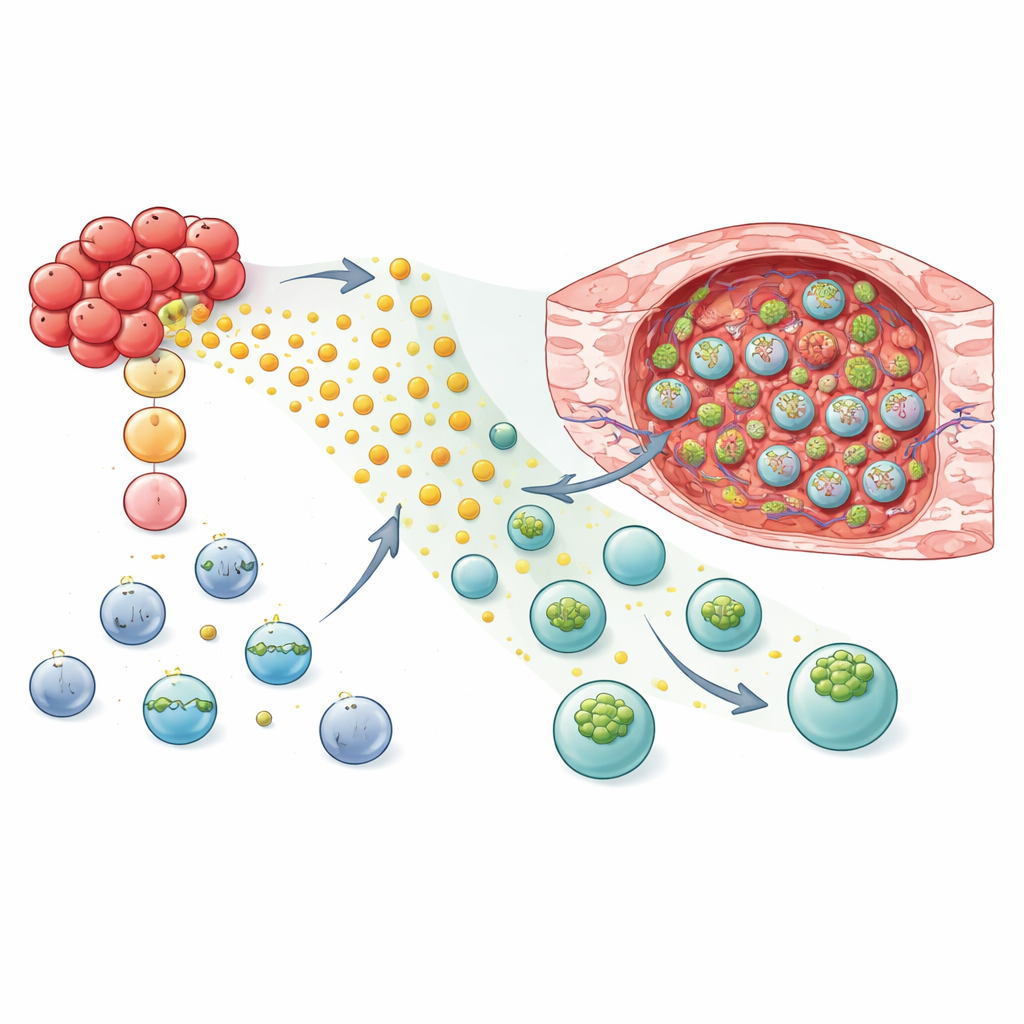
Przeprogramowanie komórek NK i T, by trafiały do celu i atakowały
Wyposażeni w to mechanistyczne zrozumienie, badacze sprawdzili, czy dodanie GPR183 może uczynić terapie komórkowe lepszymi łowcami guzów. W modelach mysich raka piersi komórki NK-92 oraz pierwotne ludzkie komórki NK zaprojektowane z GPR183 wykazywały silną, preferencyjną migrację do tkanek guza w porównaniu z zdrową tkanką płucną. Gdy te zmodyfikowane komórki NK — lub komórki CAR NK zaprojektowane do rozpoznawania markera powierzchni guza — zostały przeszczepione do myszy, guzy rosły wolniej niż u zwierząt otrzymujących standardowe komórki. Strategia zadziałała również dla limfocytów T: zarówno konwencjonalne komórki CD8, jak i terapeutyczne komórki CAR T z GPR183 gromadziły się w większej liczbie wewnątrz guzów, pozostając przy tym na podobnym poziomie w płucach i śledzionie. W immunokompetentnym modelu myszy, komórki T niosące mysie wydanie GPR183 skuteczniej kontrolowały guzy piersi i zwiększały odsetek zwierząt z całkowitym wyleczeniem guza.
Co to może oznaczać dla przyszłych terapii przeciwnowotworowych
Dla osoby nietechnicznej główny wniosek jest taki, że autorzy odkryli sposób na przekaźnikowanie komórek odpornościowych, by podążały za chemicznym „zapachem” metabolizmu guza. Wyposażając komórki NK i T w receptory wyczuwające metabolity, takie jak GPR183, przekształcili rozproszone siły odpornościowe w celowane poszukiwacze, które gromadzą się tam, gdzie są najbardziej potrzebne. Praca sugeruje, że zamiast walczyć z chemią guza, możemy ją wykorzystać — używając cząsteczek naturalnie produkowanych przez komórki nowotworowe jako sygnałów przyciągających dla inżynierowanych terapii komórkowych. Jeśli podejście to zostanie bezpiecznie przetłumaczone na warunki kliniczne, może pomóc przezwyciężyć jedną z największych przeszkód w leczeniu guzów litych: dostarczenie wystarczającej liczby silnych komórek odpornościowych we właściwe miejsce i we właściwym czasie.
Cytowanie: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
Słowa kluczowe: immunoterapia, inżynieria komórek, guzy lite, chemotaksja, GPCRy