Clear Sky Science · ar
هندسة خلايا NK وT بمستقبلات حسّاسة للتمثيل الغذائي لاستهداف الأورام الصلبة
تحويل كيمياء الورم إلى إشارة جذب
تعتمد العديد من علاجات السرطان الواعدة اليوم على تحرير الجهاز المناعي، ومع ذلك غالبًا ما تظل الأورام الصلبة محصنة كالحصون: الخلايا المخصصة لتدميرها لا تصل بأعداد كافية. تستكشف هذه الدراسة نهجًا جديدًا لتحويل نواتج التمثيل الكيميائي للورم إلى منارات تسحب خلايا القتل المناعية إلى الداخل بنشاط، مما قد يجعل علاجات الخلايا من الجيل التالي أكثر فعالية ضد سرطانات يصعب معالجتها مثل سرطانات الثدي والمبيض.
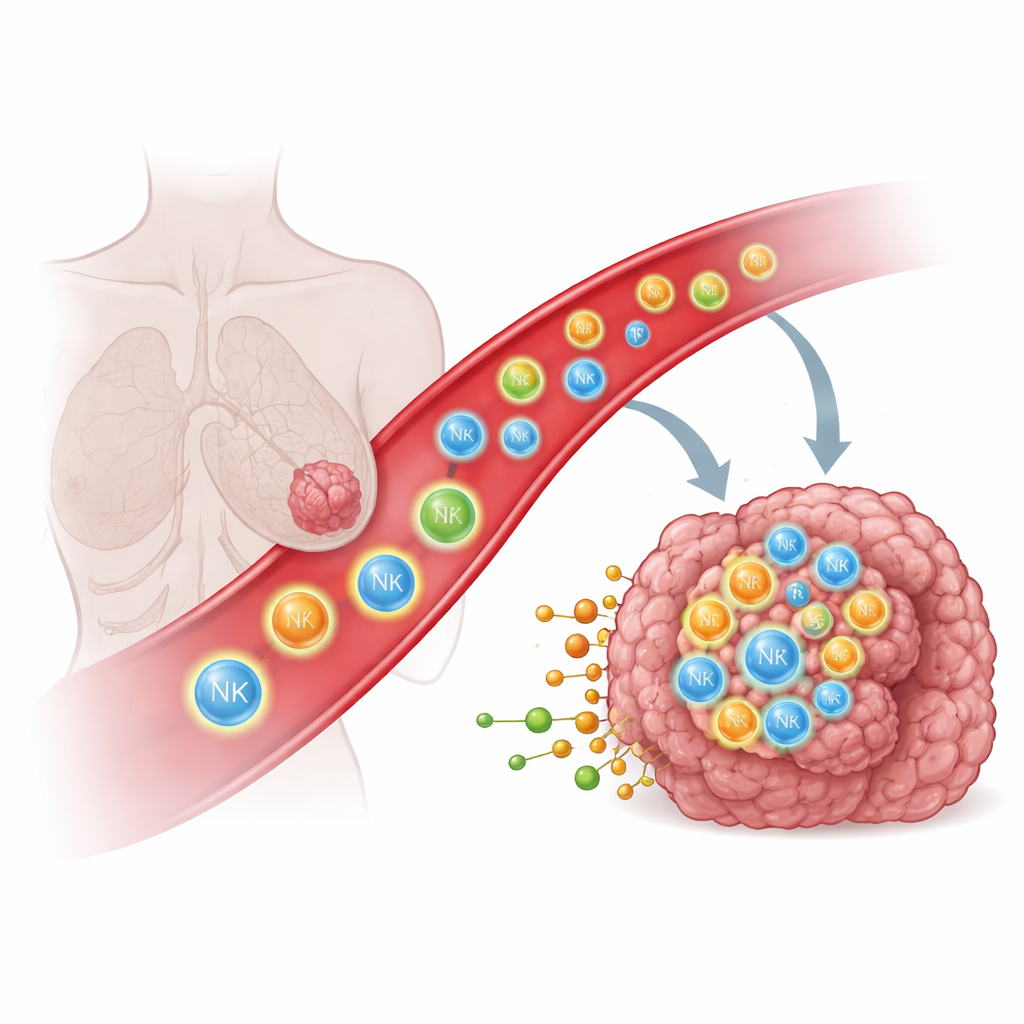
لماذا تكافح الخلايا المناعية للوصول إلى الأورام الصلبة
يمكن للخلايا المناعية مثل خلايا القاتل الطبيعي (NK) وخلايا T التعرف على الخلايا السرطانية وتدميرها، لكن ذلك يتطلب دخولها الفيزيائي إلى الورم. في كثير من المرضى، إما أن هذه الخلايا لا تصل إلى الورم أبدًا أو تتوقف في أنسجة مجاورة مثل الرئتين، مما يقلص فعالية العلاجات القوية، بما في ذلك خلايا CAR T وCAR NK المهندَسة. تقليديًا، حاول العلماء توجيه الخلايا المناعية باستخدام إشارات بروتينية مثل الكيموكينات وجزيئات الالتصاق التي تعمل كلوحات إرشادية جزيئية. ومع ذلك، حتى مع هذه المعرفة، ظل توجيه الخلايا المناعية إلى أعماق الأورام الصلبة أمرًا صعبًا بشكل مدهش، مما يشير إلى أن إشارات أخرى قد تكون ذات دور.
اكتشاف "مستقبلات شمية" خفيّة لمستقلبات الورم
لكشف أنظمة توجيه جديدة، استخدم الباحثون شاشات جينية واسعة النطاق في خلايا NK، وقاموا بتشغيل آلاف الجينات لمعرفة أيها يساعد هذه الخلايا على الهجرة نحو أورام الثدي والمبيض في الفئران. وجدوا مرارًا مجموعة صغيرة من المستقبلات—أعضاء من عائلة مستقبلات المرتبطة بالبروتين G (GPCR)—التي تستجيب ليس للبروتينات بل لجزيئات صغيرة حيوية المصدر مشتقة من الدهون والكوليسترول. كان المستقبل البارز، المسمى GPR183، إلى جانب عدة مستقبلات قريبة، يظهر عادةً فقط في أنواع مناعية محددة. عندما أُضيفت هذه المستقبلات صناعيًا إلى خلايا NK أو T، عملت كـ"مستقبلات شمية" جديدة استشعرت المستقلبات التي تفرزها الخلايا السرطانية ودفعت الخلايا المهندَسة نحو الأورام.
كيف تصبح نواتج الورم طريقًا كيميائيًا
سأل الفريق بعد ذلك عما تنتجه الأورام بالضبط لجذب الخلايا المزوَّدة بـGPR183. ركزوا على الأوكسيستيرولات—أشكال مؤكسدة من الكوليسترول—التي تصنعها إنزيمات نشطة في خلايا سرطان الثدي الغازية، خاصة عند تعرض هذه الخلايا لإشارات التهابية. من خلال تعطيل إنزيمات رئيسية في الخلايا السرطانية، أظهر الباحثون أن إزالة القدرة على صنع أوكسيستيرولات محددة قلصت بشدة هجرة خلايا NK المعبرة عن GPR183 نحو وسط مشروط بالورم. وكشفت تجارب إضافية أن هذه الليجاندات لم تخلق مجرد أثر كيميائي فحسب، بل أعادت أيضًا تشكيل نشاط الجينات في خلايا NK بطريقة تعتمد على الليجاند، مع تعزيز برامج مرتبطة بالحركة وتنظيم الغشاء بينما خفّضت بعض المسارات الأيضية.
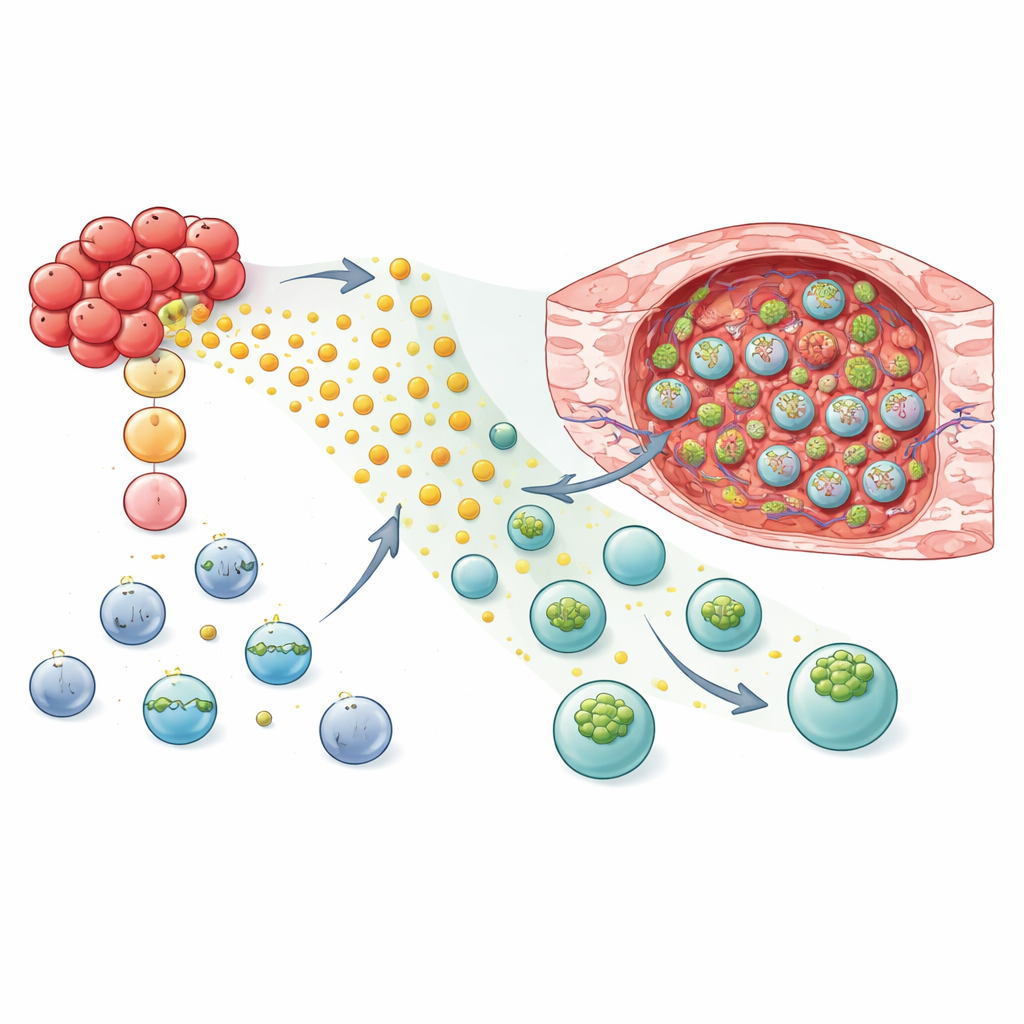
إعادة برمجة خلايا NK وT للتوّجه والهجوم
مسلحين بهذا الفهم الآلي، اختبر الباحثون ما إذا كان إضافة GPR183 يمكن أن يجعل العلاجات الحية صيادين أفضل للأورام. في نماذج فئران سرطان الثدي، أظهرت خلايا NK-92 وخلايا NK البشرية الأولية المهندَسة بـGPR183 هجرة قوية وتفضيلية إلى نسيج الورم مقارنة بنسيج الرئة الصحي. عندما نُقلت هذه الخلايا المعدلة—أو خلايا CAR NK المصممة للتعرف على علامة سطحية للورم—إلى الفئران، نما الورم ببطء أكبر مما في الحيوانات التي تلقت خلايا قياسية. نجح الاستراتيجية أيضًا مع خلايا T: تراكمت كل من خلايا CD8 التقليدية وخلايا CAR T الموجهة للورم والمعبرة عن GPR183 بمستويات أعلى داخل الأورام مع بقاء تواجدها في الرئة والطحال مماثلًا. في نموذج فأر بمناعة سليمة، سيطرت خلايا T الحاملة للنسخة الفأرية من GPR183 على أورام الثدي بشكل أكثر فعالية وزاد احتمال التخلص التام من الورم في حصة أكبر من الحيوانات.
ما الذي قد يعنيه هذا لعلاجات السرطان المستقبلية
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن المؤلفين وجدوا طريقة لإعادة توصيل الخلايا المناعية بحيث تتبع الـ"رائحة" الكيميائية لتمثيل الورم الخاص به. من خلال تزويد خلايا NK وT بمستقبلات حسّاسة للمستقلبات مثل GPR183، حوّلوا قوى مناعية مبعثرة إلى منصات استهداف تتجمع حيث تكون الأكثر حاجة. تشير الدراسة إلى أنه بدلًا من محاربة كيمياء الورم، يمكننا اختطافها—باستخدام الجزيئات التي تنتجها الخلايا السرطانية طبيعيًا كإشارات توجيه للعلاجات الخلوية المهندَسة. إذا تُرجمت هذه الفكرة بأمان إلى العيادات، فقد تساعد في التغلب على أحد أكبر العقبات في علاج الأورام الصلبة: إدخال عدد كافٍ من الخلايا المناعية الفعالة إلى المكان المناسب في الوقت المناسب.
الاستشهاد: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
الكلمات المفتاحية: العلاج المناعي, هندسة الخلايا, الأورام الصلبة, الاستِقْصال الكيميائي (كيموتاكْسِي), مستقبلات GPCR