Clear Sky Science · ja
代謝物感知受容体でNK細胞とT細胞を工学的改変して固形腫瘍を標的化する
腫瘍の化学性をホーミング信号に変える
現代で最も有望とされるがん治療法の多くは免疫系を解き放つことに依存していますが、固形腫瘍はしばしば城壁で囲まれた要塞のように存在し、腫瘍を破壊すべき細胞が十分な数で到達しません。本研究は、腫瘍自身の化学的副産物をキラー免疫細胞を引き寄せるビーコンに変える新しい方法を探り、乳がんや卵巣がんのような治療が難しい固形腫瘍に対する次世代の細胞療法をはるかに効果的にする可能性を示しています。
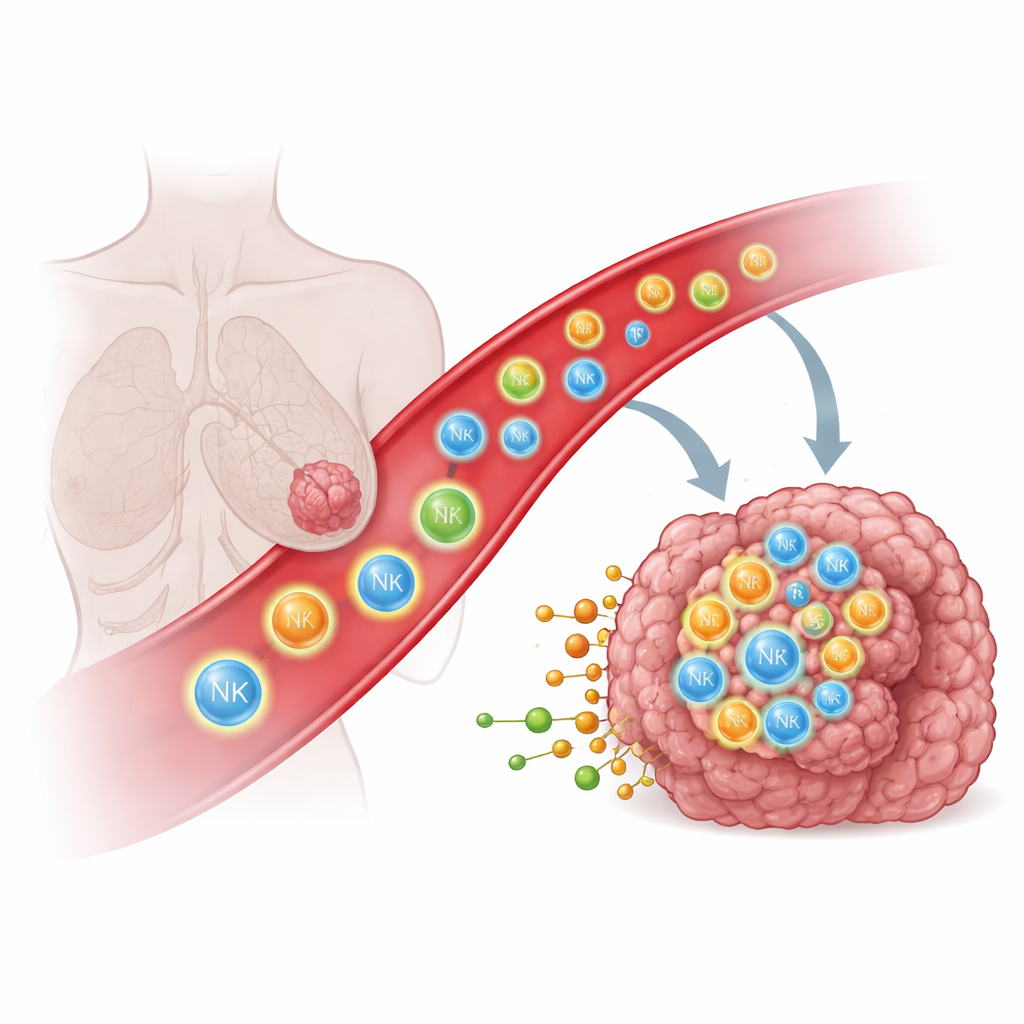
免疫細胞が固形腫瘍に到達しにくい理由
ナチュラルキラー(NK)細胞やT細胞のような免疫細胞はがん細胞を認識して破壊できますが、それは物理的に腫瘍内へ侵入した場合に限られます。多くの患者では、これらの細胞は腫瘍に到達しないか、肺のような近傍組織にとどまってしまい、CAR TやCAR NK細胞を含む強力な療法の効果を制限します。従来、研究者はケモカインや接着分子のようなタンパク質ベースの手がかりを分子の案内標識として免疫細胞を誘導しようとしました。しかしそれでも固形腫瘍の深部へ免疫細胞を導くのは驚くほど難しく、別種のシグナルが作用している可能性を示唆しています。
腫瘍代謝物の“におい受容体”を発見する
新たな誘導システムを明らかにするため、研究者らはNK細胞で大規模な遺伝学的スクリーニングを行い、何千もの遺伝子をオンにしてどれが乳がんや卵巣がんの腫瘍へこの細胞の移動を助けるかを調べました。繰り返し見つかったのは、タンパク質ではなく脂質やコレステロール由来の小さな生理活性分子に応答するGタンパク質共役受容体(GPCR)ファミリーの少数の受容体群でした。中でもGPR183と呼ばれる受容体が際立ち、いくつかの関連受容体とともに通常は限られた免疫細胞型にのみ発現します。これらを人工的にNKやT細胞に導入すると、がん細胞が放出する代謝物を感知して腫瘍に向かわせる新たな“におい受容体”として機能しました。
腫瘍の副産物が化学的な道しるべになる仕組み
研究チームは次に、GPR183装備細胞を引き寄せる腫瘍産物が何であるかを特定しました。注目したのはオキシステロール—コレステロールの酸化型—で、侵襲的な乳がん細胞で活性化される酵素によって作られ、とくに炎症シグナルにさらされたときに増加します。がん細胞側の主要な酵素をノックアウトすると、特定のオキシステロールを生成する能力を失わせた場合に、GPR183発現NK細胞の腫瘍条件培地への走化が著しく減少することを示しました。追加実験では、これらのリガンドが単に化学的な道筋を作るだけでなく、リガンド依存的にNK細胞の遺伝子発現を再構築し、運動と膜の組織化に関連するプログラムを強化し、特定の代謝経路を抑えることも明らかになりました。
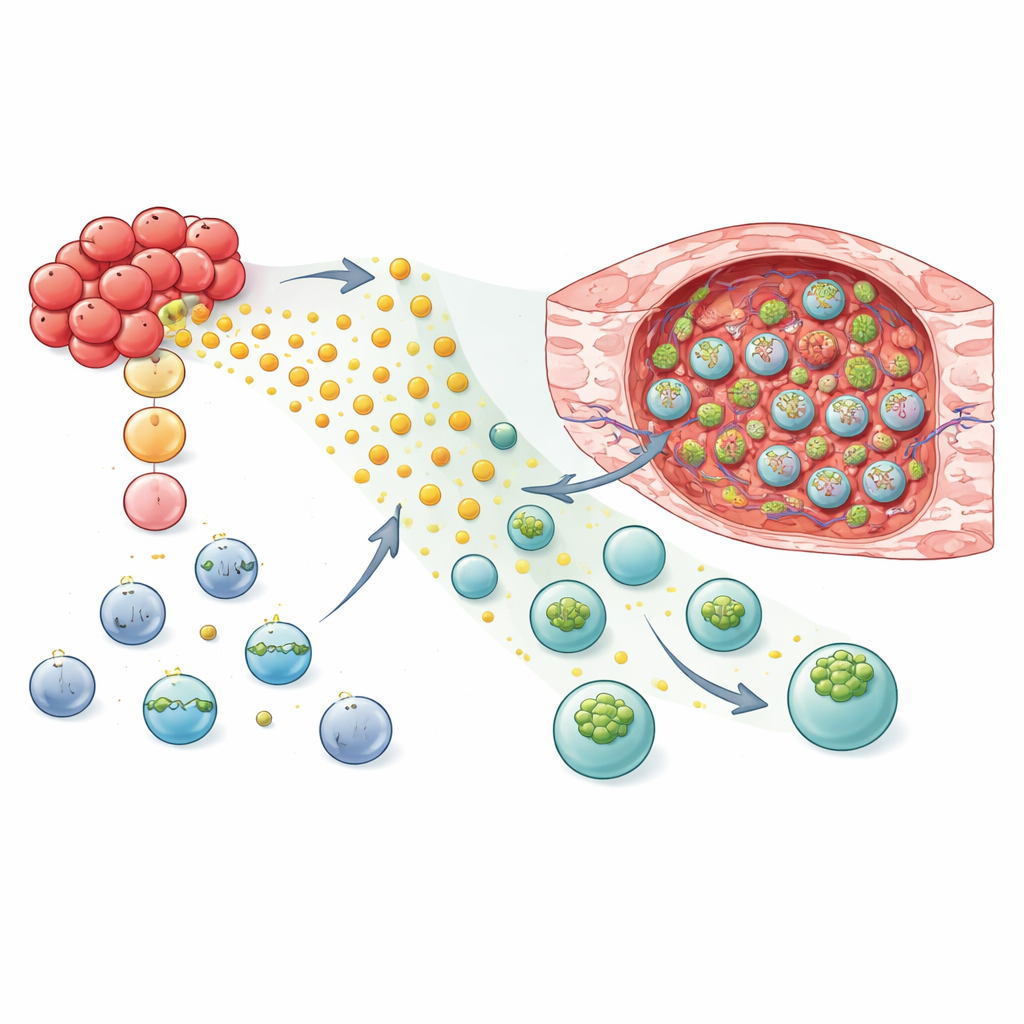
NK細胞とT細胞を再プログラムしてホーミングさせ攻撃させる
この機構的知見を踏まえ、研究者らはGPR183を付加することで生体治療が腫瘍探索能を高めるかを検証しました。乳がんのマウスモデルでは、GPR183で改変したNK-92細胞とヒト一次NK細胞が健康な肺組織よりも腫瘍組織へ強く選択的に移動しました。これらの改変NK細胞、あるいは腫瘍表面マーカーを認識するよう設計したCAR NK細胞をマウスに移入すると、標準の細胞を投与した動物に比べ腫瘍の成長が遅くなりました。この戦略はT細胞でも有効で、従来のCD8 T細胞および腫瘍標的化CAR T細胞の両方でGPR183を持たせると腫瘍内での蓄積が増え、肺や脾臓では同様のレベルにとどまりました。免疫応答可能なマウスモデルでは、マウス版GPR183を持つT細胞が乳腺腫瘍をより効果的に制御し、完全消失に至る動物の割合を高めました。
今後のがん治療にとっての意義
専門外の方に向けた要点は、著者らが免疫細胞を腫瘍代謝が放つ化学的“におい”を追うように再配線する方法を見出したことです。GPR183のような代謝物感知受容体でNK細胞やT細胞を武装させることで、散在する免疫力を必要な場所に蓄積する標的性の高い探索者へと変えました。この研究は、腫瘍の化学性と戦うのではなくそれをハイジャックし、がん細胞が自然に生産する分子を工学的細胞療法のホーミング手がかりとして利用できることを示唆します。臨床へ安全に展開できれば、このアプローチは固形腫瘍治療における最大の障壁の一つ、すなわち十分な数の強力な免疫細胞を適切な場所へ適切な時に届けるという問題の克服に役立つ可能性があります。
引用: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
キーワード: 免疫療法, 細胞工学, 固形腫瘍, 走化性, GPCR