Clear Sky Science · fr
Ingénierie des cellules NK et T avec des récepteurs détectant les métabolites pour cibler les tumeurs solides
Transformer la chimie tumorale en signal de repérage
Beaucoup des traitements anticancéreux les plus prometteurs d’aujourd’hui reposent sur la mobilisation du système immunitaire, mais les tumeurs solides font souvent office de forteresses : les cellules chargées de les détruire n’y parviennent jamais en nombre suffisant. Cette étude explore une nouvelle manière de convertir les sous-produits chimiques du tumor en balises qui attirent activement les cellules immunitaires tueuses, ce qui pourrait rendre les thérapies cellulaires de nouvelle génération beaucoup plus efficaces contre des cancers difficiles à traiter, comme les tumeurs mammaires et ovariennes.
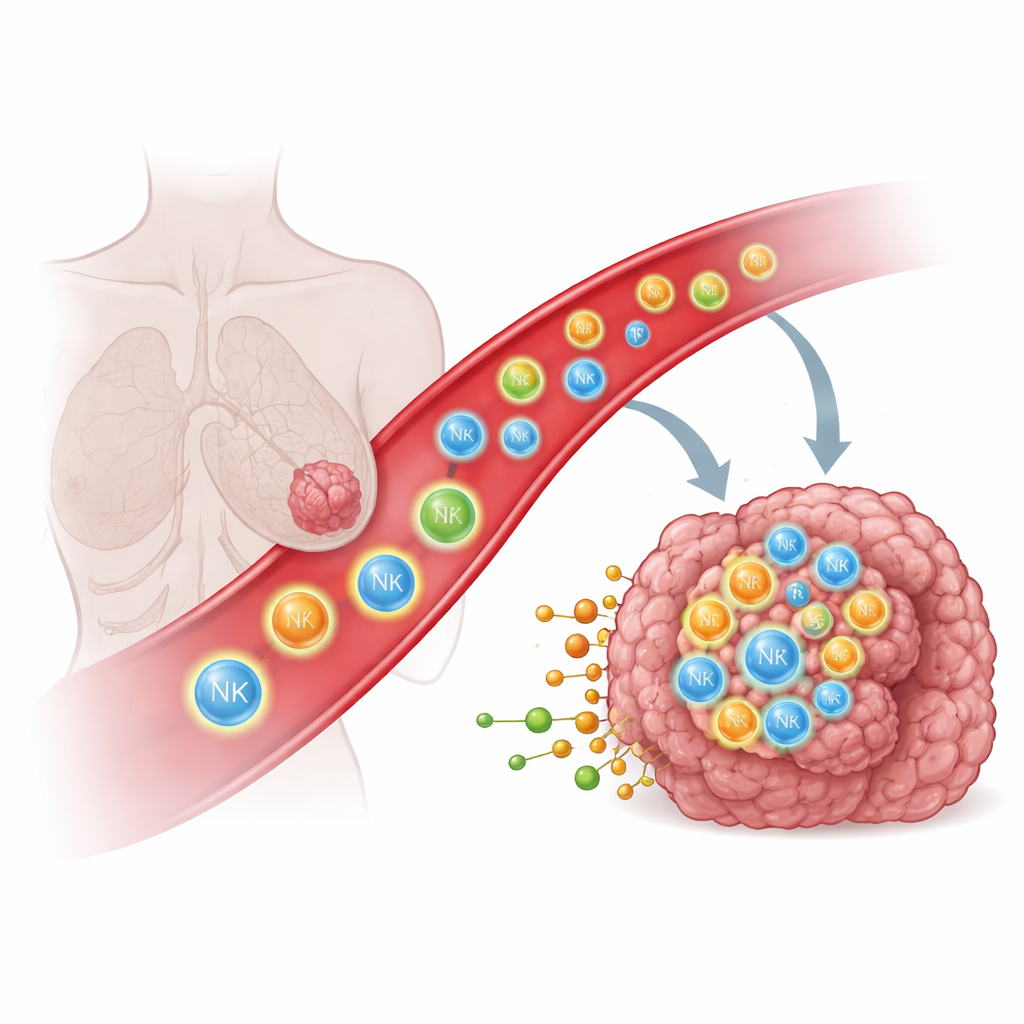
Pourquoi les cellules immunitaires peinent à atteindre les tumeurs solides
Les cellules immunitaires telles que les cellules NK (natural killer) et les lymphocytes T peuvent reconnaître et détruire les cellules cancéreuses, mais seulement si elles pénètrent physiquement dans la tumeur. Chez de nombreux patients, ces cellules n’atteignent pas la tumeur ou restent bloquées dans des tissus voisins comme les poumons, ce qui limite l’efficacité de traitements puissants, y compris les cellules CAR T et CAR NK modifiées. Traditionnellement, les scientifiques ont tenté de guider les cellules immunitaires au moyen d’indices protéiques, tels que les chimiokines et les molécules d’adhésion, qui agissent comme des panneaux de signalisation moléculaires. Pourtant, malgré ces connaissances, diriger les cellules immunitaires au cœur des tumeurs solides est resté étonnamment difficile, suggérant que d’autres types de signaux pourraient intervenir.
Découverte de “récepteurs olfactifs” cachés pour les métabolites tumoraux
Pour identifier de nouveaux systèmes de guidage, les chercheurs ont utilisé des cribles génétiques à grande échelle dans des cellules NK, activant des milliers de gènes pour déterminer lesquels favorisaient la migration de ces cellules vers des tumeurs mammaires et ovariennes chez la souris. Ils ont trouvé à plusieurs reprises un petit groupe de récepteurs — membres de la famille des récepteurs couplés aux protéines G (GPCR) — qui répondent non pas à des protéines mais à de petites molécules bioactives dérivées des lipides et du cholestérol. Le récepteur le plus remarquable, nommé GPR183, ainsi que plusieurs apparentés, n’apparaissent normalement que dans certains types de cellules immunitaires. Lorsqu’ils ont été ajoutés artificiellement à des cellules NK ou T, ces récepteurs ont agi comme de nouveaux « récepteurs olfactifs » détectant des métabolites libérés par les cellules cancéreuses et dirigeant les cellules modifiées vers les tumeurs.
Comment les sous-produits tumoraux deviennent une piste chimique
L’équipe a ensuite cherché à savoir ce que les tumeurs produisaient précisément pour attirer les cellules équipées de GPR183. Ils se sont concentrés sur les oxystérols — formes oxydées du cholestérol — synthétisés par des enzymes actives dans les cellules de cancer du sein invasif, surtout lorsque ces cellules sont exposées à des signaux inflammatoires. En supprimant des enzymes clés dans les cellules cancéreuses, les chercheurs ont montré que l’incapacité à produire certains oxystérols réduisait fortement la migration des cellules NK exprimant GPR183 vers des milieux conditionnés par la tumeur. Des expériences supplémentaires ont révélé que ces ligands non seulement créaient une piste chimique mais remodelaient aussi l’activité génique des cellules NK de façon dépendante du ligand, renforçant des programmes liés au mouvement et à l’organisation membranaire tout en diminuant certaines voies métaboliques.
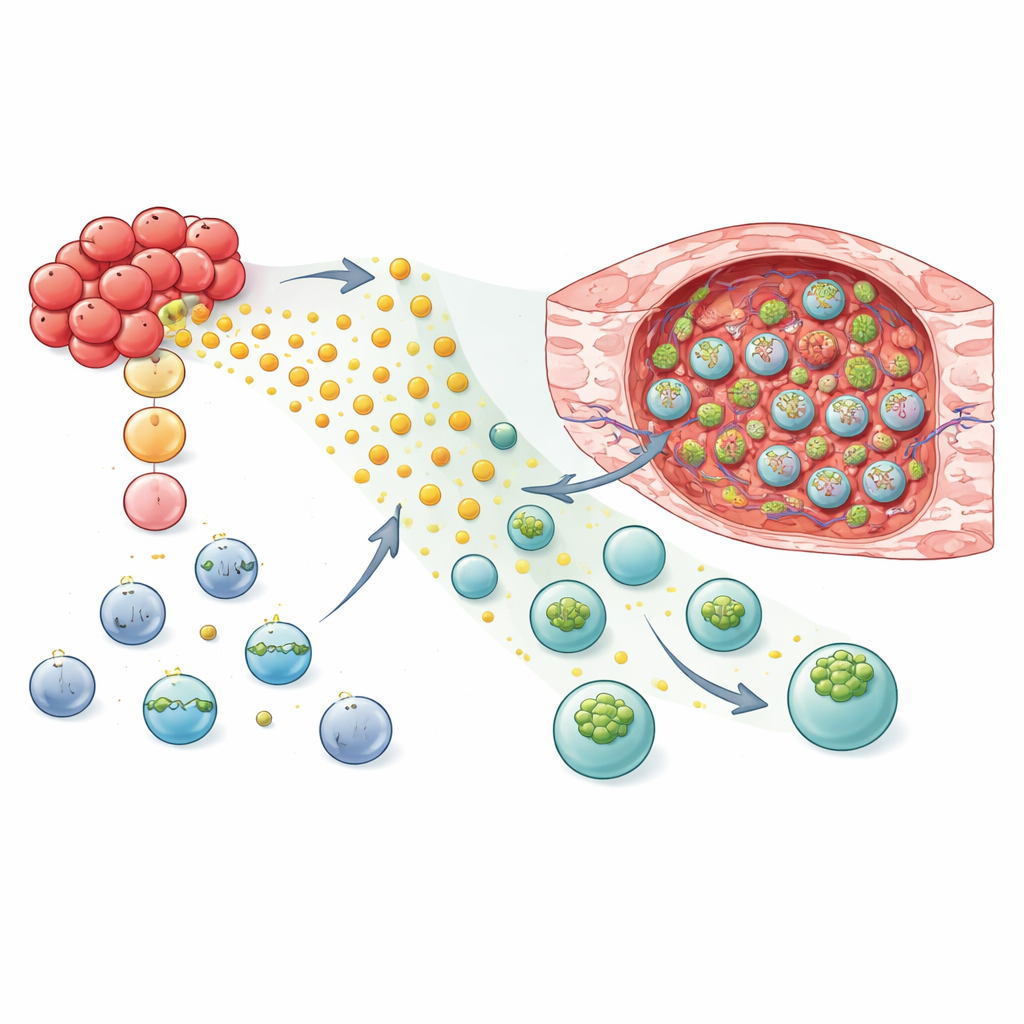
Reprogrammer les cellules NK et T pour qu’elles se localisent et attaquent
Fort de ces éclairages mécanistiques, les chercheurs ont testé si l’ajout de GPR183 pouvait améliorer les capacités de repérage des thérapies vivantes. Dans des modèles murins de cancer du sein, des cellules NK-92 et des cellules NK humaines primaires ingénierées avec GPR183 ont montré une migration préférentielle et marquée vers le tissu tumoral plutôt que vers le tissu pulmonaire sain. Lorsque ces cellules NK modifiées — ou des cellules CAR NK conçues pour reconnaître un marqueur de surface tumoral — ont été transférées chez des souris, la croissance tumorale était plus lente que chez les animaux recevant des cellules standards. La stratégie a également fonctionné pour les lymphocytes T : les cellules T CD8 conventionnelles et les cellules CAR T ciblant les tumeurs porteurs de GPR183 s’accumulaient en plus grand nombre dans les tumeurs tout en restant similaires dans les poumons et la rate. Dans un modèle murin immunocompétent, les cellules T exprimant la version murine de GPR183 contrôlaient plus efficacement les tumeurs mammaires et augmentaient la proportion d’animaux présentant une éradication complète de la tumeur.
Ce que cela pourrait signifier pour les traitements du cancer à venir
Pour un non-spécialiste, le message principal est que les auteurs ont trouvé un moyen de reprogrammer les cellules immunitaires pour qu’elles suivent « l’odeur » chimique du métabolisme tumoral. En équipant les cellules NK et T de récepteurs détectant les métabolites comme GPR183, ils ont transformé des forces immunitaires dispersées en chercheurs ciblés qui s’accumulent là où elles sont le plus nécessaires. Le travail suggère que, plutôt que de combattre la chimie tumorale, on peut la détourner — utiliser les molécules produites naturellement par les cellules cancéreuses comme repères de ciblage pour les thérapies cellulaires modifiées. Si cette approche est traduite en toute sécurité en clinique, elle pourrait aider à surmonter l’un des plus grands obstacles au traitement des tumeurs solides : amener suffisamment de cellules immunitaires puissantes au bon endroit au bon moment.
Citation: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
Mots-clés: immunothérapie, ingénierie cellulaire, tumeurs solides, chémotaxie, GPCRs