Clear Sky Science · he
הנדסת תאי NK ותאי T עם קולטנים החשים מטבוליטים כדי למקד גידולים מוצקים
הפיכת כימיה של הגידול לאות ניווט
רבים מהטיפולים המבטיחים ביותר כיום בסרטן נשענים על שחרור מערכת החיסון, אך גידולים מוצקים לעתים קרובות עומדים כמעוזים מוקפים חומות: התאים המיועדים להשמיד אותם אינם מגיעים בכמות מספקת. המחקר בוחן דרך חדשה להפוך תוצרי לוואי כימיים של הגידול לאיתותים שמושכים באופן פעיל תאי חיסון קטלנים פנימה, מה שעשוי להפוך טיפולי תאים מדור הבא ליעילים יותר כנגד סרטן שקשה לטפל בו, כמו סרטןי שד ושחלות.
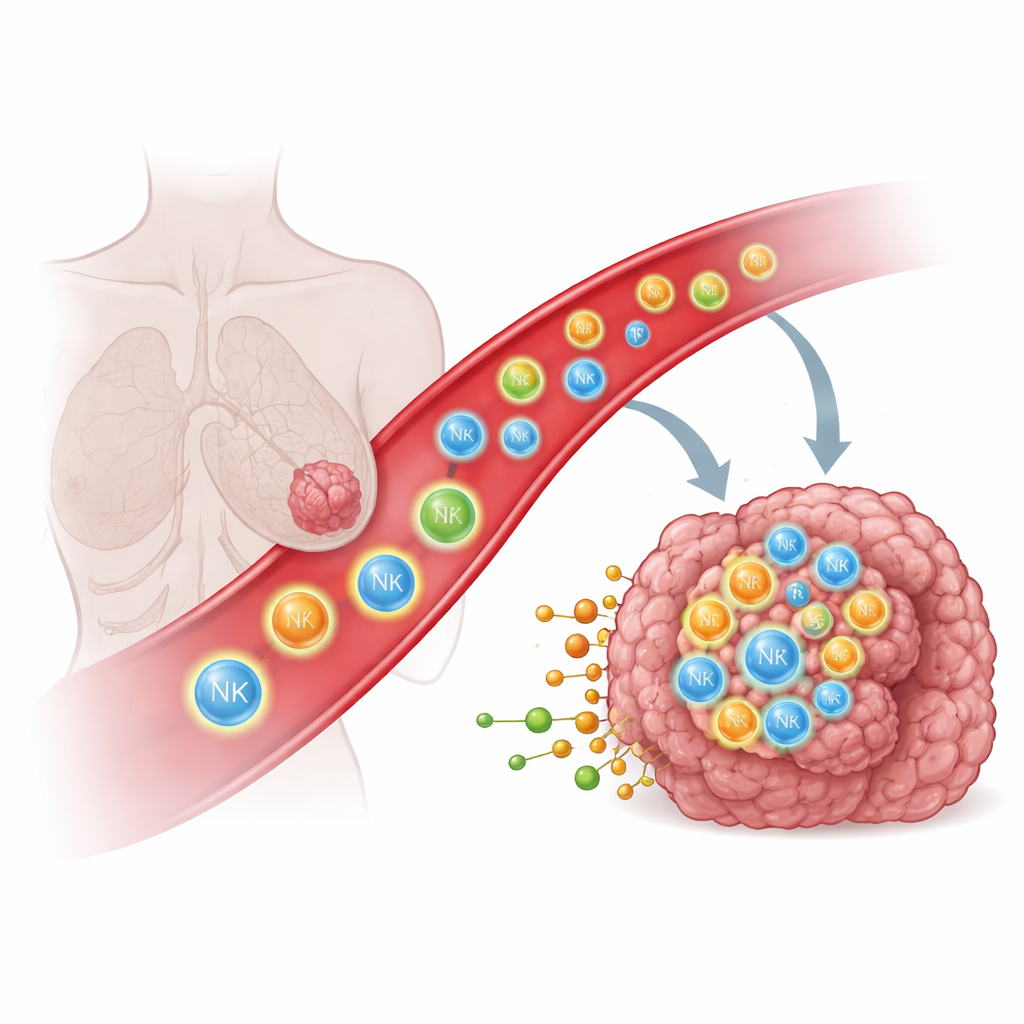
מדוע תאי חיסון מתקשים להגיע לגידולים מוצקים
תאי חיסון כגון תאי הרג טבעיים (NK) ותאי T יכולים לזהות ולהשמיד תאי סרטן, אך רק אם הם נכנסים פיזית לגידול. אצל רבים מהחולים, תאים אלה או שלא מגיעים לגידול כלל או שנתקעים ברקמות קרובות כגון הריאות, מה שמגביל את השפעתם של טיפולים רבי עוצמה, כולל תאי CAR T ותאי CAR NK מהונדסים. בדרך כלל ניסו המדענים להנחות תאי חיסון באמצעות איתותים חלבוניים, כגון כימוקינים ומולקולות הצמדה, הפועלים כסימני דרך מולקולריים. עם זאת, אפילו עם הידע הזה, כיוונון תאי החיסון עמוק לתוך גידולים מוצקים נותר קשה באופן מפתיע, מה שמרמז שאותות מסוגים אחרים עשויים לשחק תפקיד.
גילוי "קולטני ריח" חבויים למטבוליטים של הגידול
כדי לחשוף מערכות הנחיה חדשות, הצוות השתמש בסקרי גנטיקה בקנה מידה רחב בתאי NK, והפעילו אלפים של גנים כדי לראות אילו מהם עוזרים לתאים אלה להיגרר לתוך גידולי שד ושחלות בעכברים. הם מצאו שוב ושוב קבוצה קטנה של קולטנים — חברי משפחת הקולטנים הזוגיים G-protein-coupled receptor (GPCR) — שמגיבים לא לחלבונים אלא למולקולות קטנות וביואקטיביות הנגזרות משומנים וכולסטרול. הקולטן הבולט, GPR183, לצד כמה קרובים לו, מופיע בדרך כלל רק בסוגים נבחרים של תאי חיסון. כאשר הוצג באופן מלאכותי בתאי NK או T, הקולטנים הללו פעלו כ"קולטני ריח" חדשים שזיהו מטבוליטים שמשחררים תאי סרטן והכוונו את התאים המהונדסים לעבר הגידולים.
כיצד תוצרי לוואי של הגידול הופכים לשביל כימי
הצוות שאל לאחר מכן מה בדיוק מייצרים הגידולים שמושכים תאים הצוידו ב-GPR183. הם התמקדו באוקסיסטרולים — צורות מחומצנות של כולסטרול — המיוצרות על ידי אנזימים הפעילים בתאי סרטן שד פולשניים, במיוחד כאשר תאים אלה חשופים לאותות דלקתיים. על ידי השתקת אנזימים מרכזיים בתאי הסרטן, הראו החוקרים שהסרת היכולת לייצר אוקסיסטרולים ספציפיים מורידה באופן חדה את ההגירה של תאי NK מבטאים GPR183 לעבר מדיום מותנה בגידול. ניסויים נוספים חשפו שליגנדים אלה לא רק יוצרים שביל כימי אלא גם מעצבים מחדש את פעילות הגנים של תאי NK בצורה התלויה בליגנד, ומגבירים תוכניות הקשורות לתנועה ולארגון ממברנה תוך דיכוי מסלולים מטבוליים מסוימים.
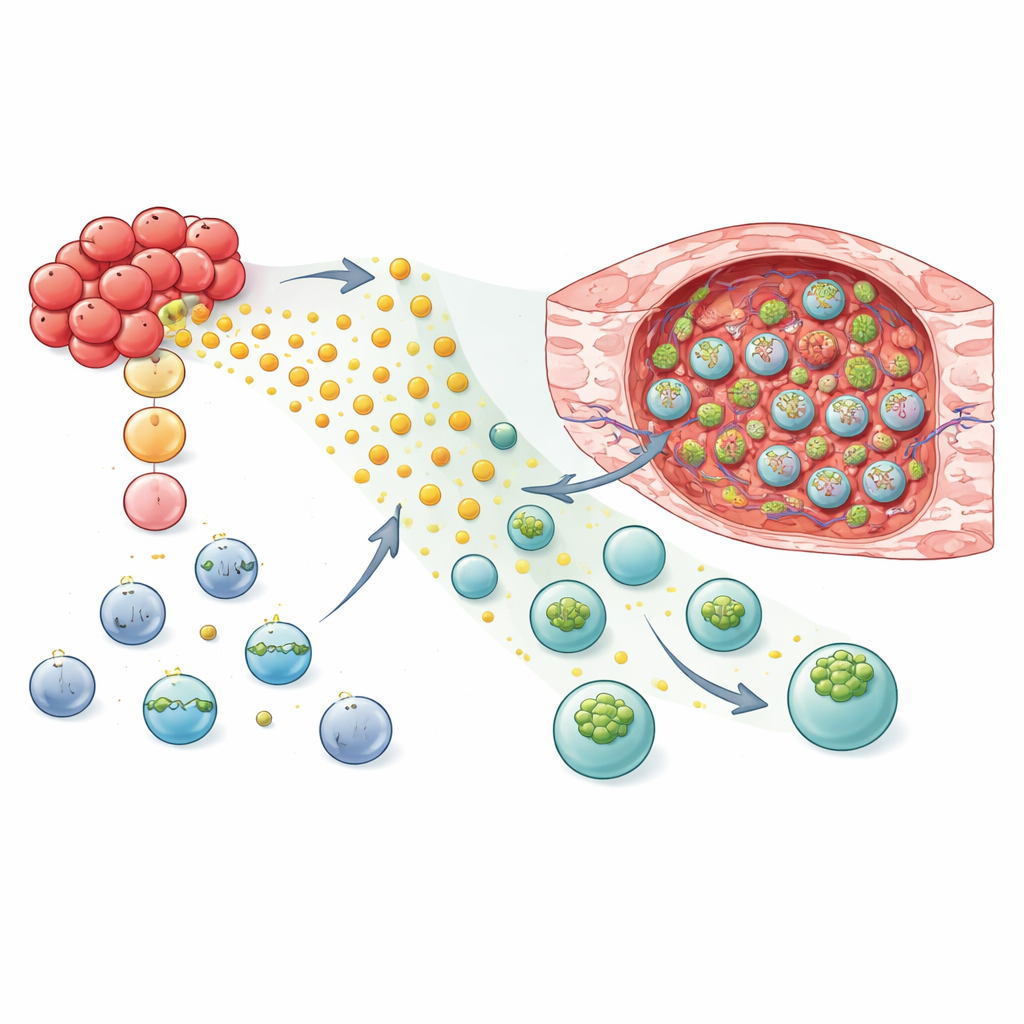
תכנות מחדש של תאי NK ותאי T כדי לנווט ולהתקיף
מצוידים בתובנה מכנית זו, החוקרים בדקו האם הוספת GPR183 יכולה להפוך טיפולים חיים לציידים טובים יותר של גידולים. במודלים של עכברים לסרטן השד, תאי NK-92 ותאי NK ראשוניים של בני אדם מהונדסים עם GPR183 הראו הגירה חזקה והעדפתית לרקמת הגידול על פני רקמת ריאה בריאה. כאשר תאים NK נערכו אלה — או תאי CAR NK המיועדים לזהות סממן פני השטח של הגידול — הוזרמו לעכברים, הגידולים גדלו לאט יותר מאשר בבעלי חיים שקיבלו תאים סטנדרטיים. האסטרטגיה עבדה גם על תאי T: גם תאי CD8 המסורתיים וגם תאי CAR T מכוונים לגידול הנשאו ברמות גבוהות יותר בתוך הגידולים בעוד שהם נשארים בדומה בריאה ובטחול. במודל עכבר בעל מערכת חיסון תקינה, תאים נושאי הגרסה העכברית של GPR183 שלטו טוב יותר בגידולי השד והעלו את שיעור בעלי החיים שבהם נצפתה הכחדה מלאה של הגידול.
מה משמעות הדבר עבור טיפולי סרטן עתידיים
לא-מומחה, המסר המרכזי הוא שהמחברים מצאו דרך לתכנת מחדש תאי חיסון כך שיפעלו לפי "ריח" כימי של המטבוליזם של הגידול עצמו. על ידי הציוד של תאי NK ותאי T בקולטנים החשים מטבוליטים כגון GPR183, הם הפכו כוחות חיסוניים מפוזרים לחודרי מטרה המצטברים במקום שבו הם נדרשים ביותר. העבודה מרמזת שبدلاً ממאבק בכימיה של הגידול, ניתן לפרמט אותה מחדש — להשתמש במולקולות שתאי הסרטן מפיקים באופן טבעי כאותות ניווט לטיפולי תאים מהונדסים. אם יותאם בצורה בטוחה לקליניקה, גישה זו עשויה לסייע להתגבר על אחת המכשולים הגדולים בטיפול בגידולים מוצקים: הבאת תאי חיסון רבי עוצמה למקום הנכון בזמנים הנכונים.
ציטוט: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
מילות מפתח: אימונותרפיה, הנדסת תאים, גידולים מוצקים, כימוטקסיס, GPCRs