Clear Sky Science · ru
Инжиниринг NK- и T-клеток с рецепторами, чувствительными к метаболитам, для нацеливания на солидные опухоли
Преобразование химии опухоли в сигнал для ориентации
Многие из наиболее перспективных противораковых методов сегодня опираются на высвобождение иммунной системы, однако солидные опухоли часто напоминают окружённые стенами крепости: клетки, предназначенные для их уничтожения, просто не попадают туда в достаточном количестве. В этом исследовании изучается новый подход, позволяющий превратить собственные химические побочные продукты опухоли в маяки, активно притягивающие киллерные иммунные клетки внутрь, что потенциально делает клеточные терапии следующего поколения гораздо более эффективными против трудноизлечимых опухолей, таких как рак молочной железы и яичников.
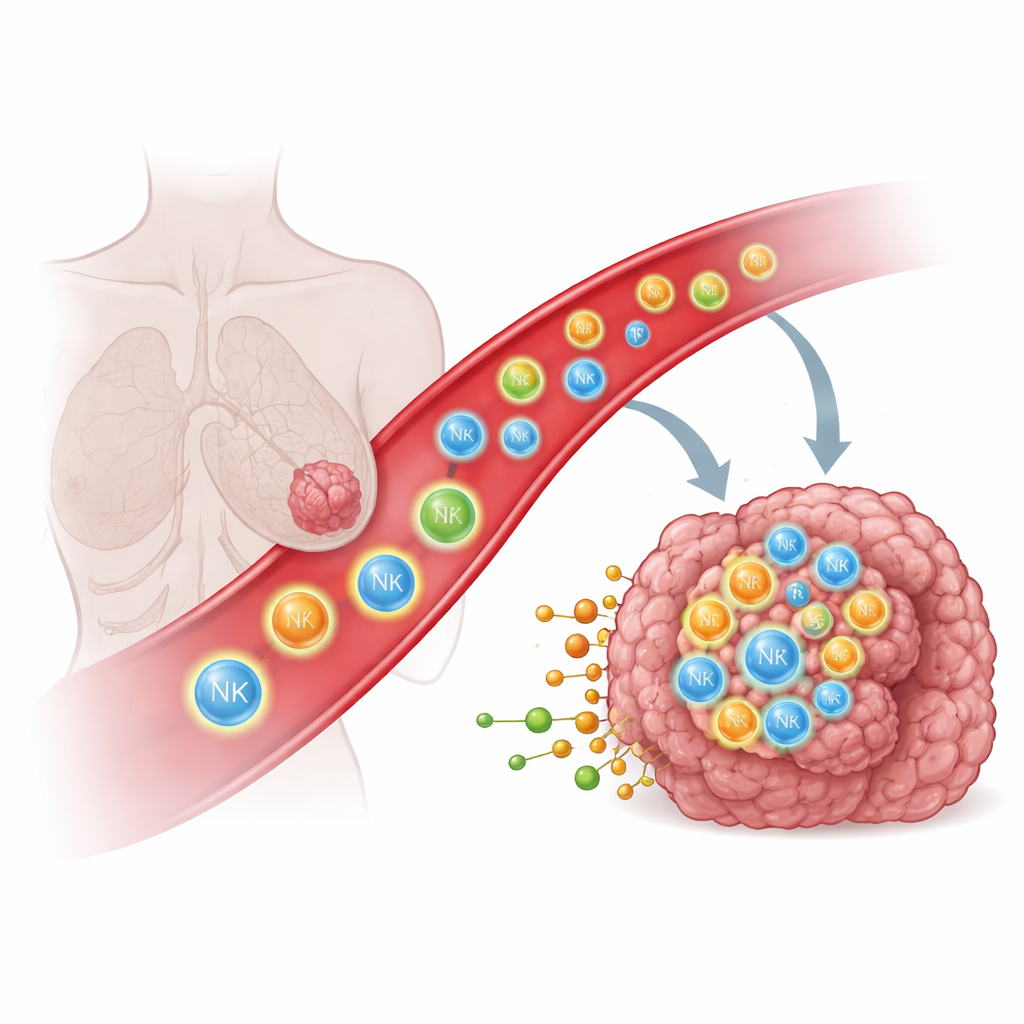
Почему иммунные клетки с трудом достигают солидных опухолей
Иммунные клетки, такие как натуральные киллеры (NK) и T-клетки, способны распознавать и уничтожать раковые клетки, но только если они физически проникают в опухоль. У многих пациентов эти клетки либо вообще не достигают опухоли, либо застревают в прилежащих тканях, например в лёгких, что ограничивает эффективность мощных терапий, включая индуцированные CAR T и CAR NK клетки. Традиционно учёные пытались направлять иммунные клетки с помощью белковых сигналов, таких как хемокины и молекулы адгезии, действующих как молекулярные указатели. Тем не менее даже с учётом этих знаний направить иммунные клетки глубоко в солидные опухоли оказалось удивительно трудно, что указывает на важность других типов сигналов.
Открытие скрытых «обонятельных рецепторов» для метаболитов опухоли
Чтобы выявить новые системы навигации, исследователи провели крупномасштабные генетические скрины в NK-клетках, поочерёдно активируя тысячи генов, чтобы выяснить, какие из них помогают этим клеткам мигрировать в молочные и яичниковые опухоли у мышей. Они неоднократно обнаруживали небольшую группу рецепторов — представителей семейства G-протеин-связанных рецепторов (GPCR) — которые реагируют не на белки, а на небольшие биоактивные молекулы, производные жиров и холестерина. Выделяющийся рецептор GPR183 и несколько его родственных форм обычно встречаются только в избранных типах иммунных клеток. При искусственном добавлении в NK- или T-клетки эти рецепторы действовали как новые «обонятельные рецепторы», улавливающие метаболиты, выделяемые раковыми клетками, и направлявшие модифицированные клетки к опухолям.
Как побочные продукты опухоли превращаются в химическую тропу
Команда затем выясняла, что именно продуцируют опухоли, привлекающее клетки, оснащённые GPR183. Они сосредоточились на оксистеролах — окисленных формах холестерина — которые синтезируются ферментами, активными в инвазивных клетках рака молочной железы, особенно при воздействии воспалительных сигналов. Устраняя ключевые ферменты в раковых клетках, исследователи показали, что потеря способности производить определённые оксистеролы резко снижает миграцию NK-клеток, экспрессирующих GPR183, к среде, обусловленной опухолью. Дополнительные эксперименты показали, что эти лиганды не только создают химическую тропу, но и изменяют активность генов NK-клеток в лигандо-зависимом ключе, усиливая программы, связанные с подвижностью и организацией мембраны, и ослабляя определённые метаболические пути.
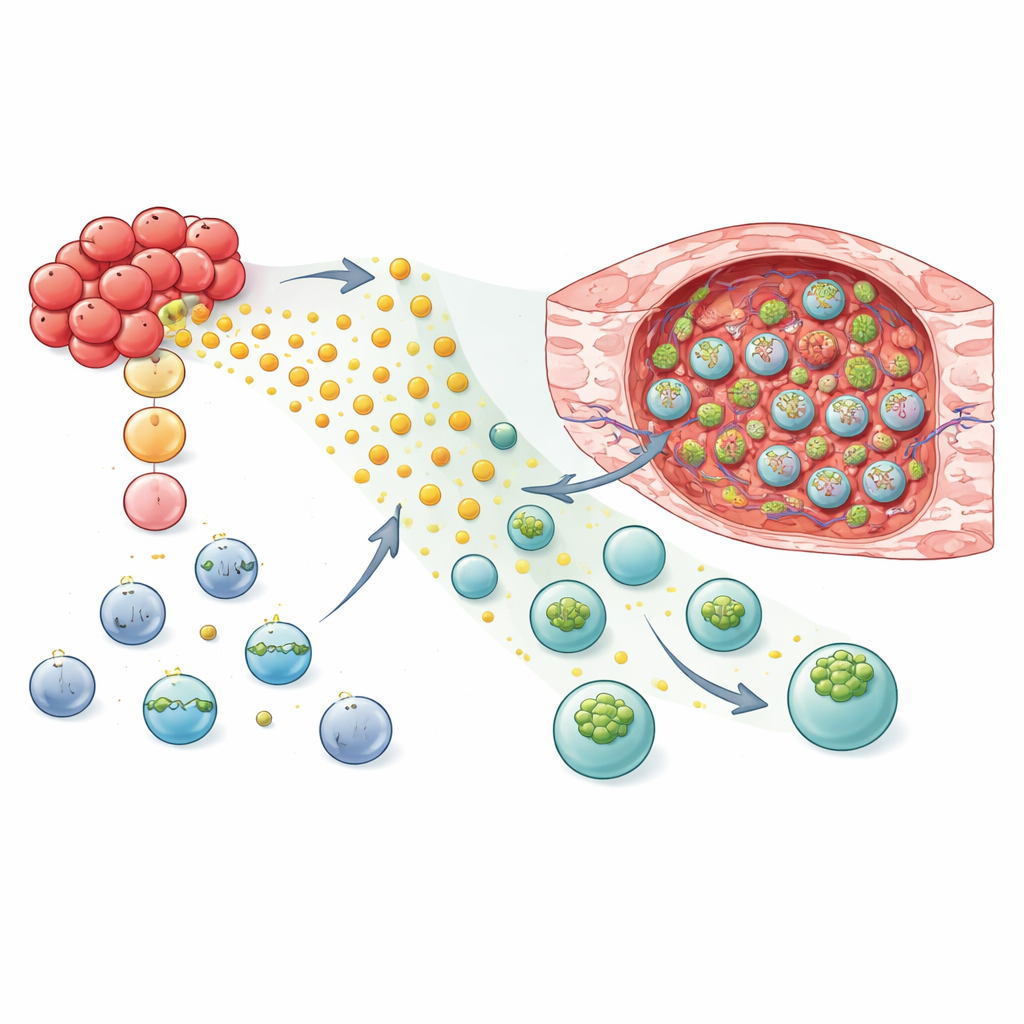
Перепрограммирование NK- и T-клеток для нацеливания и атаки
Вооружившись этим молекулярным пониманием, исследователи проверили, сможет ли добавление GPR183 сделать клеточные терапии лучшими «охотниками» за опухолью. В мышиных моделях рака молочной железы NK-92 клетки и первичные человеческие NK-клетки, инжинированные с GPR183, демонстрировали сильную, предпочтительную миграцию в опухолевую ткань по сравнению со здоровой лёгочной тканью. Когда эти модифицированные NK-клетки — или CAR NK-клетки, спроектированные для распознавания маркера на поверхности опухоли — были перенесены мышам, рост опухолей замедлялся сильнее, чем у животных, получавших стандартные клетки. Стратегия также сработала для T-клеток: как конвенциональные CD8 T-клетки, так и целевые CAR T-клетки с GPR183 накапливались в опухолях в больших количествах, оставаясь при этом на схожем уровне в лёгких и селезёнке. В иммунокомпетентной мышиной модели T-клетки, несущие мышиную версию GPR183, эффективнее контролировали рост молочных опухолей и увеличивали долю животных с полным очищением от опухоли.
Что это может значить для будущих противораковых методов
Для неспециалиста основная идея такова: авторы нашли способ перенастроить иммунные клетки так, чтобы они следовали за химическим «запахом» метаболизма самой опухоли. Оснастив NK- и T-клетки рецепторами, чувствительными к метаболитам, такими как GPR183, они превратили рассеянные иммунные силы в целенаправленных искателей, которые накапливаются там, где они наиболее нужны. Работа показывает, что вместо того чтобы бороться с химией опухоли, мы можем её перехватить — использовать молекулы, которые раковые клетки естественно продуцируют, как навигационные сигналы для модифицированных клеточных терапий. При безопасной трансляции в клинику этот подход может помочь преодолеть одну из крупнейших проблем в лечении солидных опухолей: доставить достаточное количество мощных иммунных клеток в нужное место в нужное время.
Цитирование: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
Ключевые слова: иммунотерапия, клеточная инженерия, солидные опухоли, хемотаксис, GPCRs