Clear Sky Science · es
Ingeniería de células NK y T con receptores que detectan metabolitos para atacar tumores sólidos
Convertir la química tumoral en una señal de guiado
Muchos de los tratamientos oncológicos más prometedores de hoy se basan en liberar al sistema inmunitario, sin embargo los tumores sólidos a menudo permanecen como fortalezas amuralladas: las mismas células encargadas de destruirlos nunca llegan en número suficiente. Este estudio explora una nueva forma de convertir los subproductos químicos del propio tumor en balizas que atraen activamente a las células inmunitarias asesinas, lo que podría hacer que las terapias celulares de nueva generación sean mucho más efectivas contra cánceres de difícil tratamiento, como los de mama y ovario.
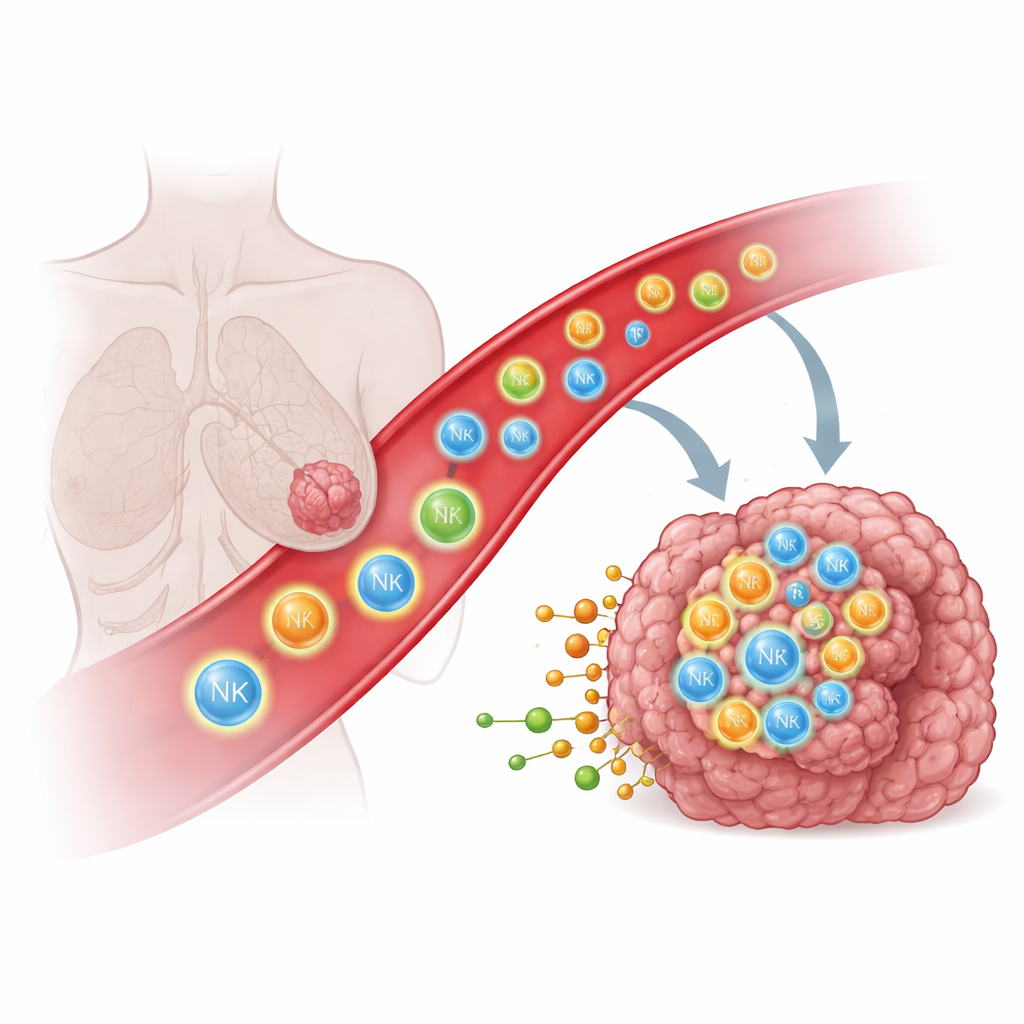
Por qué las células inmunitarias tienen dificultades para alcanzar los tumores sólidos
Células inmunitarias como las natural killer (NK) y las células T pueden reconocer y destruir células cancerosas, pero sólo si penetran físicamente en el tumor. En muchos pacientes, estas células o bien nunca alcanzan el tumor o quedan atrapadas en tejidos cercanos, como los pulmones, lo que limita el impacto de terapias potentes, incluidas las CAR T y CAR NK diseñadas. Tradicionalmente, los científicos han intentado dirigir las células inmunitarias usando señales proteicas, como quimiocinas y moléculas de adhesión, que actúan como señales moleculares. No obstante, incluso con ese conocimiento, dirigir las células inmunitarias hacia el interior de tumores sólidos ha seguido siendo sorprendentemente difícil, lo que sugiere que podrían intervenir otros tipos de señales.
Descubrir “receptores olfativos” ocultos para metabolitos tumorales
Para desvelar nuevos sistemas de guiado, los investigadores emplearon cribados genéticos a gran escala en células NK, activando miles de genes para ver cuáles ayudaban a estas células a migrar hacia tumores de mama y ovario en ratones. Repetidamente encontraron un pequeño grupo de receptores—miembros de la familia de receptores acoplados a proteínas G (GPCR)—que responden no a proteínas, sino a pequeñas moléculas bioactivas derivadas de grasas y colesterol. El receptor destacado, llamado GPR183, junto con varios homólogos, aparece normalmente solo en tipos selectos de células inmunitarias. Cuando se añadieron de forma artificial a células NK o T, estos receptores actuaron como nuevos “receptores olfativos” que detectaban metabolitos liberados por las células cancerosas y guiaban a las células modificadas hacia los tumores.
Cómo los subproductos tumorales se convierten en un rastro químico
El equipo preguntó luego qué estaban produciendo exactamente los tumores que atraía a las células equipadas con GPR183. Se centraron en las oxisteroles—formas oxidadas del colesterol—producidas por enzimas activas en células de cáncer de mama invasivo, especialmente cuando esas células están expuestas a señales inflamatorias. Al eliminar enzimas clave en las células cancerosas, los investigadores demostraron que suprimir la capacidad de fabricar oxisteroles específicos reducía drásticamente la migración de células NK que expresaban GPR183 hacia medios condicionados por tumores. Experimentos adicionales revelaron que estos ligandos no solo creaban un rastro químico, sino que también remodelaban la actividad génica de las NK de manera dependiente del ligando, potenciando programas vinculados al movimiento y a la organización de la membrana mientras atenuaban ciertas rutas metabólicas.
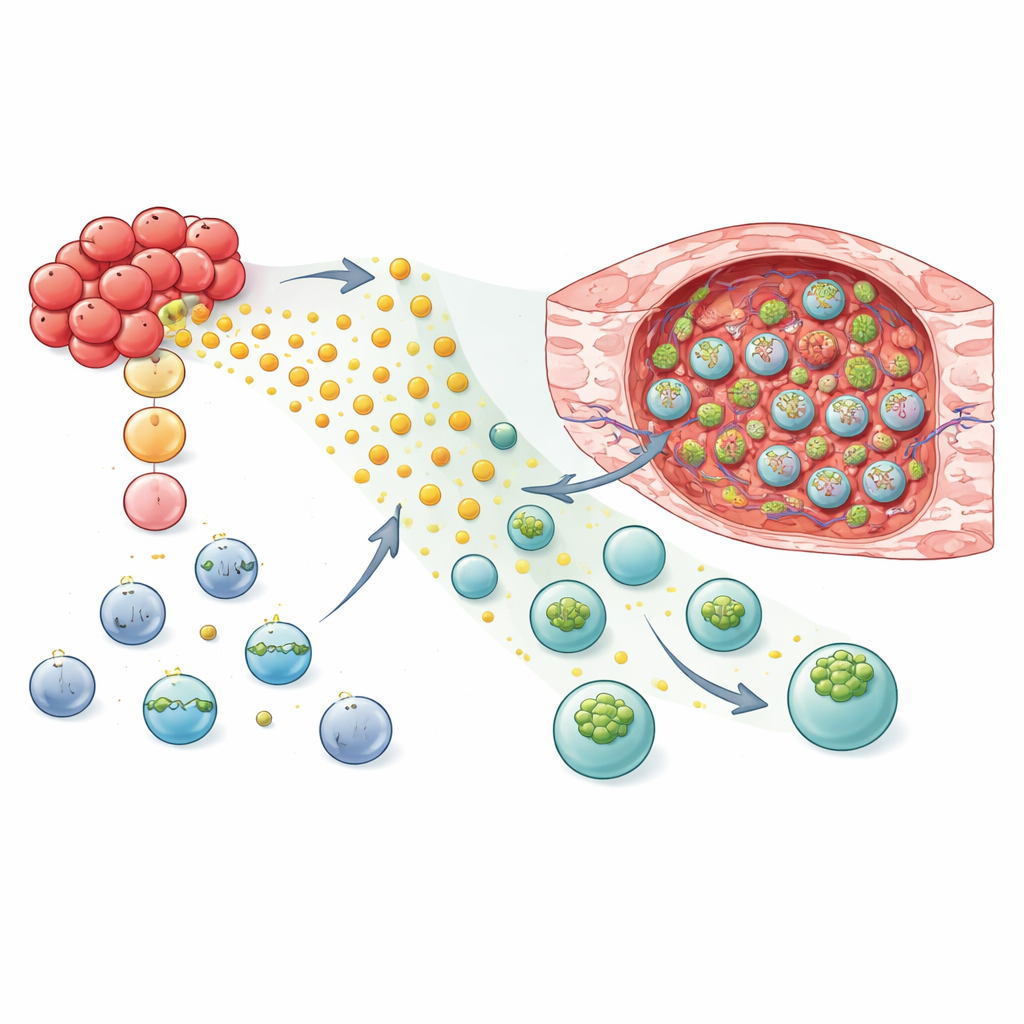
Reprogramar células NK y T para localizar y atacar
Con este conocimiento mecanístico, los investigadores probaron si añadir GPR183 podía convertir las terapias vivas en mejores buscadores tumorales. En modelos murinos de cáncer de mama, células NK-92 y células NK humanas primarias modificadas con GPR183 mostraron una migración fuerte y preferente hacia tejido tumoral frente al tejido pulmonar sano. Cuando estas NK editadas—or células NK con CAR diseñadas para reconocer un marcador tumoral de superficie—se transfirieron a ratones, los tumores crecieron más despacio que en animales que recibieron células estándar. La estrategia también funcionó con células T: tanto células T CD8 convencionales como células CAR T dirigidas al tumor con GPR183 se acumularon en mayor medida dentro de los tumores mientras permanecían similares en pulmón y bazo. En un modelo murino inmunocompetente, las células T portadoras de la versión murina de GPR183 controlaron mejor los tumores mamarios y aumentaron la fracción de animales con eliminación completa del tumor.
Qué podría significar esto para futuros tratamientos contra el cáncer
Para un público no especializado, el mensaje central es que los autores han encontrado una forma de reconectar las células inmunitarias para que sigan el “olor” químico del propio metabolismo tumoral. Al equipar células NK y T con receptores que detectan metabolitos como GPR183, convirtieron fuerzas inmunitarias dispersas en buscadores dirigidos que se acumulan donde más se les necesita. El trabajo sugiere que, en lugar de combatir la química tumoral, podemos secuestrarla—usando las moléculas que las células cancerosas producen de forma natural como señales de guiado para terapias celulares diseñadas. Si se traduce de forma segura a la clínica, este enfoque podría ayudar a superar uno de los mayores obstáculos en el tratamiento de tumores sólidos: conseguir que suficientes células inmunitarias potentes lleguen al lugar correcto en el momento adecuado.
Cita: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
Palabras clave: inmunoterapia, ingeniería celular, tumores sólidos, quimiotaxis, GPCRs