Clear Sky Science · it
Ingegnerizzare cellule NK e T con recettori sensibili ai metaboliti per mirare i tumori solidi
Trasformare la chimica del tumore in un segnale di richiamo
Molti dei trattamenti antitumorali più promettenti oggi si basano sul liberare il sistema immunitario, ma i tumori solidi spesso si comportano come fortezze: le stesse cellule destinate a eliminarli non arrivano mai in numero sufficiente. Questo studio esplora un nuovo modo per trasformare i prodotti chimici del tumore in segnali che attirano attivamente le cellule immunitarie citotossiche all’interno, potenzialmente rendendo le terapie cellulari di nuova generazione molto più efficaci contro tumori difficili da trattare, come quelli al seno e alle ovaie.
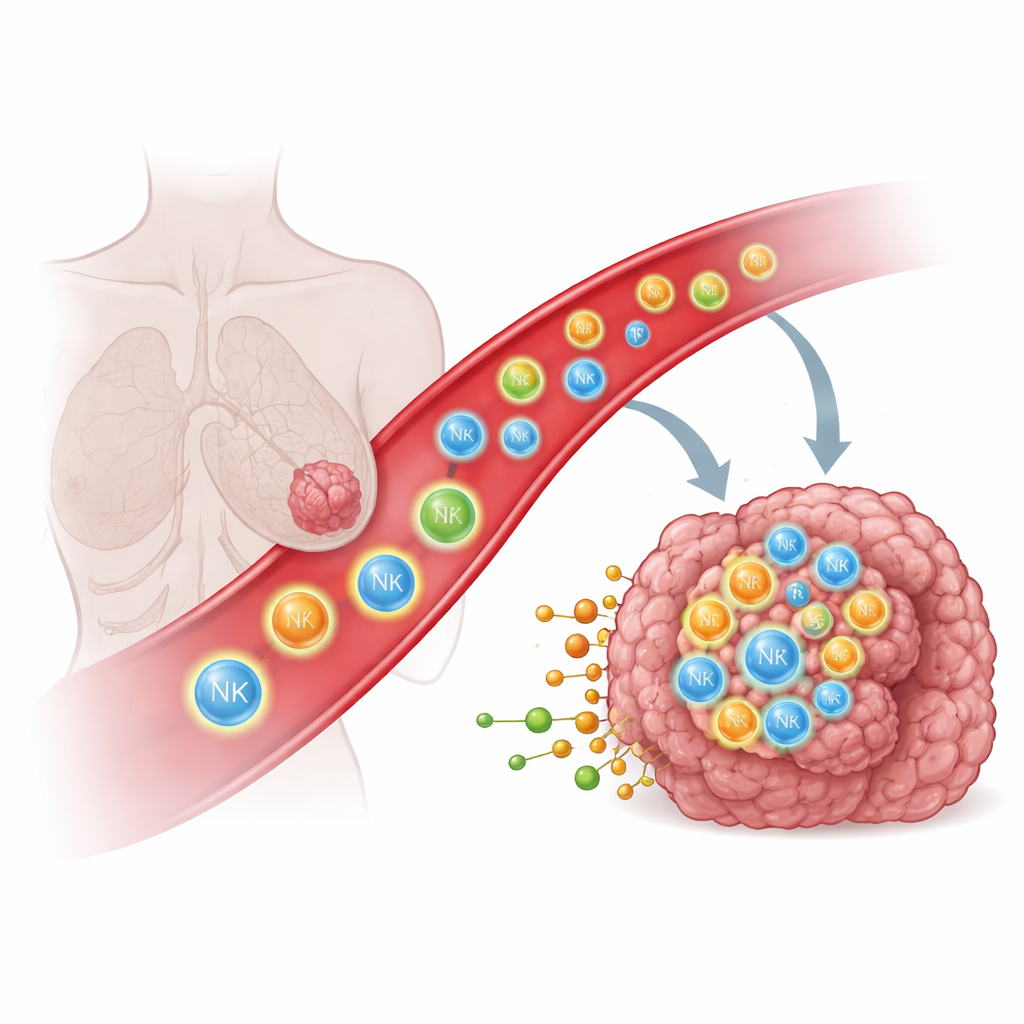
Perché le cellule immunitarie faticano a raggiungere i tumori solidi
Cellule immunitarie come le natural killer (NK) e le cellule T possono riconoscere e distruggere le cellule cancerose, ma solo se entrano fisicamente nel tumore. In molti pazienti queste cellule o non raggiungono mai il tumore o rimangono intrappolate in tessuti vicini come i polmoni, limitando l’impatto di terapie potenti, incluse le cellule CAR T e CAR NK ingegnerizzate. Tradizionalmente, i ricercatori hanno cercato di guidare le cellule immunitarie usando segnali proteici, come chemiokine e molecole di adesione, che funzionano come segnali stradali molecolari. Eppure, anche con queste conoscenze, indirizzare le cellule immunitarie in profondità nei tumori solidi è rimasto sorprendentemente difficile, suggerendo che potrebbero agire altri tipi di segnali.
Scoprire «recettori dell’olfatto» nascosti per i metaboliti tumorali
Per individuare nuovi sistemi di guida, i ricercatori hanno utilizzato screening genetici su larga scala in cellule NK, attivando migliaia di geni per vedere quali favorivano la migrazione di queste cellule verso tumori mammari e ovarici nei topi. Hanno ripetutamente trovato un piccolo gruppo di recettori — membri della famiglia dei recettori accoppiati alla proteina G (GPCR) — che rispondono non a proteine ma a piccole molecole bioattive derivate da lipidi e colesterolo. Il recettore più significativo, chiamato GPR183, insieme ad alcuni suoi simili, normalmente compare solo in tipi selezionati di cellule immunitarie. Quando è stato aggiunto artificialmente a cellule NK o T, questi recettori si sono comportati come nuovi “recettori dell’olfatto” che percepiscono i metaboliti rilasciati dalle cellule tumorali e guidano le cellule ingegnerizzate verso i tumori.
Come i prodotti di scarto del tumore diventano una traccia chimica
Il gruppo ha poi indagato cosa esattamente producessero i tumori che attirava le cellule dotate di GPR183. Si sono concentrati sugli oxysterol — forme ossidate del colesterolo — sintetizzate da enzimi attivi nelle cellule di carcinoma mammario invasivo, soprattutto in presenza di segnali infiammatori. Disattivando enzimi chiave nelle cellule tumorali, i ricercatori hanno dimostrato che rimuovere la capacità di produrre specifici oxysterol riduceva nettamente la migrazione delle cellule NK esprimenti GPR183 verso i meiosi condizionati dal tumore. Esperimenti aggiuntivi hanno rivelato che questi ligandi non solo creavano una traccia chimica, ma rimodellavano anche l’attività genica delle NK in modo dipendente dal ligando, potenziando programmi legati al movimento e all’organizzazione della membrana e attenuando alcune vie metaboliche.
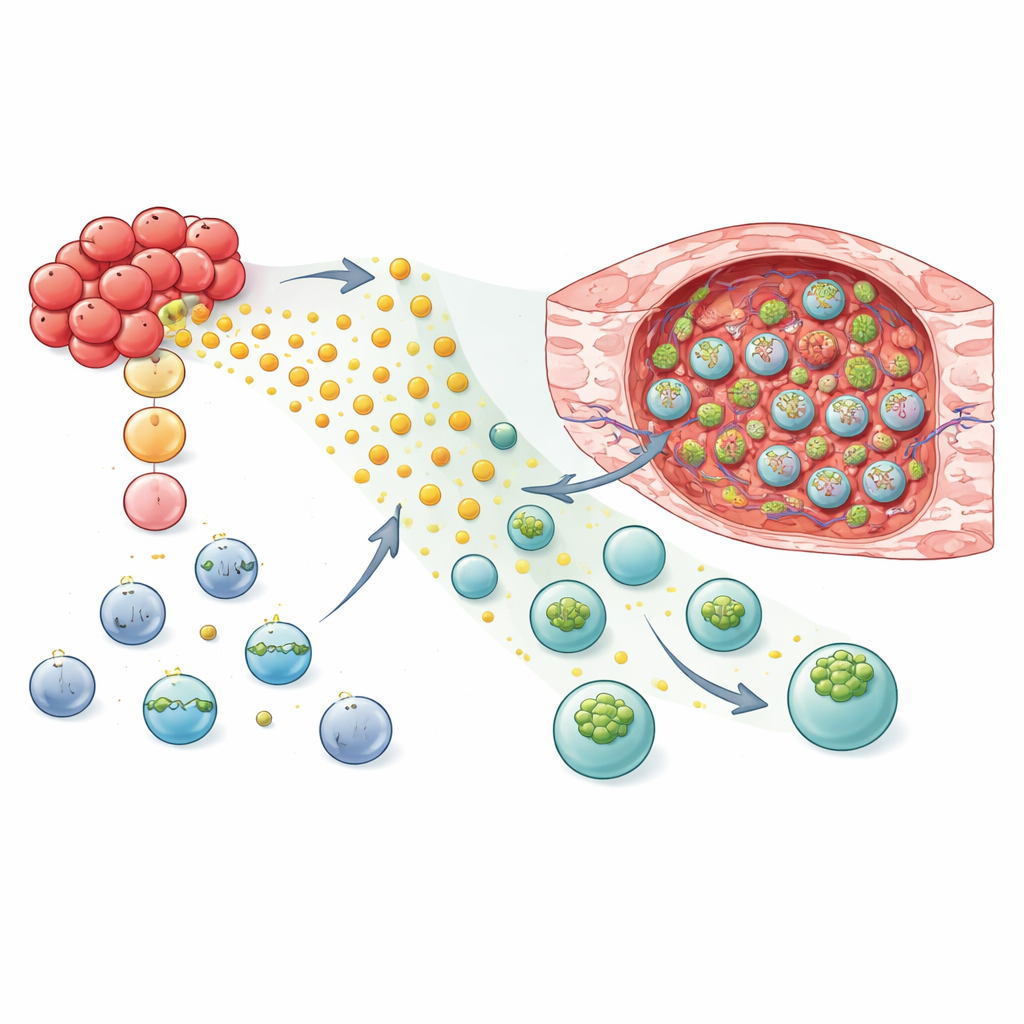
Riprogammazione di cellule NK e T per localizzare e attaccare
Forti di questa comprensione meccanicistica, i ricercatori hanno testato se aggiungere GPR183 potesse rendere le terapie cellulari migliori cacciatrici di tumori. Nei modelli murini di carcinoma mammario, cellule NK-92 e NK primarie umane ingegnerizzate con GPR183 hanno mostrato una forte migrazione preferenziale verso il tessuto tumorale rispetto al tessuto polmonare sano. Quando queste NK modificate — o NK CAR progettate per riconoscere un marcatore di superficie tumorale — sono state trasferite nei topi, i tumori crescevano più lentamente rispetto agli animali che ricevevano cellule standard. La strategia ha funzionato anche per le cellule T: sia le cellule CD8 convenzionali sia le CAR T tumorali con GPR183 si sono accumulate in quantità maggiori all’interno dei tumori mantenendo livelli simili in polmone e milza. In un modello murino immunocompetente, le T dotate della versione murina di GPR183 hanno controllato meglio i tumori mammari e aumentato la frazione di animali con completa eliminazione del tumore.
Cosa potrebbe significare per i trattamenti antitumorali futuri
Per un non specialista, il messaggio centrale è che gli autori hanno trovato un modo per riprogrammare le cellule immunitarie affinché seguano il “odore” chimico del metabolismo del tumore. Dotando NK e T di recettori sensibili ai metaboliti come GPR183, hanno trasformato forze immunitarie disperse in cercatori mirati che si accumulano dove sono più necessarie. Il lavoro suggerisce che, invece di combattere la chimica del tumore, possiamo sfruttarla — usando le molecole prodotte naturalmente dalle cellule cancerose come segnali di richiamo per terapie cellulari ingegnerizzate. Se tradotto in sicurezza in clinica, questo approccio potrebbe aiutare a superare uno dei maggiori ostacoli nel trattamento dei tumori solidi: portare un numero sufficiente di cellule immunitarie potenti nel posto giusto al momento giusto.
Citazione: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
Parole chiave: immunoterapia, ingegneria cellulare, tumori solidi, chemiotassi, GPCR