Clear Sky Science · de
Ingenieurmäßige Modifikation von NK- und T-Zellen mit stoffwechsel-sensitiven Rezeptoren zur gezielten Bekämpfung solider Tumoren
Tumorchemie in ein Ortungssignal verwandeln
Viele der heute vielversprechendsten Krebstherapien beruhen darauf, das Immunsystem zu entfesseln, doch solide Tumoren gleichen oft befestigten Festungen: Die Zellen, die sie angreifen sollen, erreichen sie nie in ausreichender Zahl. Diese Studie untersucht einen neuen Weg, die chemischen Abbauprodukte des Tumors in Leuchtsignale zu verwandeln, die aktiv Killer-Immunzellen anziehen und so die Wirksamkeit künftiger Zelltherapien bei schwer behandelbaren Krebsarten wie Brust- und Eierstocktumoren deutlich steigern könnten.
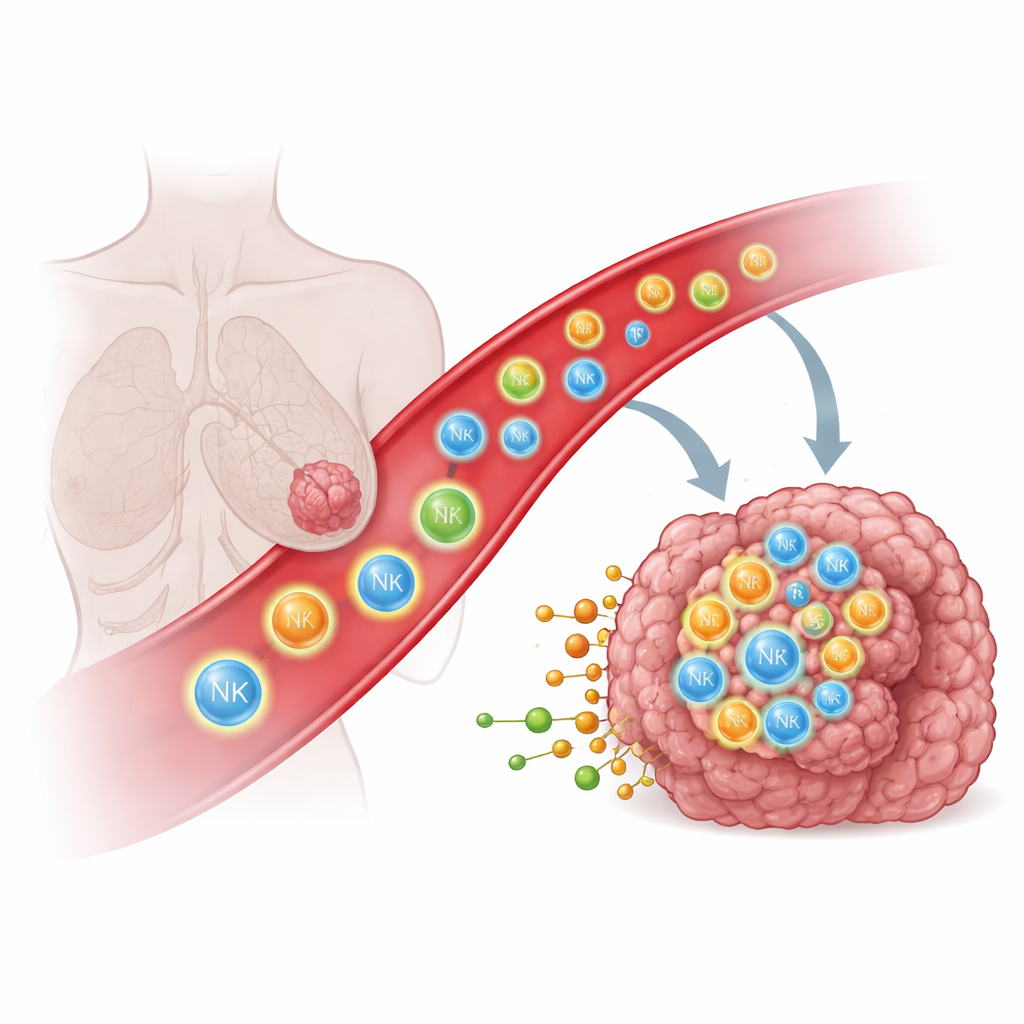
Warum Immunzellen Schwierigkeiten haben, solide Tumoren zu erreichen
Immunzellen wie natürliche Killer-(NK-)Zellen und T-Zellen können Krebszellen erkennen und zerstören, aber nur, wenn sie physisch in den Tumor eindringen. Bei vielen Patientinnen und Patienten erreichen diese Zellen den Tumor gar nicht oder bleiben in angrenzenden Geweben wie der Lunge stecken, was die Wirkung leistungsstarker Therapien — darunter gentechnisch veränderte CAR-T- und CAR-NK-Zellen — einschränkt. Traditionell versuchten Wissenschaftler, Immunzellen mit proteinbasierten Signalen wie Chemokinen und Adhäsionsmolekülen zu leiten, die wie molekulare Straßenschilder wirken. Dennoch bleibt es überraschend schwierig, Immunzellen tief in solide Tumoren zu dirigieren, was nahelegt, dass andere Signalarten eine Rolle spielen.
Verborgene „Geruchsrezeptoren“ für Tumormetabolite entdecken
Um neue Orientierungssysteme aufzuspüren, nutzten die Forschenden groß angelegte genetische Screens in NK-Zellen und schalteten Tausende von Genen ein, um zu sehen, welche das Eindringen dieser Zellen in Brust- und Eierstocktumoren bei Mäusen förderten. Wiederholt fanden sie eine kleine Gruppe von Rezeptoren — Mitglieder der Familie der G-Protein-gekoppelten Rezeptoren (GPCR) — die nicht auf Proteine, sondern auf kleine, bioaktive Moleküle reagieren, die aus Fetten und Cholesterin abgeleitet sind. Der herausragende Rezeptor GPR183, zusammen mit mehreren Verwandten, kommt normalerweise nur in ausgewählten Immunzelltypen vor. Werden diese Rezeptoren künstlich in NK- oder T-Zellen eingeführt, wirkten sie wie neue „Geruchsrezeptoren“: Sie erkannten von Krebszellen freigesetzte Metabolite und lenkten die konstruierten Zellen in Richtung der Tumoren.
Wie Tumorabfallprodukte zu einer chemischen Fährte werden
Das Team untersuchte danach, was genau die Tumoren produzierten, das GPR183-ausgerüstete Zellen anzog. Im Fokus standen Oxysterole — oxidierte Formen von Cholesterin —, die von Enzymen erzeugt werden, die in invasiven Brustkrebszellen aktiv sind, insbesondere unter Einwirkung entzündlicher Signale. Durch das Ausschalten bestimmter Enzyme in den Krebszellen zeigten die Forschenden, dass der Verlust der Fähigkeit, spezifische Oxysterole zu produzieren, die Migration von GPR183-exprimierenden NK-Zellen zu tumorbedingten Medien deutlich verringerte. Weitere Experimente zeigten, dass diese Liganden nicht nur eine chemische Spur erzeugten, sondern auch die Genaktivität der NK-Zellen ligandenabhängig umgestalteten, Bewegungsprogramme und Membranorganisation förderten und gleichzeitig bestimmte Stoffwechselwege herunterregulierten.
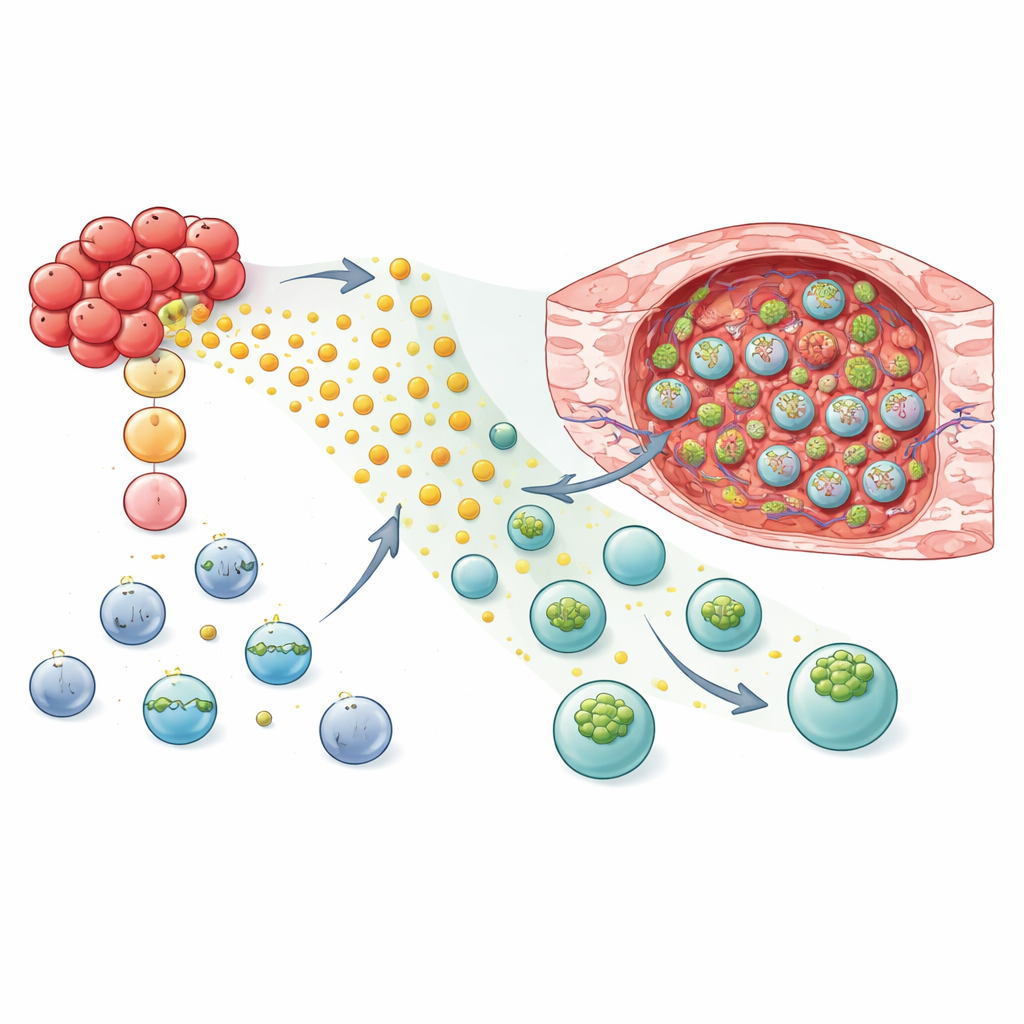
Umprogrammierung von NK- und T-Zellen zum gezielten Ansteuern und Angreifen
Mit diesem mechanistischen Verständnis testeten die Forschenden, ob das Hinzufügen von GPR183 lebende Zelltherapien zu besseren Tumorjägern macht. In Mausmodellen des Brustkrebses zeigten mit GPR183 versehene NK-92-Zellen und primäre humane NK-Zellen eine starke, präferentielle Migration ins Tumorgewebe im Vergleich zum gesunden Lungengewebe. Wurden diese editierten NK-Zellen — oder CAR-NK-Zellen, die auf ein Tumoroberflächenprotein abzielen — in Mäuse übertragen, wuchsen die Tumoren langsamer als bei Tieren, die Standardzellen erhielten. Die Strategie funktionierte auch für T-Zellen: Sowohl konventionelle CD8-T-Zellen als auch tumorgerichtete CAR-T-Zellen mit GPR183 reichern sich in höherer Zahl im Tumor an, während sie in Lunge und Milz ähnlich blieben. In einem immunkompetenten Mausmodell kontrollierten T-Zellen mit der Mausversion von GPR183 Brusttumoren wirksamer und erhöhten die Zahl der Tiere mit vollständiger Tumorreduktion.
Was das für künftige Krebstherapien bedeuten könnte
Für Nichtfachleute lautet die Kernbotschaft: Die Autorinnen und Autoren haben einen Weg gefunden, Immunzellen so umzurüsten, dass sie dem chemischen „Geruch“ des Tumorstoffwechsels folgen. Indem man NK- und T-Zellen mit stoffwechsel-sensitiven Rezeptoren wie GPR183 ausstattet, verwandelt man verstreute Immunkräfte in gezielte Sucher, die sich genau dort ansammeln, wo sie am meisten gebraucht werden. Die Arbeit legt nahe, dass man der Tumorchemie nicht zwingend entgegenwirken muss, sondern sie kapern kann — die von Krebszellen natürlich produzierten Moleküle als Ortungssignale für konstruktive Zelltherapien nutzend. Wenn sich dieser Ansatz sicher in die Klinik übersetzen lässt, könnte er eines der größten Probleme bei der Behandlung solider Tumoren überwinden: genügend potente Immunzellen zur richtigen Zeit an den richtigen Ort zu bringen.
Zitation: Kim, YM., Tsai, M.K., Sun, C. et al. Engineering NK and T cells with metabolite-sensing receptors to target solid tumors. Nat Immunol 27, 1039–1052 (2026). https://doi.org/10.1038/s41590-026-02473-y
Schlüsselwörter: Immuntherapie, Zelltechnik, solide Tumoren, Chemotaxis, GPCRs