Clear Sky Science · zh
体内位点特异性工程以重编程T细胞
将身体变成自身的细胞工厂
医生现在可以通过向患者输注定制的免疫细胞——称为CAR T细胞——治愈某些血液癌症,但这些强效疗法的制造过程既缓慢又极其昂贵。本文探讨了另一种思路:与其在工厂里制造这些细胞药物再回输,不如直接在体内对人的T细胞进行重编程?研究者描述了一种在携带人体免疫系统的小鼠体内实现该目标的方法,指向未来可能更快、更便宜且更普及的癌症疗法。
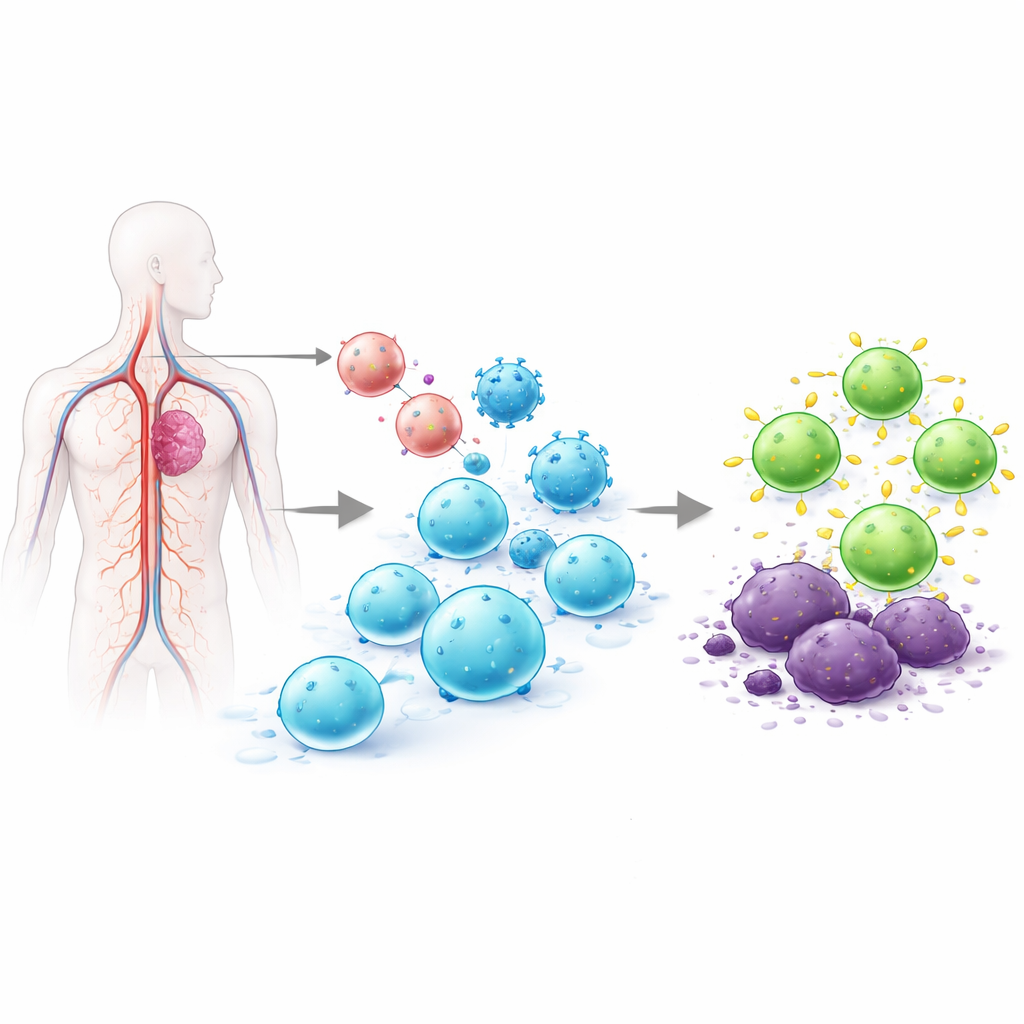
为何重编程T细胞如此困难
T细胞是能够追踪并消灭被感染或癌变细胞的白细胞。在现有获批的CAR T疗法中,T细胞被从患者体内提取,在实验室中通过基因改造加入识别肿瘤的受体、扩增到大量,然后再回输体内。这个体外流程可能耗时数周、花费数十万美金,并且产生的细胞制剂差异很大。早期尝试在体内直接编程T细胞的方法依赖于会在基因组随机插入DNA的病毒载体,或依赖短暂存在的信使RNA。随机插入带来安全隐患,而短暂表达可能无法持续抑制癌症。本文团队的目标是同时解决这两类问题:将CAR精确插入T细胞的自然控制开关中,从而仅改变T细胞,并使新受体以更受控、更持久的方式表达。
血流中实现精确编辑的双工具系统
研究者创造了一个“两载体”递送系统,使两种工具在体内协同工作。一种工具称为包膜化递送载体,携带经过编程的CRISPR–Cas9基因编辑蛋白,用于在T细胞DNA的特定位点切割。第二种工具由腺相关病毒(AAV)构建,携带一段匹配的DNA模板,模板中含有CAR蓝本,并由引导序列包 flank 指引进入所选插入位点——即T细胞受体基因中称为TRAC的区域。当两者同时进入同一细胞时,切口通过以模板为模板的修复被修补,从而整齐地将无启动子的CAR盒插入到受TRAC自然开/关控制的位点下。在体外人体T细胞的试管实验中,这种配对产生了大量精确编辑的细胞,并且研究者展示了被编辑的T细胞能够高效杀死B细胞白血病细胞。
设计递送载体以命中T细胞并避开错误靶标
在活体中安全递送这些基因工具比在培养皿中困难得多,因为血液中存在抗体和许多必须避免的其他细胞类型。为克服这一点,团队进化出一种AAV衣壳变体,称为AAV-hT7,它在有人血清存在时仍能保持活性,并且偏好进入人类T细胞而非干细胞或癌细胞。通过CRISPR筛选,他们发现一种称为CD7的表面蛋白显著影响该载体进入T细胞的效率,帮助解释其特异性。同时,他们通过突变其常规病毒衣壳使其不再能结合原有受体,并用识别T细胞标志CD3的抗体片段对其进行装饰,重新设计了包膜化递送载体。这种双重靶向策略不仅将颗粒导向T细胞,还短暂激活了它们,促使更多细胞进入有利于精确DNA修复和CAR盒稳定插入的细胞周期状态。
体内产生的CAR T细胞可控制白血病、多发性骨髓瘤和实体瘤
配备了优化后的组合——CD3靶向颗粒加上AAV-hT7 DNA载体——科学家在多种人源化小鼠模型中测试了该方法。在移植有人类血细胞的小鼠中,单次静脉注射这两种载体可将大约五分之一的T细胞在预定的TRAC位点转化为CAR T细胞,并清除正常B细胞,这是抗CD19 CAR活性的标志。在侵袭性白血病模型中,这一体内生成的CAR T群体快速扩增、清除肿瘤,并常常在后续肿瘤再挑战中提供保护。与体内慢病毒CAR递送直接比较时,TRAC靶向方法在每个细胞上产生更均一的CAR表达、更快的T细胞扩增以及更好的整体肿瘤控制。团队随后将CAR设计替换为针对骨髓瘤标志BCMA或存在于多种实体瘤中的蛋白B7-H3,并在多发性骨髓瘤和肉瘤模型中显示出强烈反应,包括在许多动物中在再挑战后仍保持持久控制。
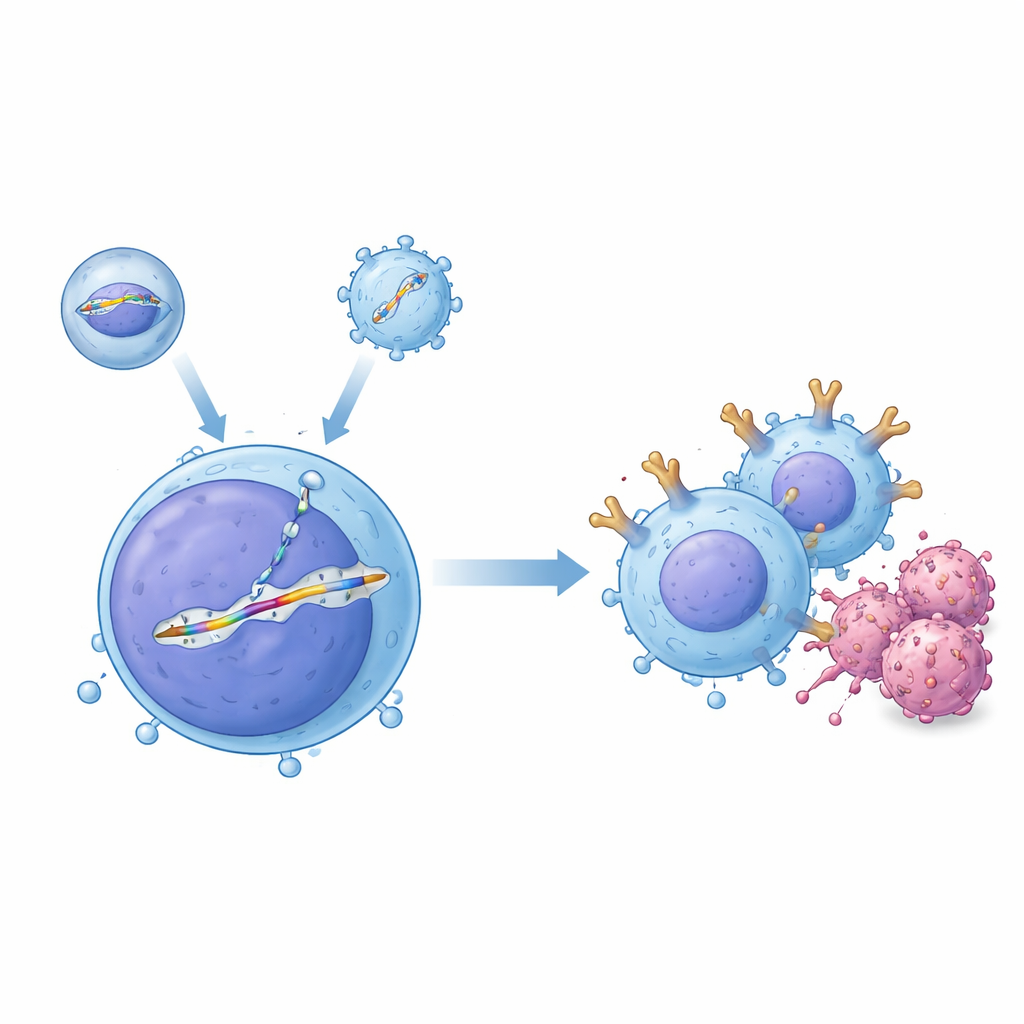
这对未来癌症护理意味着什么
对非专业读者而言,关键的信息是作者已将身体自身变成了可编程的设计免疫细胞工厂。通过共同递送CRISPR装置和精心设计的DNA模板,并且仅将两者定向至T细胞,他们在活体动物内实现了对人T细胞的精确、稳定“重布线”。这些新产生的CAR T细胞在多个癌症模型中的表现与或优于当前体外培养的版本。尽管要证明安全性、控制剂量并实现向人体转化仍有大量工作,但这项研究为推出无需将细胞送往工厂即可指示患者自身免疫系统对抗血液癌症——并可能对某些实体瘤有效——的现成注射剂勾画了一条现实可行的路径。
引用: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
关键词: CAR T细胞, 体内基因编辑, CRISPR, 癌症免疫疗法, 病毒载体