Clear Sky Science · fr
Ingénierie in vivo spécifique au site pour reprogrammer les lymphocytes T
Transformer le corps en sa propre usine à cellules
Les médecins peuvent désormais guérir certains cancers du sang en administrant aux patients des cellules immunitaires sur mesure appelées cellules CAR T, mais ces traitements puissants sont lents et extrêmement coûteux à produire. Cette étude explore une autre idée : au lieu de fabriquer ces médicaments cellulaires en usine puis de les réinjecter, que se passerait-il si l’on pouvait reprogrammer directement les propres lymphocytes T d’une personne à l’intérieur du corps ? Les chercheurs décrivent une méthode pour faire exactement cela chez des souris dotées d’un système immunitaire humain, ouvrant la voie à des thérapies anticancer qui pourraient un jour être plus rapides, moins chères et plus largement accessibles.
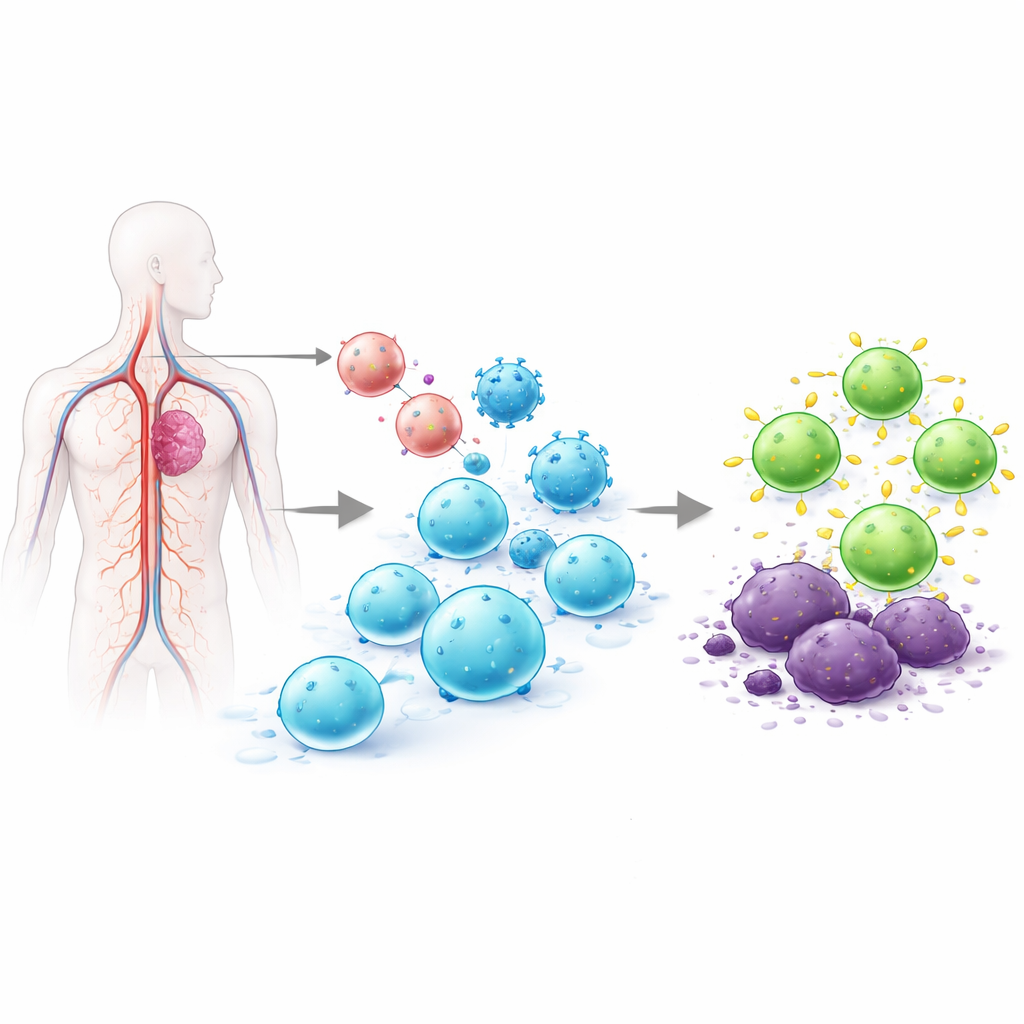
Pourquoi reprogrammer les lymphocytes T est si difficile
Les lymphocytes T sont des globules blancs capables de traquer les cellules infectées ou cancéreuses. Dans les thérapies CAR T approuvées aujourd’hui, les lymphocytes T sont prélevés chez le patient, génétiquement modifiés en laboratoire pour porter un récepteur ciblant la tumeur, amplifiés en grand nombre, puis réinjectés. Ce processus ex vivo peut prendre des semaines, coûter des centaines de milliers de dollars et produire des lots cellulaires variables. Les tentatives antérieures pour programmer les lymphocytes T directement dans l’organisme s’appuyaient sur des vecteurs viraux qui insèrent l’ADN à des positions aléatoires dans le génome, ou sur de l’ARN messager qui disparaît au bout de peu de temps. L’insertion aléatoire soulève des problèmes de sécurité, et une expression de courte durée peut ne pas suffire à contrôler les cancers. L’équipe derrière cet article a cherché à résoudre ces deux problèmes à la fois en insérant le CAR précisément dans un interrupteur de contrôle naturel des T — de sorte que seuls les lymphocytes T seraient modifiés et que le nouveau récepteur serait exprimé de manière plus régulée et durable.
Un système à deux outils pour une édition de précision dans le courant sanguin
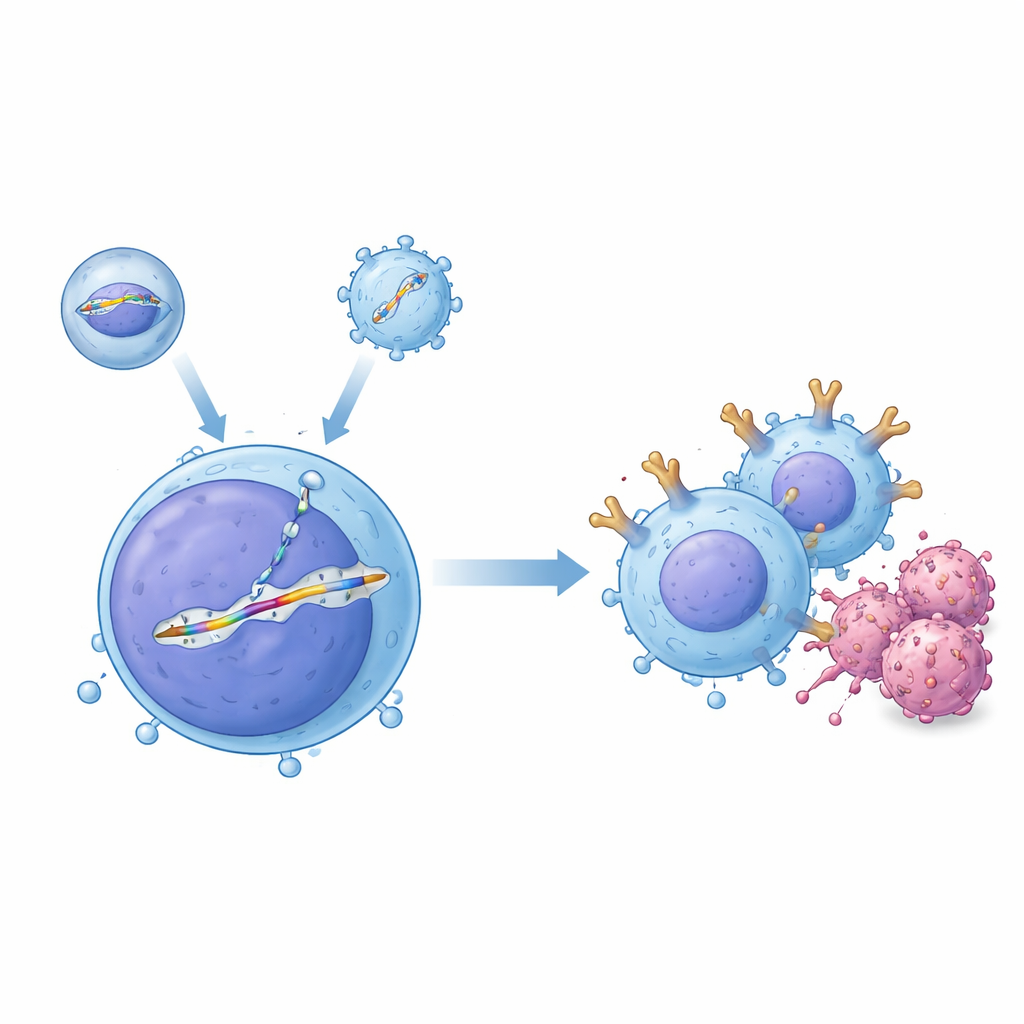
Les chercheurs ont créé un système de livraison « à deux vecteurs » qui coopère à l’intérieur du corps. Un outil, appelé véhicule de livraison enveloppé, apporte la protéine d’édition génique CRISPR–Cas9 programmée pour couper un site spécifique de l’ADN des lymphocytes T. Le second outil, construit à partir d’un adénovirus associé (AAV), porte un brin d’ADN matrice contenant le plan du CAR encadré par des séquences qui guident son insertion dans l’emplacement choisi, une région du gène du récepteur des T connue sous le nom de TRAC. Lorsque les deux arrivent dans la même cellule, la cassure est réparée par copie à partir du modèle, insérant proprement une cassette CAR sans promoteur sous le contrôle de l’interrupteur naturel on/off de TRAC. Dans des expériences en tube avec des lymphocytes T humains, cette combinaison a produit de fortes proportions de cellules précisément éditées, et les auteurs ont montré que ces lymphocytes T modifiés pouvaient tuer efficacement des cellules de leucémie B.
Concevoir des véhicules de livraison qui ciblent les T et évitent les mauvaises cibles
Livrer ces outils génétiques en toute sécurité dans un organisme vivant est bien plus difficile que dans une culture, car le sang contient des anticorps et de nombreux autres types cellulaires à éviter. Pour surmonter cela, l’équipe a fait évoluer une variante de capsid AAV, nommée AAV-hT7, qui reste active même en présence de sérum humain et préfère les lymphocytes T humains aux cellules souches et aux cellules cancéreuses. À l’aide d’écrans CRISPR, ils ont découvert qu’une protéine de surface appelée CD7 influence fortement l’entrée de ce vecteur dans les lymphocytes T, ce qui aide à expliquer sa spécificité. Parallèlement, ils ont redessiné leur véhicule de livraison enveloppé en mutant sa coque virale habituelle afin qu’il ne puisse plus se lier à ses récepteurs habituels, puis en le décorant d’un fragment d’anticorps reconnaissant CD3, une marque des lymphocytes T. Cette stratégie à double ciblage a non seulement orienté les particules vers les lymphocytes T, mais les a également activés brièvement, incitant davantage d’entre eux à entrer dans un état du cycle cellulaire favorable à une réparation d’ADN précise et à une insertion stable de la cassette CAR.
Des cellules CAR T produites in vivo qui contrôlent la leucémie, le myélome et des tumeurs solides
Munis de leur paire optimisée — particules ciblant CD3 plus le transporteur d’ADN AAV-hT7 — les scientifiques ont testé l’approche dans plusieurs modèles murins humanisés. Chez des souris greffées de cellules sanguines humaines, une seule dose intraveineuse des deux vecteurs a converti jusqu’à environ un lymphocyte T sur cinq en cellules CAR T à l’emplacement TRAC souhaité et a éliminé les cellules B normales, un marqueur d’activité des CAR anti-CD19. Dans des modèles de leucémie agressive, cette population de CAR T générée in vivo s’est rapidement étendue, a éradiqué les tumeurs et a souvent protégé contre un nouveau défi tumoral ultérieur. Comparée tête-à-tête à une livraison CAR par lentivirus in vivo, la méthode ciblant TRAC a produit des niveaux de CAR plus uniformes par cellule, une expansion des T plus rapide et un meilleur contrôle global des tumeurs. L’équipe a ensuite testé des constructions CAR ciblant BCMA, un marqueur du myélome, ou B7-H3, une protéine présente sur de nombreuses tumeurs solides, et a montré des réponses robustes dans des modèles de myélome multiple et de sarcome, y compris un contrôle durable après rechallenge chez de nombreux animaux.
Ce que cela pourrait signifier pour les soins du cancer à l’avenir
Pour le grand public, le message clé est que les auteurs ont transformé le corps lui‑même en une usine programmable de cellules immunitaires sur mesure. En délivrant ensemble la machinerie CRISPR et un modèle d’ADN soigneusement conçu, et en orientant les deux uniquement vers les lymphocytes T, ils ont obtenu une « reprogrammation » précise et stable des lymphocytes T humains à l’intérieur d’animaux vivants. Ces cellules CAR nouvellement produites se sont comportées comme — ou mieux que — les versions actuelles cultivées en laboratoire dans plusieurs modèles tumoraux. Bien que de nombreux travaux restent à faire pour prouver la sécurité, contrôler la posologie et traduire la méthode chez l’humain, l’étude trace une voie réaliste vers des injections prêtes à l’emploi qui instruisent le système immunitaire du patient à combattre les cancers du sang — et potentiellement certaines tumeurs solides — sans jamais avoir à envoyer leurs cellules en usine.
Citation: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
Mots-clés: Cellules CAR T, édition génomique in vivo, CRISPR, immunothérapie du cancer, vecteurs viraux