Clear Sky Science · ru
Ин виво таргетная инженерия для перепрограммирования Т‑лимфоцитов
Превращение организма в собственную клеточную фабрику
Врачи уже умеют излечивать некоторые заболевания крови, вводя пациентам индивидуально созданные иммунные клетки — CAR‑T‑клетки, но эти мощные терапии медленны и чрезвычайно дороги в производстве. В этом исследовании рассматривается другая идея: вместо того чтобы выращивать такие клеточные лекарства на фабрике и затем вводить их обратно, что если перепрограммировать собственные Т‑клетки человека прямо внутри организма? Авторы описывают способ сделать это у мышей с человеческой иммунной системой, что указывает путь к онкотерапиям, которые однажды могут стать быстрее, дешевле и доступнее.
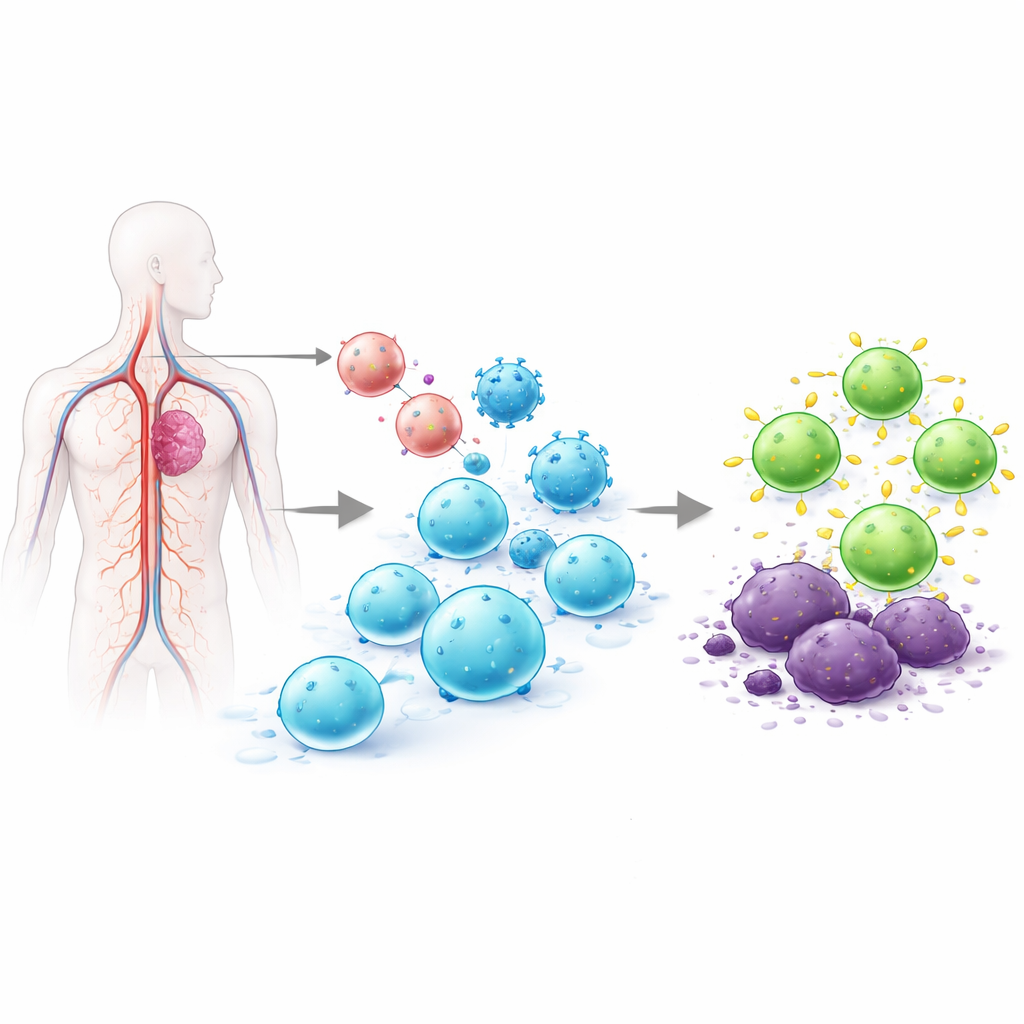
Почему перепрограммировать Т‑клетки так трудно
Т‑лимфоциты — это лейкоциты, которые способны находить инфицированные или раковые клетки. В одобренных сегодня CAR‑T‑терапиях Т‑клетки извлекают у пациента, генетически модифицируют в лаборатории, чтобы они несли рецептор, нацеленный на опухоль, увеличивают их количество и затем вводят обратно. Этот экс-виво процесс может занимать недели, стоить сотни тысяч долларов и давать непостоянные клеточные продукты. Ранние попытки программировать Т‑клетки прямо в организме опирались на вирусные векторы, вставляющие ДНК в случайные позиции генома, или на матричную РНК, которая исчезает через короткое время. Случайная вставка вызывает вопросы безопасности, а недолговременная экспрессия может не удерживать рак под контролем. Команда авторов этой работы поставила цель решить обе проблемы одновременно, вставив CAR точно в естественный контрольный переключатель Т‑клетки, так чтобы изменялись только Т‑клетки, а новый рецептор экспрессировался более регулируемо и устойчиво.
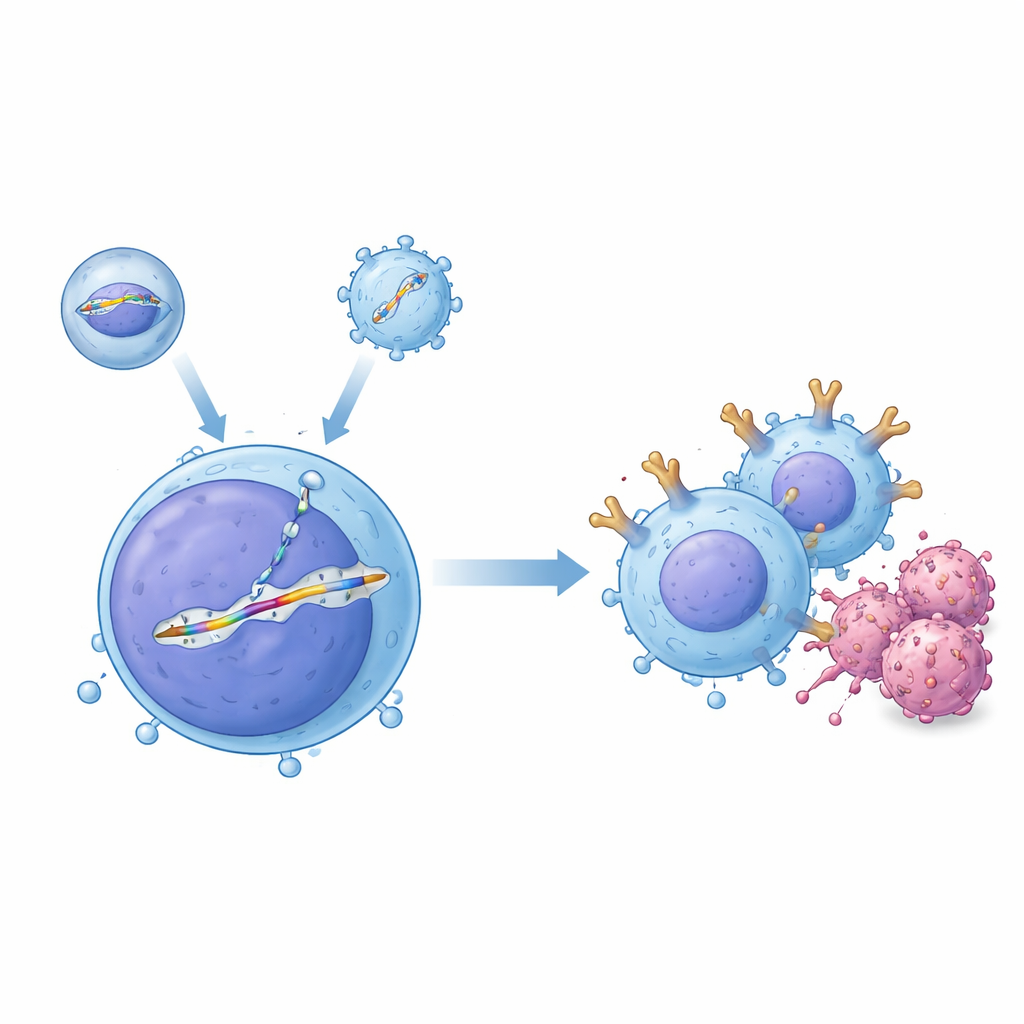
Система из двух инструментов для прецизионного редактирования в кровотоке
Исследователи создали «двухвекторную» систему доставки, где оба компонента работают совместно в организме. Один инструмент, названный оболочечным переносчиком, доставляет белок редактирования генома CRISPR–Cas9, запрограммированный на разрез конкретного участка ДНК Т‑клетки. Второй инструмент, созданный на основе адено‑ассоциированного вируса, несёт соответствующий ДНК‑шаблон, содержащий чертеж CAR, окружённый последовательностями, которые направляют его в выбранное место — участок гена T‑клеточного рецептора, известный как TRAC. Когда оба компонента попадают в одну и ту же клетку, разрез восстанавливается копированием с шаблона, аккуратно вставляя промотор‑независимую кассету CAR под управление естественного переключателя TRAC. В опытных экспериментах с человеческими Т‑клетками в пробирке такое сочетание давало большие доли точно отредактированных клеток, и авторы показали, что отредактированные Т‑клетки эффективно уничтожают клетки B‑клеточной лейкемии.
Проектирование носителей доставки, которые попадают в Т‑клетки — и обходят нежелательные цели
Доставить эти генетические инструменты безопасно в живом организме гораздо сложнее, чем в культуре, потому что в крови есть антитела и множество других типов клеток, которых нужно избегать. Чтобы преодолеть это, команда эволюционировала вариант капсида AAV, названный AAV‑hT7, который остаётся активным даже в присутствии человеческой сыворотки и предпочитает человеческие Т‑клетки по сравнению со стволовыми и раковыми клетками. С помощью CRISPR‑скринов они обнаружили, что поверхностный белок CD7 сильно влияет на способность этого вектора входить в Т‑клетки, что помогает объяснить его специфичность. Параллельно они переработали свой оболочечный переносчик, мутировав его обычный вирусный «покров», чтобы он больше не связывался со своими привычными рецепторами, а затем украсили его фрагментом антитела, распознающим CD3 — маркер Т‑клеток. Эта стратегия с двойной наводкой не только направляла частицы к Т‑клеткам, но и кратковременно активировала их, подталкивая больше клеток в фазу клеточного цикла, благоприятную для точного ремонта ДНК и стабильной вставки кассеты CAR.
In vivo CAR‑T‑клетки, контролирующие лейкоз, миелому и солидные опухоли
Вооружившись оптимизированной парой — частицами, нацеленными на CD3, и ДНК‑носителем AAV‑hT7 — учёные протестировали подход в нескольких моделях гуманизированных мышей. У мышей, пересаженных человеческими кровяными клетками, однократная внутривенная доза двух векторов преобразовывала до примерно одной из пяти Т‑клеток в CAR‑T‑клетки в желаемом месте TRAC и уничтожала нормальные B‑клетки, что является признаком активности анти‑CD19 CAR. В агрессивных моделях лейкемии популяция CAR‑T‑клеток, созданная in vivo, быстро расширялась, очищала опухоли и часто защищала от повторного введения опухоли. В сравнении с in vivo доставкой через лентивирус метод, нацеленный на TRAC, давал более однородный уровень CAR на каждой клетке, более быстрое расширение Т‑клеток и лучшее общее подавление опухоли. Затем команда заменила конструкции CAR на нацеленные против BCMA (маркер миеломы) или B7‑H3 (белок, обнаруживаемый на многих солидных опухолях) и показала сильные ответы в моделях множественной миеломы и саркомы, включая стойкий контроль после повторного введения опухоли у многих животных.
Что это может означать для будущей помощи при раке
Для неспециалистов главное: авторы превратили сам организм в программируемую фабрику по созданию дизайнерских иммунных клеток. Доставив компоненты CRISPR и тщательно разработанный ДНК‑шаблон вместе, и направив оба только в Т‑клетки, они добились прецизионного, стабильного «перепрограммирования» человеческих Т‑клеток внутри живых животных. Эти новосозданные CAR‑T‑клетки вели себя не хуже, а иногда и лучше, чем нынешние лабораторно выращенные версии в нескольких онкомоделях. Хотя ещё предстоит многое сделать, чтобы доказать безопасность, контролировать дозирование и перенести метод к человеку, исследование описывает реалистичный путь к готовым инъекциям, которые инструктируют собственную иммунную систему пациента бороться с кровяными онкозаболеваниями — и, возможно, с некоторыми солидными опухолями — без необходимости отправлять клетки на фабрику.
Цитирование: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
Ключевые слова: CAR-Т‑клетки, редактирование генов in vivo, CRISPR, иммунотерапия рака, вирусные векторы