Clear Sky Science · pt
Engenharia in vivo específica de sítio para reprogramar células T
Transformando o Corpo em Sua Própria Fábrica de Células
Médicos já conseguem curar alguns cânceres hematológicos ao administrar aos pacientes células imunes personalizadas chamadas células CAR T, mas esses tratamentos poderosos são lentos e extremamente caros de fabricar. Este estudo explora uma ideia diferente: em vez de fabricar esses medicamentos celulares numa fábrica e reinfundí‑los, e se pudéssemos reprogramar as próprias células T de uma pessoa diretamente dentro do corpo? Os pesquisadores descrevem uma forma de fazer exatamente isso em camundongos com sistemas imunes humanos, apontando para terapias contra o câncer que, no futuro, podem ser mais rápidas, baratas e amplamente acessíveis.
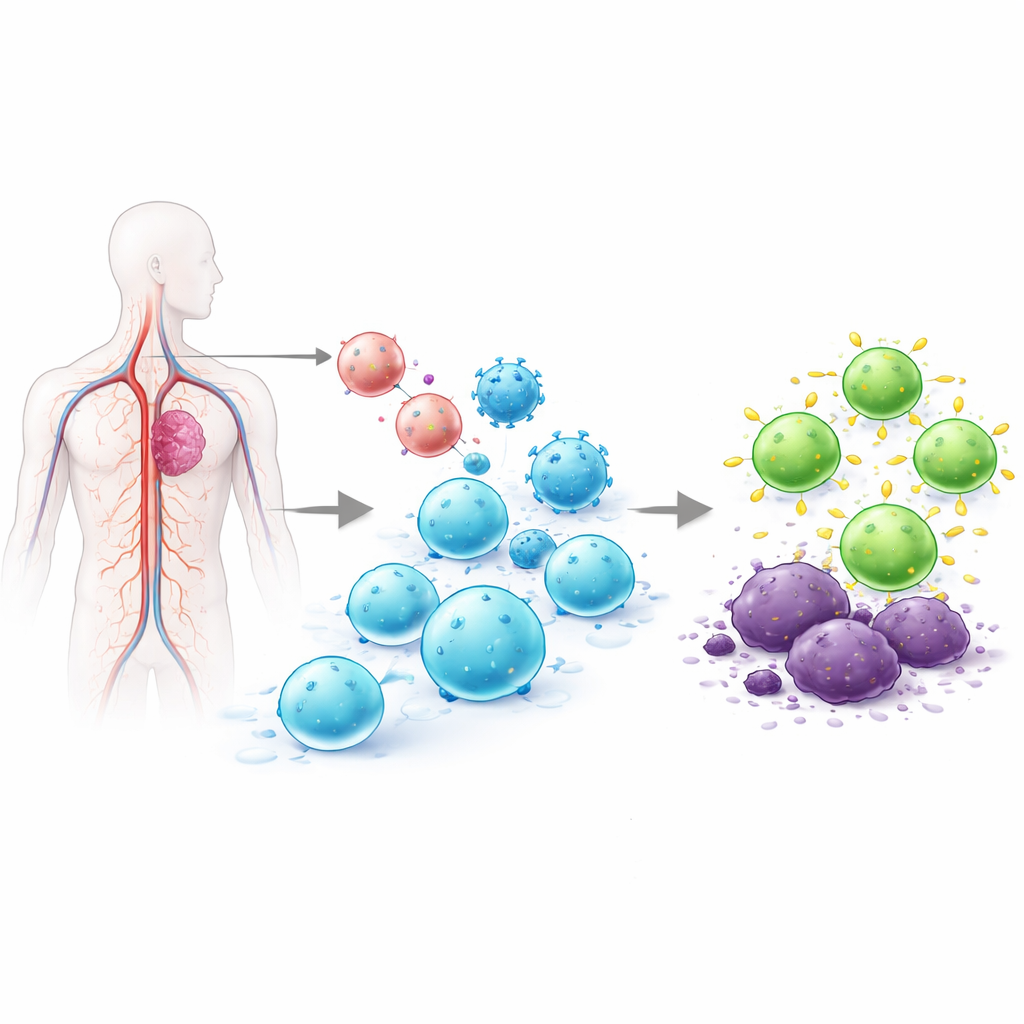
Por Que Reprogramar Células T é Tão Difícil
As células T são glóbulos brancos que podem localizar células infectadas ou cancerosas. Nas terapias CAR T aprovadas hoje, as células T são retiradas do paciente, alteradas geneticamente em laboratório para portar um receptor que mira no tumor, expandidas em grande número e então reinfundidas. Esse processo ex vivo pode levar semanas, custar centenas de milhares de dólares e produzir produtos celulares com variabilidade. Tentativas anteriores de programar células T diretamente no corpo dependeram de vetores virais que inserem DNA em posições aleatórias no genoma, ou de RNA mensageiro que desaparece após pouco tempo. A inserção aleatória levanta preocupações de segurança, e a expressão de curta duração pode não controlar os cânceres. A equipe por trás deste trabalho buscou resolver ambos os problemas de uma vez, inserindo o CAR precisamente em um interruptor natural de controle das células T, de modo que apenas as células T seriam alteradas e o novo receptor fosse expresso de maneira mais regulada e duradoura.
Um Sistema de Duas Ferramentas para Edição de Precisão na Corrente Sanguínea
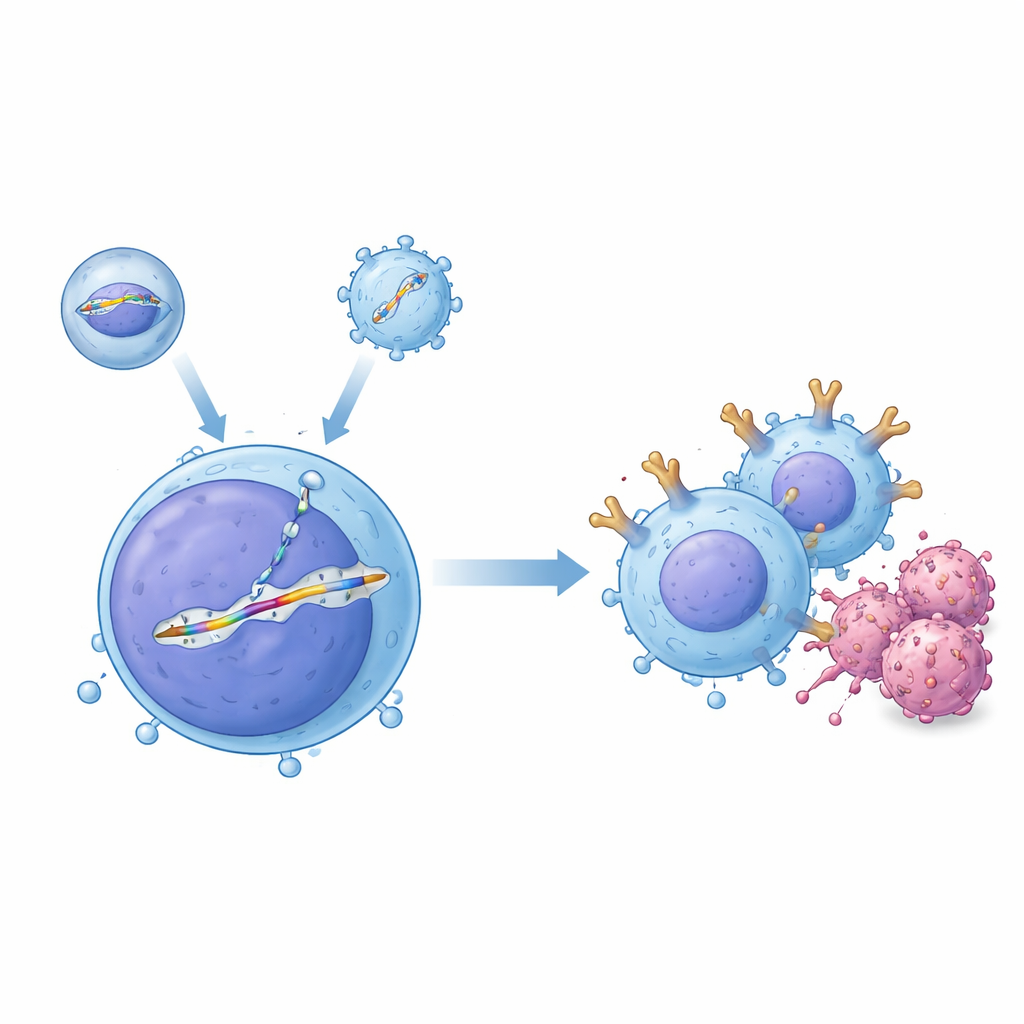
Os pesquisadores criaram um sistema de entrega “de dois vetores” que atuam em conjunto dentro do corpo. Uma ferramenta, chamada veículo de entrega envelopado, traz a proteína de edição gênica CRISPR–Cas9 programada para cortar um sítio específico no DNA da célula T. A segunda ferramenta, construída a partir de um vírus adeno‑associado (AAV), carrega um molde de DNA correspondente que contém o projeto do CAR flanqueado por sequências que o guiam para a posição escolhida, uma região do gene do receptor de células T conhecida como TRAC. Quando ambos chegam à mesma célula, o corte é reparado copiando a partir do molde, inserindo de forma ordenada um cassete CAR sem promotor sob o controle do interruptor natural liga/desliga do TRAC. Em experimentos em tubo com células T humanas, esse pareamento gerou frações significativas de células precisamente editadas, e os pesquisadores mostraram que as células T editadas podiam matar eficientemente células de leucemia de células B.
Projetando Veículos de Entrega para Acertar as Células T—e Não Alvos Errados
Entregar essas ferramentas genéticas com segurança em um corpo vivo é muito mais desafiador do que em uma placa de cultura, porque o sangue contém anticorpos e muitos outros tipos celulares que devem ser evitados. Para superar isso, a equipe evoluiu uma variante de cápside de AAV, apelidada AAV‑hT7, que permanece ativa mesmo na presença de soro humano e prefere células T humanas em relação a células-tronco e células cancerosas. Usando telas CRISPR, eles descobriram que uma proteína de superfície chamada CD7 influencia fortemente a entrada desse vetor nas células T, ajudando a explicar sua especificidade. Paralelamente, eles redesenharam seu veículo de entrega envelopado mutando seu envelope viral normal para que não pudesse mais se ligar a seus receptores usuais, e então o adornaram com um fragmento de anticorpo que reconhece CD3, um marcador característico de células T. Essa estratégia de dupla direcionamento não apenas guiou as partículas para as células T, como também as ativou brevemente, empurrando mais células para um estado do ciclo celular que favorece reparo de DNA preciso e inserção estável do cassete CAR.
Células CAR T Geradas In Vivo que Controlam Leucemia, Mieloma e Tumores Sólidos
Equipados com seu par otimizado — partículas direcionadas a CD3 mais o transportador de DNA AAV-hT7 — os cientistas testaram a abordagem em vários modelos de camundongos humanizados. Em camundongos enxertados com células sanguíneas humanas, uma dose intravenosa única dos dois vetores converteu até aproximadamente uma em cada cinco células T em células CAR T no sítio TRAC desejado e eliminou células B normais, um sinal de função ativa de CAR anti‑CD19. Em modelos de leucemia agressiva, essa população de CAR T gerada in vivo se expandiu rapidamente, eliminou tumores e frequentemente protegeu contra um novo desafio tumoral posterior. Em comparação direta com entrega de CAR por lentivírus in vivo, o método direcionado ao TRAC produziu níveis de CAR mais uniformes em cada célula, expansão de células T mais rápida e melhor controle tumoral geral. A equipe então substituiu os projetos de CAR por alvos para BCMA, um marcador de mieloma, ou B7‑H3, uma proteína encontrada em muitos tumores sólidos, e mostrou respostas robustas em modelos de mieloma múltiplo e sarcoma, incluindo controle duradouro após novo desafio em muitos animais.
O Que Isso Pode Significar para o Cuidado do Câncer no Futuro
Para não especialistas, a mensagem principal é que os autores transformaram o próprio corpo em uma fábrica programável de células imunes sob medida. Ao entregar a maquinaria CRISPR e um molde de DNA cuidadosamente elaborado juntos, e ao direcionar ambos apenas para células T, eles conseguiram um “reconfiguramento” preciso e estável de células T humanas dentro de animais vivos. Essas células CAR recém-geradas se comportaram de forma tão boa quanto ou melhor que as versões cultivadas em laboratório em vários modelos de câncer. Embora ainda seja necessário muito trabalho para comprovar segurança, controlar a dosagem e traduzir para humanos, o estudo delineia um caminho realista rumo a injeções prontas para uso que instruam o próprio sistema imune do paciente a combater cânceres hematológicos — e potencialmente alguns tumores sólidos — sem jamais precisar enviar suas células a uma fábrica.
Citação: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
Palavras-chave: células CAR T, edição gênica in vivo, CRISPR, imunoterapia contra o câncer, vetores virais