Clear Sky Science · it
In vivo site-specific engineering per riprogrammare le cellule T
Trasformare il corpo nella propria fabbrica di cellule
I medici oggi possono curare alcuni tumori del sangue somministrando ai pazienti cellule immunitarie su misura chiamate cellule CAR-T, ma questi trattamenti potenti sono lenti e estremamente costosi da produrre. Questo studio esplora un’idea diversa: invece di costruire questi medicinali cellulari in una fabbrica e poi reinfonderli, cosa succederebbe se potessimo riprogrammare direttamente nel corpo le cellule T di una persona? I ricercatori descrivono un modo per farlo esattamente nei topi con sistemi immunitari umani, indicando terapie antitumorali che un giorno potrebbero essere più rapide, meno costose e più ampiamente accessibili.
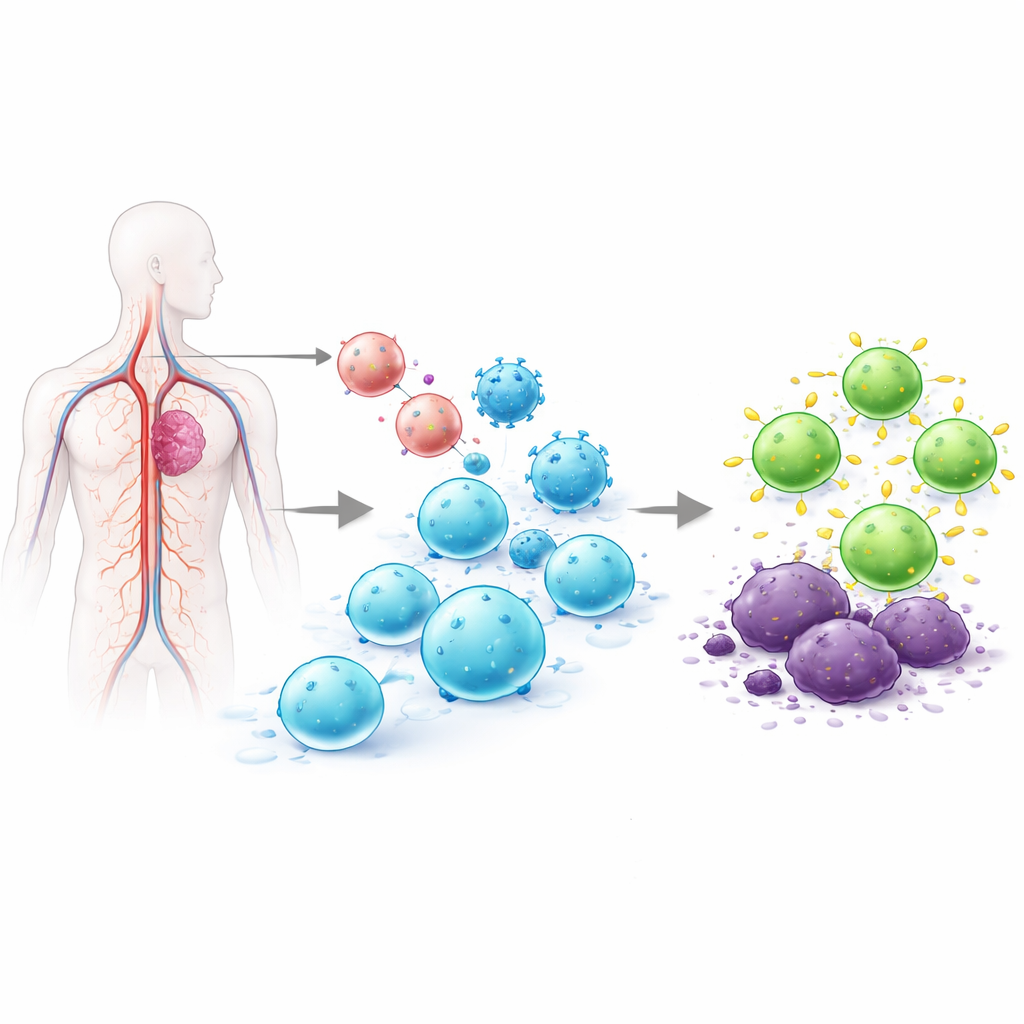
Perché riprogrammare le cellule T è così difficile
Le cellule T sono globuli bianchi che possono individuare cellule infette o cancerose. Nelle terapie CAR-T approvate oggi, le cellule T vengono prelevate dal paziente, alterate geneticamente in laboratorio per esprimere un recettore che riconosce il tumore, amplificate in grandi quantità e quindi reinfuse. Questo processo ex vivo può richiedere settimane, costare centinaia di migliaia di dollari e produrre lotti cellulari variabili. I tentativi precedenti di programmare le cellule T direttamente nell’organismo hanno usato vettori virali che inseriscono DNA in posizioni casuali del genoma, o RNA messaggero che scompare dopo poco tempo. L’inserimento casuale solleva problemi di sicurezza, e un’espressione di breve durata potrebbe non controllare il tumore. Il gruppo dietro questo lavoro ha cercato di risolvere entrambi i problemi inserendo il CAR con precisione in un interruttore di controllo naturale delle cellule T, in modo che solo le cellule T vengano modificate e il nuovo recettore venga espresso in modo più regolato e duraturo.
Un sistema a due strumenti per l’editing di precisione nel flusso sanguigno
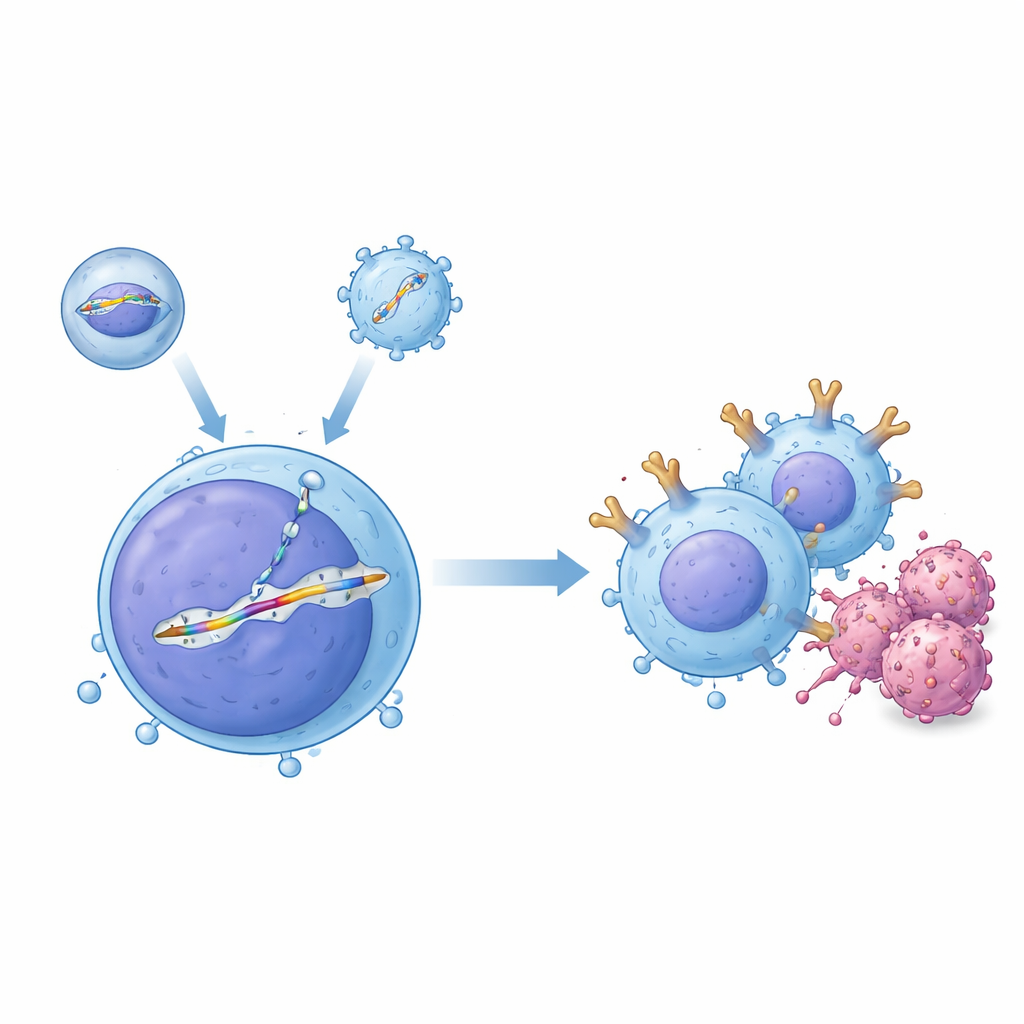
I ricercatori hanno creato un sistema di consegna “a due vettori” che opera in sinergia all’interno dell’organismo. Uno strumento, chiamato veicolo di consegna incapsulato, trasporta la proteina di editing genico CRISPR–Cas9 programmata per tagliare un sito specifico nel DNA delle cellule T. Il secondo, basato su un virus adeno-associato (AAV), porta un modello di DNA corrispondente che contiene il progetto del CAR affiancato da sequenze che guidano il suo inserimento nello slot scelto, una regione del gene del recettore delle cellule T nota come TRAC. Quando entrambi arrivano nella stessa cellula, il taglio viene riparato copiando dal modello, inserendo ordinatamente un cassette CAR priva di promotore sotto il controllo dell’interruttore on/off naturale di TRAC. In esperimenti in provetta con cellule T umane, questa coppia ha generato frazioni significative di cellule precisamente modificate, e gli sperimentatori hanno dimostrato che le cellule T modificate potevano uccidere efficacemente cellule di leucemia B.
Progettare veicoli di consegna che colpiscano le cellule T—e evitino i bersagli sbagliati
Consegnare questi strumenti genetici in modo sicuro in un organismo vivente è molto più impegnativo che in una coltura, perché il sangue contiene anticorpi e molti altri tipi di cellule da evitare. Per superare questo, il gruppo ha evoluto una variante del capsidio AAV, chiamata AAV-hT7, che rimane attiva anche in presenza di siero umano e predilige le cellule T umane rispetto a cellule staminali e cellule tumorali. Tramite schermi CRISPR, hanno scoperto che una proteina di superficie chiamata CD7 influenza fortemente l’efficienza con cui questo vettore entra nelle cellule T, contribuendo a spiegare la sua specificità. Parallelamente, hanno riprogettato il loro veicolo di consegna incapsulato mutando il suo rivestimento virale normale in modo che non potesse più legarsi ai recettori abituali, quindi lo hanno decorato con un frammento di anticorpo che riconosce CD3, un marcatore delle cellule T. Questa strategia a doppio bersaglio non solo ha diretto le particelle verso le cellule T ma le ha anche attivate brevemente, spingendo molte di esse in uno stato del ciclo cellulare che favorisce una riparazione del DNA precisa e l’inserimento stabile della cassette CAR.
Cellule CAR-T generate in vivo che controllano leucemia, mieloma e tumori solidi
Armati della coppia ottimizzata—particelle dirette a CD3 più il vettore AAV-hT7 portatore di DNA—gli scienziati hanno testato l’approccio in diversi modelli murini umanizzati. In topi trapiantati con cellule del sangue umano, una singola somministrazione endovenosa dei due vettori ha convertito fino a circa una cellula su cinque in cellule CAR-T nel sito TRAC desiderato e ha eliminato le cellule B normali, un segno distintivo della funzione anti-CD19 CAR attiva. Nei modelli di leucemia aggressiva, questa popolazione di CAR-T generata in vivo si è espansa rapidamente, ha eliminato i tumori e spesso ha protetto da una successiva nuova sfida tumorale. Confrontato testa a testa con la consegna di CAR tramite lentivirus in vivo, il metodo mirato a TRAC ha prodotto livelli di CAR più uniformi su ciascuna cellula, un’espansione più rapida delle cellule T e un controllo tumorale complessivamente migliore. Il gruppo ha quindi impiegato progetti di CAR che prendono di mira BCMA, un marcatore del mieloma, o B7‑H3, una proteina presente in molti tumori solidi, mostrando risposte robuste in modelli di mieloma multiplo e sarcoma, incluso un controllo duraturo dopo una nuova sfida in molti animali.
Cosa potrebbe significare per la cura del cancro in futuro
Per i non specialisti, il messaggio chiave è che gli autori hanno trasformato il corpo stesso in una fabbrica programmabile di cellule immunitarie su misura. Consegnando insieme la macchina CRISPR e un modello di DNA accuratamente progettato, e indirizzando entrambi solo nelle cellule T, hanno realizzato una “ricablaggio” preciso e stabile delle cellule T umane all’interno di animali viventi. Queste cellule CAR-T appena generate si sono comportate in molti modelli tumorali in modo paragonabile o migliore rispetto alle versioni cresciute in laboratorio. Sebbene rimangano molti lavori per dimostrare sicurezza, controllo delle dosi e traduzione nell’uomo, lo studio traccia un percorso realistico verso iniezioni pronte all’uso che istruiscono il sistema immunitario del paziente a combattere i tumori del sangue—e potenzialmente alcuni tumori solidi—senza dover mai spedire le loro cellule in una fabbrica.
Citazione: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
Parole chiave: Cellule CAR-T, editing genico in vivo, CRISPR, immunoterapia del cancro, vettori virali