Clear Sky Science · ar
الهندسة الموجهة في الجسم لإعادة برمجة الخلايا التائية
تحويل الجسم إلى مصنع خلوي ذاتي
بات الأطباء قادِرين الآن على علاج بعض سرطانات الدم بمنح المرضى خلايا مناعية مُصممة خصيصًا تُعرف بخلايا CAR T، لكن هذه العلاجات الفعّالة بطيئة ومكلفة للغاية في التصنيع. تستكشف هذه الدراسة فكرة مختلفة: بدلًا من تصنيع هذه الأدوية الخلوية في مصنع وإعادتها إلى المريض، ماذا لو أمكننا إعادة برمجة الخلايا التائية للشخص مباشرة داخل الجسم؟ يصف الباحثون هنا طريقة لتحقيق ذلك في فئران ذات جهاز مناعي بشري، مما يشير إلى علاجات سرطانية قد تكون يومًا ما أسرع وأرخص وأكثر توفّرًا على نطاق واسع.
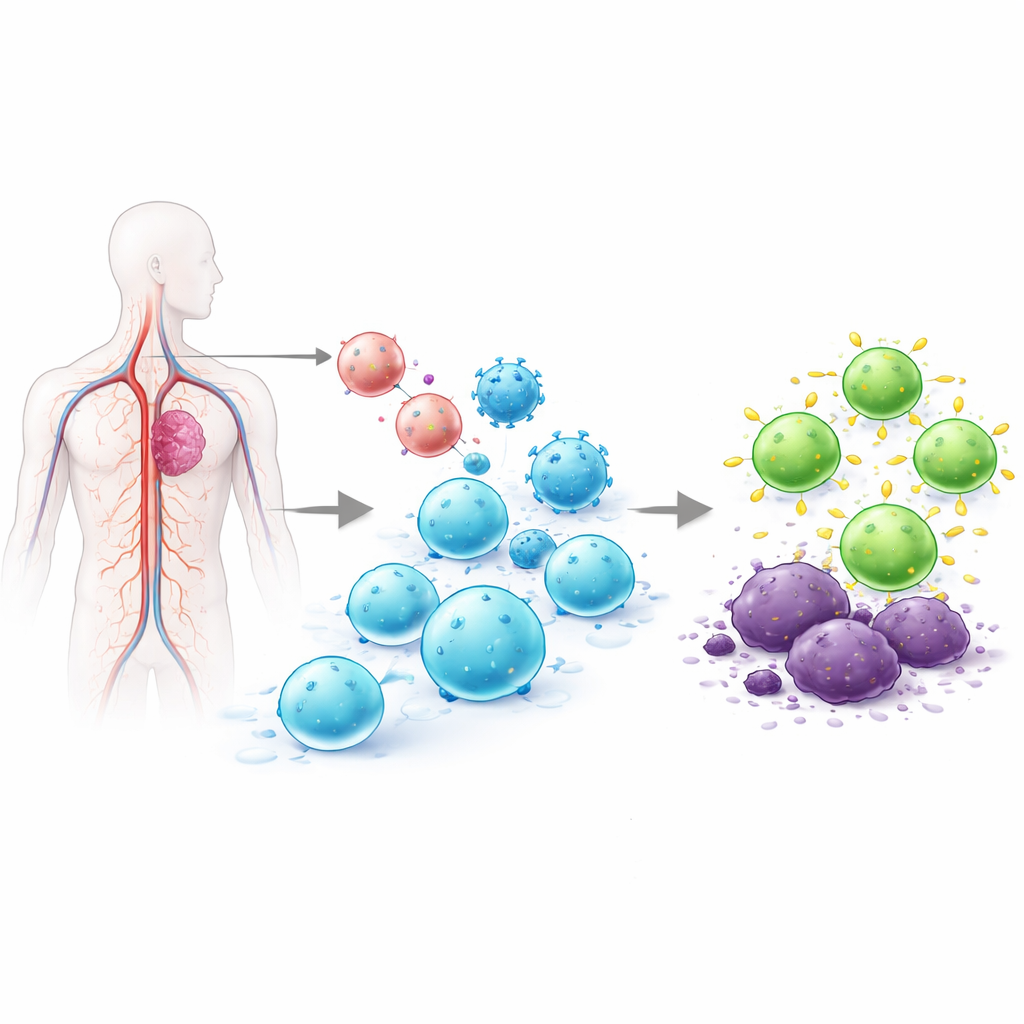
لماذا إعادة برمجة الخلايا التائية صعبة للغاية
الخلايا التائية هي خلايا دم بيضاء يمكنها اصطياد الخلايا المصابة أو السرطانية. في علاجات CAR T المعتمدة حاليًا، تُستخرج الخلايا التائية من المريض، وتُعدّل وراثيًا في المختبر لحمل مستقبل يستهدف الورم، ثم تُنمّى بكميات كبيرة وتُعاد إلى المريض. قد تستغرق هذه العملية خارج الجسم أسابيع، وتكلّف مئات الآلاف من الدولارات، وتنتج منتجات خلوية متغيرة الجودة. اعتمدت محاولات سابقة لبرمجة الخلايا التائية داخل الجسم على ناقلات فيروسية تُدخل الحمض النووي في مواقع عشوائية في الجينوم، أو على حمض ريبوزي مرسال يختفي بعد وقت قصير. الإدخال العشوائي يثير مخاوف تتعلق بالسلامة، والتعبير قصير الأمد قد لا يكبح السرطان. سعى فريق هذه الورقة إلى حل هاتين المشكلتين معًا عن طريق إدخال CAR بدقة في مفتاح تحكم طبيعي للخلايا التائية، بحيث تُعدّل الخلايا التائية وحدها ويُعبّر عن المستقبل الجديد بطريقة أكثر تنظيمًا وديمومة.
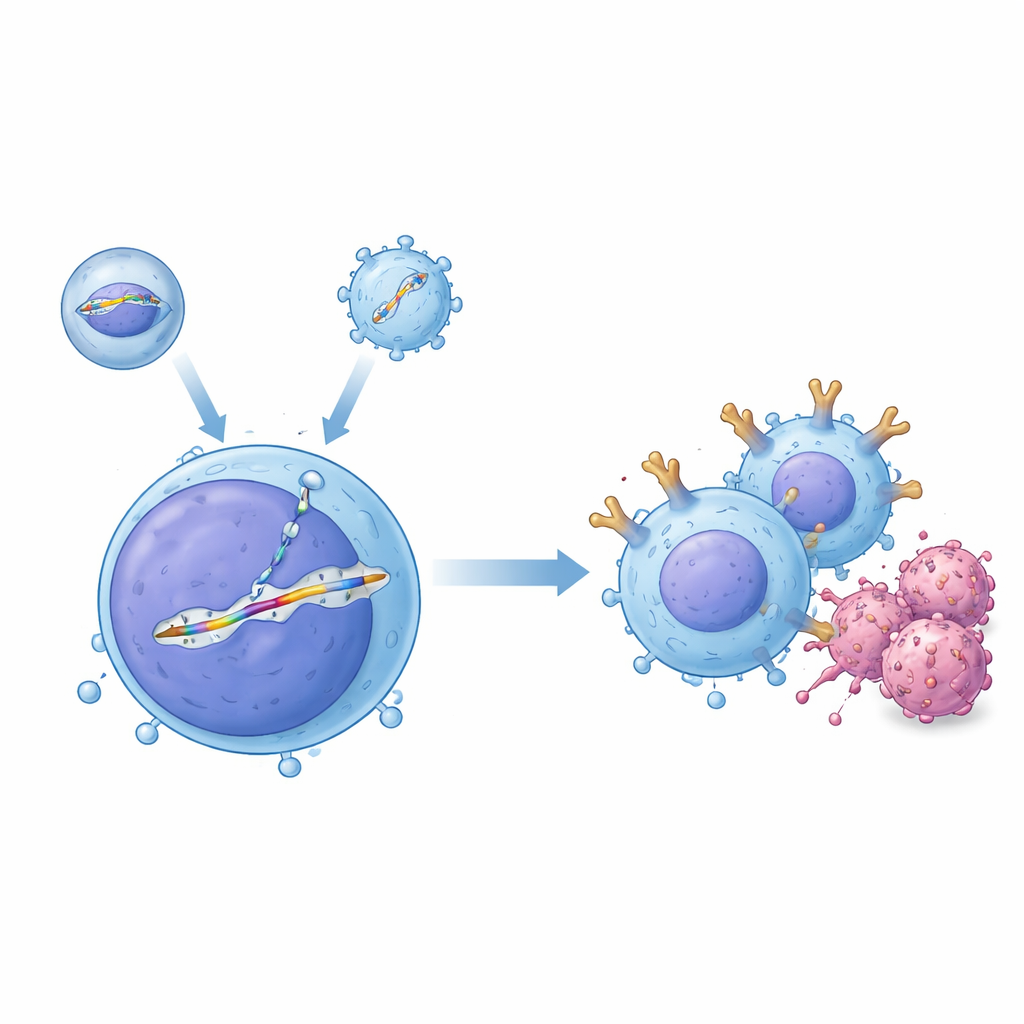
نظام بأداتين لتحرير دقيق في مجرى الدم
أنشأ الباحثون نظام توصيل «ثنائي الناقل» يعمل معًا داخل الجسم. الأداة الأولى، المسماة مركبة توصيل مغلفة، تُدخل بروتين تحرير الجينات CRISPR–Cas9 المبرمج لقطع موقع محدد في حمض الخلية التائية. الأداة الثانية، المبنية من فيروسٍ شبيه بنقصي التغلب على شبيهة للفيروس الأدينوي المرتبط (AAV)، تحمل قالب DNA مطابقًا يتضمن مخطط CAR محاطًا بتتابعات ترشده نحو الفتحة المختارة، وهي منطقة في جين مستقبل الخلية التائية تُعرف باسم TRAC. عندما يصل الاثنان إلى نفس الخلية، يُصلَح القطع عن طريق النسخ من القالب، مما يُدخِل بكفاءة كاسيت CAR بلا مُحفز تحت سيطرة مفتاح التشغيل/الإيقاف الطبيعي لـTRAC. في تجارب أنبوبية على خلايا تائية بشرية، أنتج هذا الاقتران نسبًا كبيرة من الخلايا المعدّلة بدقة، وأظهر الباحثون أن الخلايا التائية المعدّلة يمكنها قتل خلايا سرطان الدم من خلايا B بكفاءة.
تصميم مركبات توصيل تستهدف الخلايا التائية وتتفادى الأهداف الخاطئة
توصيل هذه الأدوات الجينية بأمان داخل جسم حي أشد تعقيدًا من العمل في طبق، لأن الدم يحتوي على أجسام مضادة وأنواع خلايا عديدة يجب تجنّبها. لتجاوز ذلك، طوّر الفريق متغيرًا لقشرة AAV أطلقوا عليه اسم AAV-hT7، يبقى نشطًا حتى في وجود مصل بشري ويفضل الخلايا التائية البشرية على الخلايا الجذعية وخلايا السرطان. باستخدام شاشات CRISPR، وجدوا أن بروتين سطحيًا يُدعى CD7 يؤثر بشدة على مدى دخول هذا الناقل إلى الخلايا التائية، وهو ما يفسّر تخصصه. بالتوازي، أعادوا تصميم مركبة التوصيل المغلفة عن طريق طَفْر غلافها الفيروسي الطبيعي حتى لا يعود بإمكانه الارتباط بمستقبلاته الاعتيادية، ثم زَيَّنوها بشظية من جسم مضاد تتعرف إلى CD3، وهو علامة مميزة للخلايا التائية. هذه الاستراتيجية ذات الاستهداف المزدوج لم تُرْشِد الجسيمات نحو الخلايا التائية فحسب، بل قامت أيضًا بتنشيطها قصيرًا، مما دفع عددًا أكبر منها إلى حالة دورة خلوية تُفضّل إصلاح الحمض النووي بدقة وإدخالًا مستقرًا لكاسيت CAR.
خلايا CAR T المنتجة داخل الجسم تسيطر على اللوكيميا والمايلوما والأورام الصلبة
مسلحين بالزوج المحسّن—جسيمات موجهة إلى CD3 بالإضافة إلى ناقل DNA AAV-hT7—اختبر العلماء النهج في عدة نماذج فئران مُشوَّهة بجهاز مناعي بشري. في الفئران المُغرزَة بخلايا دم بشرية، حوّلت جرعة وريدية واحدة من الناقلين ما يصل إلى نحو خُمس الخلايا التائية إلى خلايا CAR T في موقع TRAC المرغوب وأتلفت الخلايا B الطبيعية، وهو علامة مميزة لوظيفة CAR المضاد لـCD19 النشطة. في نماذج اللوكيميا العدوانية، توسّعت مجموعة CAR T المتولّدة داخل الجسم بسرعة، وأزالت الأورام، وغالبًا ما وفّرت حماية ضد إعادة تحدي الورم لاحقًا. بالمقارنة المباشرة مع توصيل CAR بواسطة لنتيفيروس داخل الجسم، أنتجت الطريقة المستهدفة لـTRAC مستويات أكثر تجانسًا من CAR على كل خلية، وتوسعًا أسرع للخلايا التائية، وتحكمًا أفضل في الورم بشكل عام. بعد ذلك استبدل الفريق تصميمات CAR لاستهداف BCMA، علامة المايلوما، أو B7-H3، بروتين موجود على العديد من الأورام الصلبة، وأظهر استجابات قوية في نماذج متعددة للمايلوما والساركومة، بما في ذلك سيطرة دائمة بعد إعادة التحدي في العديد من الحيوانات.
ما الذي قد يعنيه هذا لرعاية السرطان في المستقبل
للغير متخصصين، الرسالة الأساسية أن المؤلفين حوّلوا الجسم نفسه إلى مصنع مبرمج للخلايا المناعية المصممة. من خلال توصيل آليات كريسبر وقالب DNA مصمّم بعناية معًا، وعن طريق توجيههما نحو الخلايا التائية فقط، حققوا «إعادة توصيل» دقيقة ومستقرة للخلايا التائية البشرية داخل حيوانات حية. تصرفت خلايا CAR T المتولّدة حديثًا بشكل مقارن أو أفضل من النسخ المزروعة مختبريًا في عدة نماذج سرطانية. ومع أن العمل الكبير لا يزال مطلوبًا لإثبات السلامة، والتحكم بالجرعات، والترجمة إلى الإنسان، توضح الدراسة مسارًا واقعيًا نحو حقنات جاهزة تُخاطب جهاز المريض المناعي لقتال سرطانات الدم—ومحتملًا بعض الأورام الصلبة—دون الحاجة أبدًا إلى شحن خلاياه إلى مصنع.
الاستشهاد: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
الكلمات المفتاحية: خلايا CAR T, تحرير الجينات داخل الجسم, كريسبر, مناعة السرطان, ناقلات فيروسية