Clear Sky Science · sv
In vivo-platspecifik ingenjörskonst för att programmera om T‑celler
Göra kroppen till en egen cellfabrik
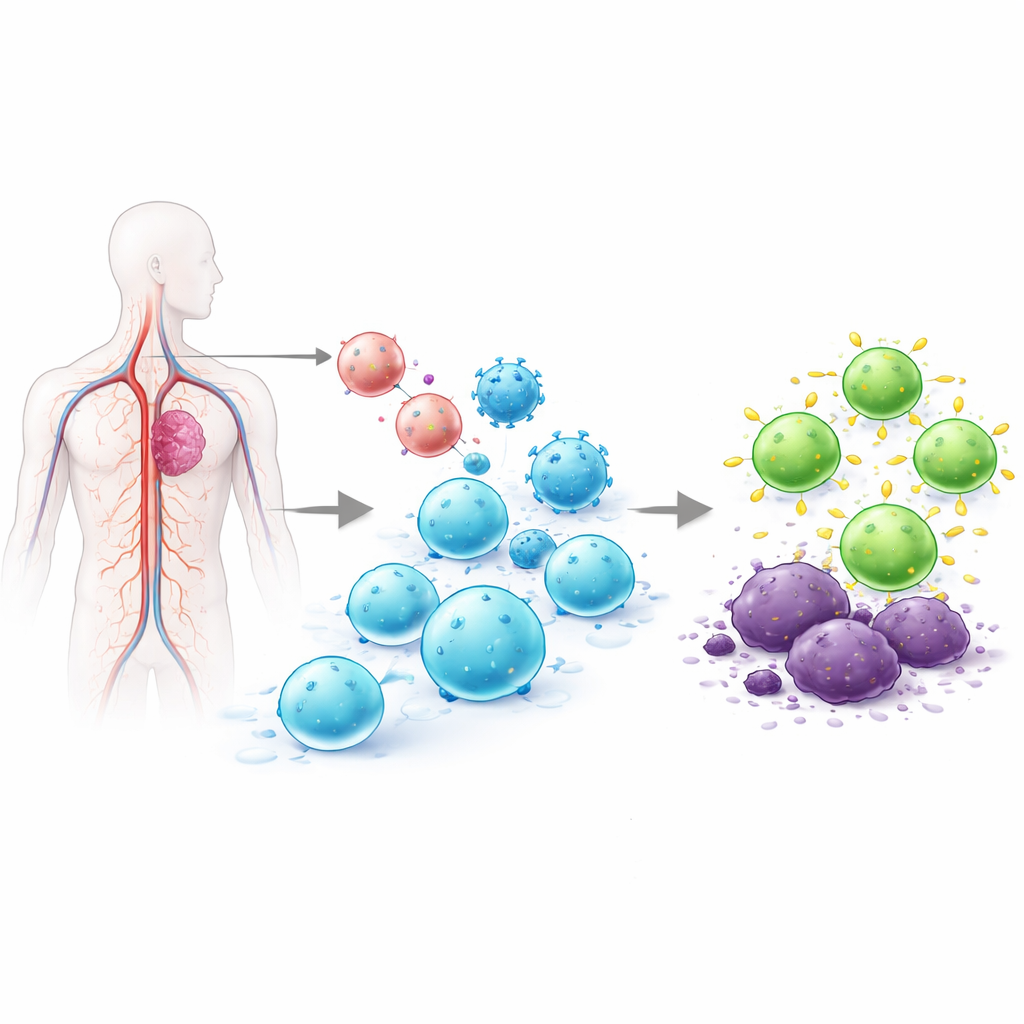
Läkare kan i dag bota vissa blodcancerformer genom att ge patienter skräddarsydda immunceller kallade CAR‑T‑celler, men dessa kraftfulla behandlingar är långsamma och extremt kostsamma att framställa. Denna studie undersöker en annan idé: i stället för att bygga dessa cellulära läkemedel i en fabrik och återföra dem, vad om vi kunde programmera en persons egna T‑celler direkt i kroppen? Forskarna beskriver ett sätt att göra just det i möss med mänskligt immunsystem, vilket pekar mot cancerterapier som en dag kan bli snabbare, billigare och mer lättillgängliga.
Varför det är så svårt att programmera om T‑celler
T‑celler är vita blodkroppar som kan hitta infekterade eller cancerösa celler. I dagens godkända CAR‑T‑terapier tas T‑celler ut från patienten, genmodifieras i ett laboratorium för att bära en tumörtajmande receptor, odlas upp till stora mängder och ges tillbaka. Denna ex vivo‑process kan ta veckor, kosta hundratusentals dollar och ge varierande cellprodukter. Tidigare försök att programmera T‑celler direkt i kroppen har förlitat sig på virala vektorer som slumpmässigt infogar DNA i genomet eller på budbärar‑RNA som försvinner efter kort tid. Slumpmässig insättning väcker säkerhetsfrågor, och kortlivad uttryck kan vara otillräckligt för att kontrollera cancer. Forskargruppen bakom denna artikel lade sig på målet att lösa båda problemen samtidigt genom att placera CAR exakt in i en naturlig T‑cellsreglerande växel, så att endast T‑celler påverkas och den nya receptorn uttrycks på ett mer reglerat och varaktigt sätt.
En två‑verktygs‑system för precis redigering i blodomloppet
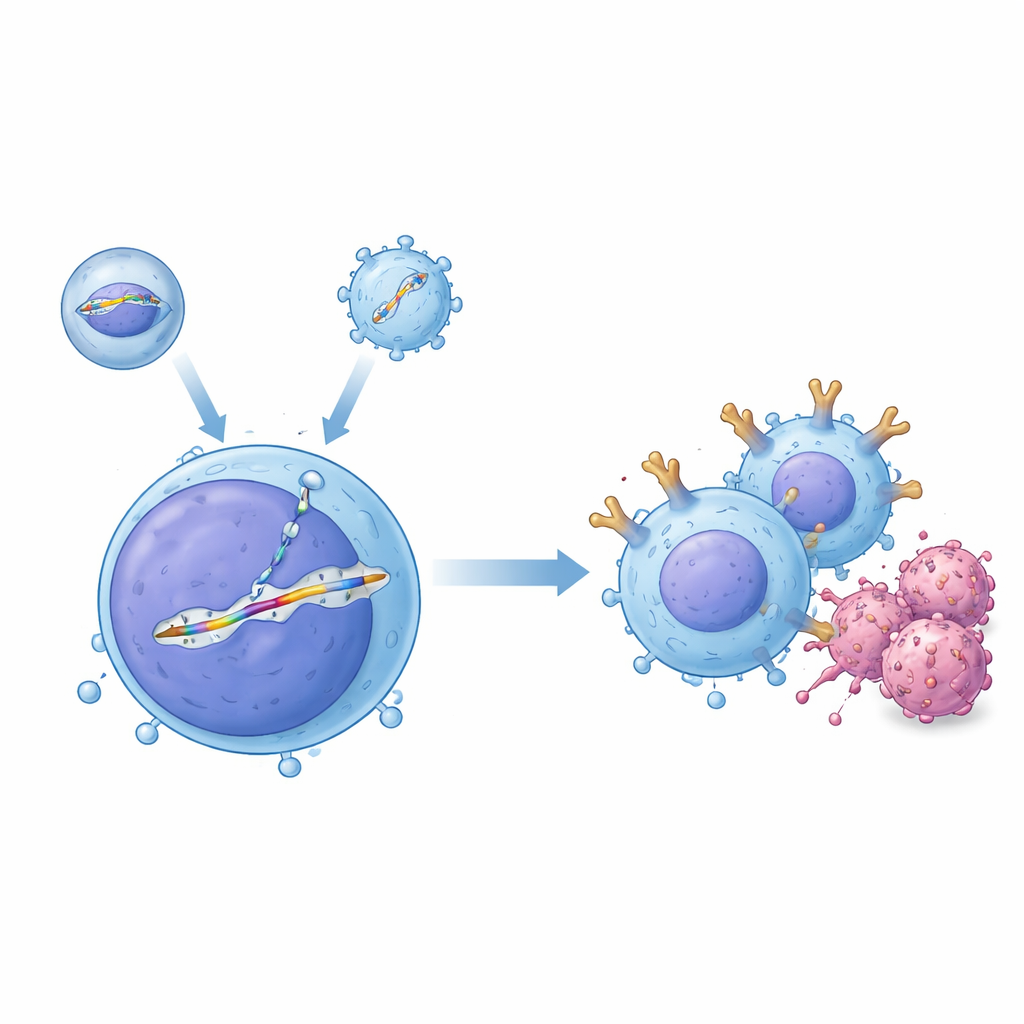
Forskarna skapade ett ”två‑vektor” leveranssystem som samarbetar inne i kroppen. Ett verktyg, kallat ett inklätt leveransfordon, för in CRISPR–Cas9 genredigeringsproteinet som är programmerat att klippa vid en specifik plats i T‑cellens DNA. Det andra verktyget, uppbyggt från ett adenoassocierat virus (AAV), bär en matchande DNA‑mall som innehåller CAR‑ritningen omgiven av sekvenser som vägleder den in i det valda slotet, ett område i T‑cellreceptorgenen känt som TRAC. När båda anländer i samma cell repareras snittet genom att kopiera från mallen och infogar prydligt ett promoterlöst CAR‑kassett under kontroll av TRAC:s naturliga på/av‑strömbrytare. I provrörsexperiment med mänskliga T‑celler genererade denna kombination stora andelar precis redigerade celler, och forskarna visade att de redigerade T‑cellerna effektivt kunde döda B‑cellsleukemiceller.
Konstruera leveransfordon för att träffa T‑celler — och missa fel mål
Att leverera dessa genetiska verktyg säkert i en levande kropp är mycket mer utmanande än i en skål, eftersom blod innehåller antikroppar och många andra celltyper som måste undvikas. För att övervinna detta utvecklade teamet en AAV‑kapsidvariant, döpt till AAV‑hT7, som förblir aktiv även i närvaro av mänskligt serum och föredrar mänskliga T‑celler framför stamceller och cancerceller. Med hjälp av CRISPR‑skärmar fann de att ett ytantigen kallat CD7 starkt påverkar hur väl denna vektor tar sig in i T‑celler, vilket hjälper till att förklara dess specificitet. Parallellt redesignade de sitt inklädda leveransfordon genom att mutera dess normala virala hölje så att det inte längre kunde binda sina vanliga receptorer, för att sedan pryda det med en antikroppsfragment som känner igen CD3, ett kännetecken för T‑celler. Denna dubbelriktade strategi styrde inte bara partiklarna mot T‑celler utan aktiverade dem också kortvarigt, vilket knuffade fler av dem in i en cellcykelstatus som gynnar precis DNA‑reparation och stabil insättning av CAR‑kassetten.
In‑body CAR‑T‑celler som kontrollerar leukemi, myelom och solida tumörer
Utrustade med sitt optimerade par — CD3‑riktade partiklar plus AAV‑hT7 DNA‑bärare — testade forskarna tillvägagångssättet i flera humaniserade musemodeller. I möss transplanterade med mänskliga blodceller omvandlade en enda intravenös dos av de två vektorerna upp till ungefär en av fem T‑celler till CAR‑T‑celler vid önskad TRAC‑plats och utplånade normala B‑celler, ett kännetecken för aktiv anti‑CD19 CAR‑funktion. I aggressiva leukemimodeller expanderade denna in vivo‑genererade CAR‑T‑population snabbt, rensade tumörer och skyddade ofta mot en senare tumöråterutmaning. Jämfört direkt med in vivo‑lentiviral CAR‑leverans gav TRAC‑riktad metod mer enhetliga CAR‑nivåer på varje cell, snabbare T‑cellexpansion och bättre tumörkontroll totalt. Teamet bytte sedan in CAR‑designer som riktar mot BCMA, en myelommarkör, eller B7‑H3, ett protein som förekommer på många solida tumörer, och visade starka svar i modeller för multipelt myelom och sarkom, inklusive varaktig kontroll efter återutmaning i många djur.
Vad detta kan innebära för framtidens cancervård
För icke‑specialister är huvudbudskapet att författarna har förvandlat kroppen till en programmerbar fabrik för skräddarsydda immunceller. Genom att leverera CRISPR‑maskineri och en omsorgsfullt utformad DNA‑mall tillsammans, och genom att rikta båda enbart till T‑celler, uppnådde de precis, stabil ”omkoppling” av mänskliga T‑celler inne i levande djur. Dessa nyskapade CAR‑T‑celler uppträdde i flera cancermodeller ungefär som eller bättre än dagens laboratorieodlade varianter. Även om mycket arbete återstår för att bevisa säkerhet, styra dosering och översätta metoden till människor, skisserar studien en realistisk väg mot färdiga injektioner som instruerar patientens eget immunsystem att bekämpa blodcancer — och potentiellt vissa solida tumörer — utan att cellerna någonsin behöver skickas till en fabrik.
Citering: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
Nyckelord: CAR‑T‑celler, in vivo genredigering, CRISPR, cancerimmunterapi, virala vektorer