Clear Sky Science · es
Ingeniería in vivo específica del sitio para reprogramar células T
Convertir el cuerpo en su propia fábrica de células
Los médicos ya pueden curar algunos cánceres de la sangre administrando a los pacientes células inmunitarias diseñadas a medida llamadas células CAR T, pero estos tratamientos tan potentes son lentos y extremadamente caros de fabricar. Este estudio explora una idea distinta: en lugar de construir estos medicamentos celulares en una fábrica e infundirlos después, ¿y si pudiéramos reprogramar directamente las células T de una persona dentro del propio cuerpo? Los investigadores describen una forma de hacer exactamente eso en ratones con sistemas inmunitarios humanos, apuntando a terapias contra el cáncer que algún día podrían ser más rápidas, baratas y más accesibles.
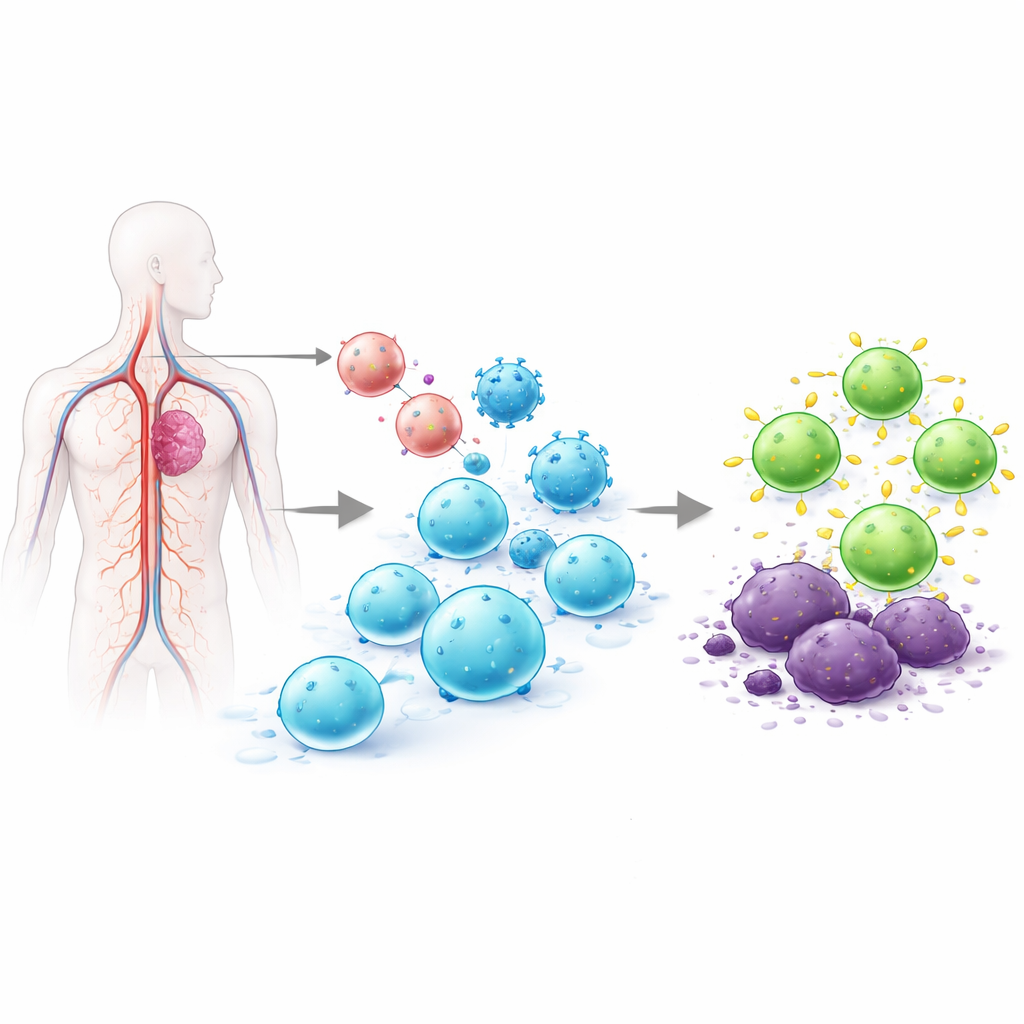
Por qué es tan difícil reprogramar células T
Las células T son leucocitos que pueden localizar células infectadas o cancerosas. En las terapias CAR T aprobadas hoy en día, las células T se extraen del paciente, se alteran genéticamente en laboratorio para portar un receptor que reconoce el tumor, se expanden hasta obtener grandes cantidades y luego se reinyectan. Este proceso ex vivo puede llevar semanas, costar cientos de miles de dólares y producir productos celulares variables. Intentos previos de programar células T directamente en el cuerpo han dependido de vectores virales que insertan ADN en posiciones aleatorias del genoma, o de ARN mensajero que desaparece tras poco tiempo. La inserción aleatoria plantea problemas de seguridad, y la expresión de corta duración puede no ser suficiente para contener los cánceres. El equipo detrás de este trabajo trató de resolver ambos problemas a la vez insertando el CAR con precisión en un interruptor de control natural de las células T, de modo que solo las células T se verían alteradas y el nuevo receptor se expresaría de manera más regulada y duradera.
Un sistema de dos herramientas para edición precisa en el torrente sanguíneo
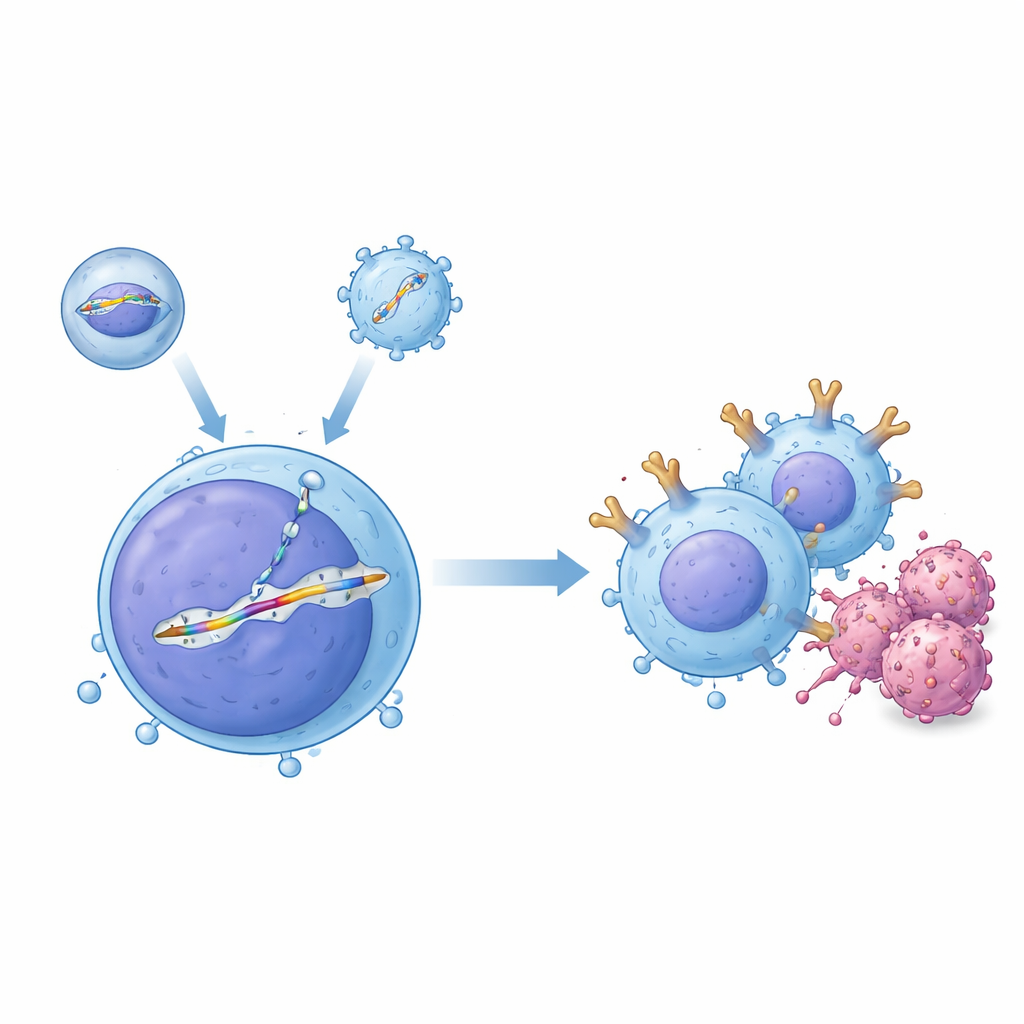
Los investigadores crearon un sistema de «dos vectores» que actúa de forma conjunta dentro del cuerpo. Una herramienta, denominada vehículo de entrega envuelto, introduce la proteína de edición génica CRISPR–Cas9 programada para cortar un sitio específico en el ADN de la célula T. La segunda herramienta, basada en un virus adenoasociado, transporta una plantilla de ADN coincidente que contiene el plano del CAR flanqueado por secuencias que guían su inserción en el hueco elegido, una región del gen del receptor de células T conocida como TRAC. Cuando ambas llegan a la misma célula, el corte se repara copiando desde la plantilla, insertando limpiamente un casete CAR sin promotor bajo el control del interruptor natural de encendido/apagado de TRAC. En experimentos en tubo con células T humanas, esta combinación generó grandes fracciones de células editadas con precisión, y los investigadores demostraron que las células T editadas podían matar eficientemente células de leucemia de linfocitos B.
Diseñar vehículos de entrega que alcancen las células T y eviten los objetivos equivocados
Administrar estas herramientas genéticas de forma segura en un organismo vivo es mucho más desafiante que en una placa de cultivo, porque la sangre contiene anticuerpos y muchos otros tipos celulares que deben evitarse. Para superar esto, el equipo evolucionó una variante de cápside de AAV, denominada AAV-hT7, que permanece activa incluso en presencia de suero humano y prefiere las células T humanas frente a células madre y células cancerosas. Mediante cribados CRISPR, hallaron que una proteína de superficie llamada CD7 influye fuertemente en la capacidad de este vector para entrar en células T, lo que ayuda a explicar su especificidad. En paralelo, rediseñaron su vehículo de entrega envuelto mutando su cubierta vírica habitual para que ya no pudiera unirse a sus receptores habituales, y luego lo decoraron con un fragmento de anticuerpo que reconoce CD3, un marcador distintivo de las células T. Esta estrategia de doble orientación no solo dirigió las partículas hacia las células T, sino que también las activó brevemente, empujando a más células hacia un estado del ciclo celular que favorece la reparación precisa del ADN y la inserción estable del casete CAR.
Células CAR T generadas in vivo que controlan leucemia, mieloma y tumores sólidos
Con su par optimizado —partículas dirigidas a CD3 más el portador de ADN AAV-hT7—, los científicos probaron el enfoque en varios modelos de ratón humanizado. En ratones injertados con células sanguíneas humanas, una única dosis intravenosa de los dos vectores convirtió hasta aproximadamente una de cada cinco células T en células CAR T en el sitio TRAC deseado y eliminó las células B normales, una señal distintiva de función activa de los CAR anti‑CD19. En modelos de leucemia agresiva, esta población de CAR T generada in vivo se expandió rápidamente, eliminó tumores y a menudo protegió frente a un reintento tumoral posterior. Comparado cara a cara con la entrega in vivo mediante lentivirus, el método dirigido a TRAC produjo niveles de CAR más uniformes en cada célula, una expansión más rápida de las células T y un mejor control global del tumor. El equipo sustituyó luego los diseños de CAR por otros dirigidos a BCMA, un marcador de mieloma, o a B7‑H3, una proteína presente en muchos tumores sólidos, y mostró respuestas contundentes en modelos de mieloma múltiple y sarcoma, incluida un control duradero tras reexposición en muchos animales.
Qué podría significar esto para la atención oncológica futura
Para quienes no son especialistas, el mensaje clave es que los autores han convertido el propio cuerpo en una fábrica programable de células inmunitarias a medida. Al administrar maquinaria CRISPR y una plantilla de ADN cuidadosamente diseñada simultáneamente, y al dirigir ambas únicamente hacia las células T, lograron un «reconectado» preciso y estable de células T humanas dentro de animales vivos. Estas células CAR recién formadas se comportaron de manera similar o superior a las versiones cultivadas en laboratorio en varios modelos de cáncer. Aunque queda mucho trabajo por delante para demostrar seguridad, controlar la dosificación y traducirlo a humanos, el estudio traza una ruta realista hacia inyecciones listas para usar que instruyan al propio sistema inmunitario del paciente para combatir cánceres de la sangre —y potencialmente algunos tumores sólidos— sin tener que enviar nunca sus células a una fábrica.
Cita: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
Palabras clave: células CAR T, edición génica in vivo, CRISPR, inmunoterapia contra el cáncer, vectores virales