Clear Sky Science · nl
In vivo sitespecifieke engineering om T-cellen te herprogrammeren
Het lichaam als eigen cel‑fabriek
Artsen kunnen sommige bloedkankers al genezen door patiënten op maat gemaakte immuuncellen, zogeheten CAR‑T‑cellen, te geven, maar deze krachtige behandelingen zijn traag en extreem duur om te produceren. Deze studie onderzoekt een ander idee: in plaats van deze cellulaire medicijnen in een fabriek te maken en terug te infuseren, wat als we iemands eigen T‑cellen rechtstreeks in het lichaam zouden kunnen herprogrammeren? De onderzoekers beschrijven een manier om precies dat te doen in muizen met een menselijk immuunsysteem, wat wijst op kankertherapieën die ooit sneller, goedkoper en breder beschikbaar zouden kunnen zijn.
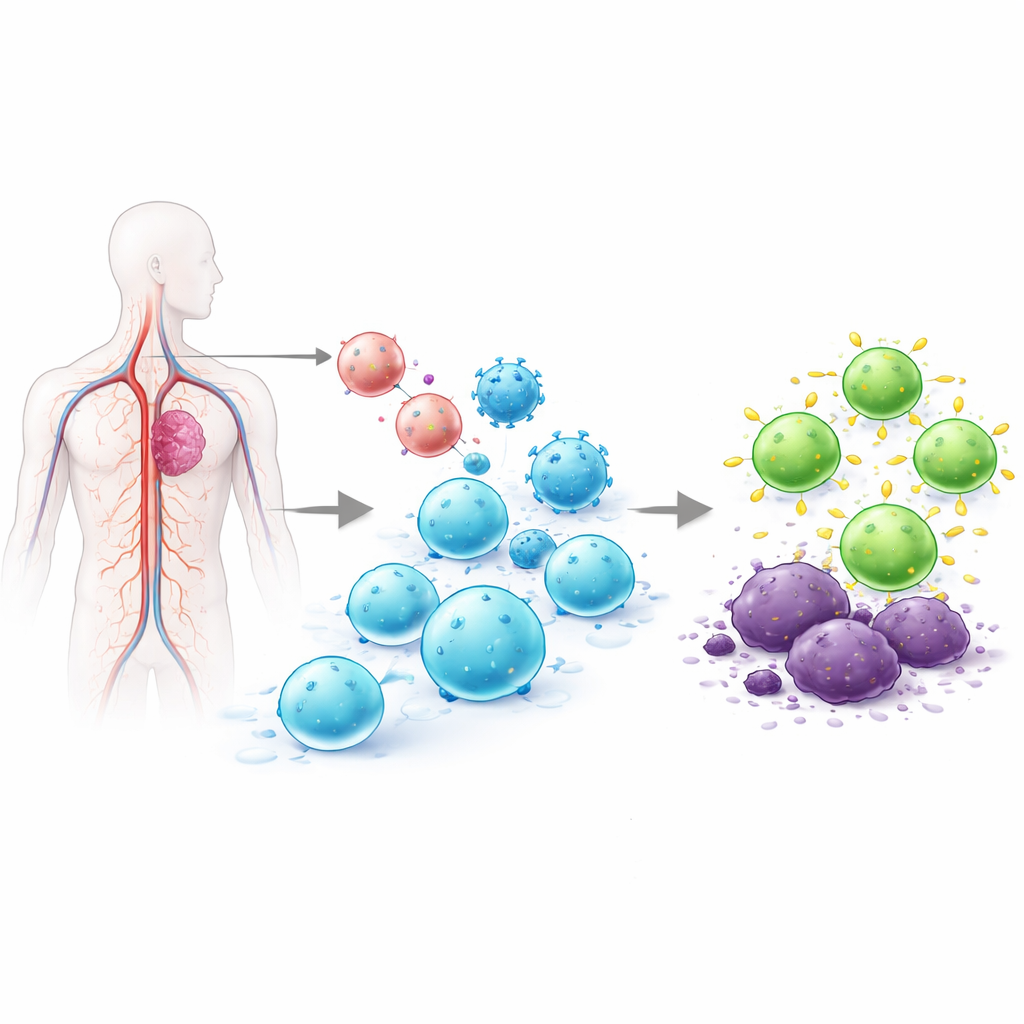
Waarom het herprogrammeren van T‑cellen zo moeilijk is
T‑cellen zijn witte bloedcellen die geïnfecteerde of kankercellen kunnen opsporen. Bij de momenteel goedgekeurde CAR‑T‑therapieën worden T‑cellen uit de patiënt genomen, in een laboratorium genetisch aangepast om een tumor‑herkennende receptor te dragen, tot grote aantallen gekweekt en vervolgens opnieuw toegediend. Dit ex vivo‑proces kan weken duren, kost honderdduizenden dollars en levert variabele celproducten op. Eerdere pogingen om T‑cellen direct in het lichaam te programmeren, leunden op virale vectoren die DNA op willekeurige plaatsen in het genoom invoegen, of op boodschapper‑RNA dat na korte tijd verdwijnt. Willekeurige insertie roept veiligheidszorgen op, en kortdurende expressie houdt mogelijk kankers niet onder controle. Het team achter dit paper wilde beide problemen tegelijk oplossen door de CAR precies in een natuurlijke T‑cel‑regelaar in te voegen, zodat alleen T‑cellen zouden worden aangepast en de nieuwe receptor op een beter gereguleerde, duurzamere manier tot expressie zou komen.
Een systeem met twee hulpmiddelen voor precieze bewerking in de bloedbaan
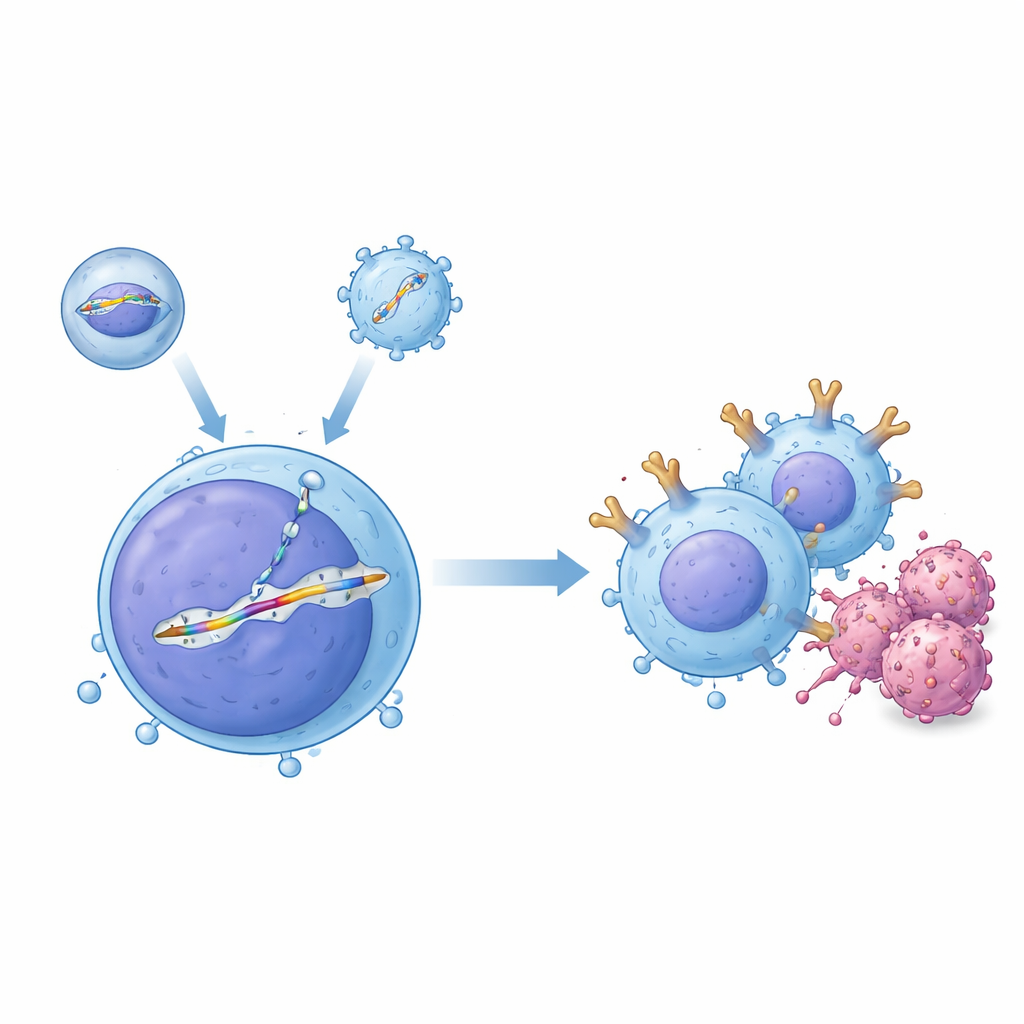
De onderzoekers ontwikkelden een “twee‑vector” afleveringssysteem dat samen in het lichaam werkt. Het ene hulpmiddel, een omhulde afleveringsvector, brengt het CRISPR–Cas9 genbewerkingsproteïne in, geprogrammeerd om een specifieke plek in het DNA van de T‑cel te knippen. Het tweede hulpmiddel, opgebouwd uit een adeno‑associated virus (AAV), draagt een bijpassend DNA‑sjabloon dat het CAR‑ontwerp bevat, geflankeerd door sequenties die het naar de gekozen plaats leiden, een regio van het T‑celreceptorgen bekend als TRAC. Wanneer beide in dezelfde cel aankomen, wordt de knip gerepareerd door van het sjabloon te kopiëren, waardoor een promoterloze CAR‑cassette netjes onder de controle van TRAC’s natuurlijke aan/uit‑schakelaar wordt ingevoegd. In reageerbuisexperimenten met menselijke T‑cellen genereerde deze combinatie grote fracties precies bewerkte cellen, en de onderzoekers toonden aan dat de bewerkte T‑cellen efficiënt B‑celleukemiecellen konden doden.
Bezorgen van vectoren die T‑cellen raken — en de verkeerde doelen missen
Het veilig afleveren van deze genetische hulpmiddelen in een levend lichaam is veel uitdagender dan in een schaaltje, omdat bloed antilichamen en vele andere celtypen bevat die moeten worden vermeden. Om dit te overwinnen, evolueerde het team een AAV‑capsidevariant, gedoopt AAV‑hT7, die actief blijft zelfs in aanwezigheid van humaan serum en voorkeur heeft voor humane T‑cellen boven stamcellen en kankercellen. Met CRISPR‑screens vonden ze dat een oppervlakteproteïne genaamd CD7 sterk beïnvloedt hoe goed deze vector T‑cellen binnendringt, wat de specificiteit deels verklaart. Parallel herontwierpen ze hun omhulde afleveringsvector door het normale virale jasje te muteren zodat het zijn gebruikelijke receptoren niet meer kon binden, en voorzagen het vervolgens van een antilichaamfragment dat CD3 herkent, een kenmerk van T‑cellen. Deze dubbelgerichte strategie stuurde de deeltjes niet alleen naar T‑cellen, maar activeerde ze ook kort, waardoor meer cellen in een celfasetoestand kwamen die precieze DNA‑reparatie en stabiele insertie van de CAR‑cassette bevordert.
In‑body CAR‑T‑cellen die leukemie, myeloom en solide tumoren onder controle houden
Gewapend met hun geoptimaliseerde paar — CD3‑gerichte deeltjes plus de AAV‑hT7 DNA‑drager — testten de wetenschappers de aanpak in meerdere gehumaniseerde muismodellen. In muizen met menselijke bloedcellen kon een enkele intraveneuze dosis van de twee vectoren tot ruwweg één op de vijf T‑cellen omzetten in CAR‑T‑cellen op de gewenste TRAC‑plek en normale B‑cellen uitroeien, een kenmerk van actieve anti‑CD19 CAR‑functie. In agressieve leukemiemodellen breidde deze in vivo‑gegenereerde CAR‑T‑populatie zich snel uit, ruimde tumoren op en bood vaak bescherming tegen een latere tumor‑heruitdaging. Vergeleken met in vivo‑levering via lentivirussen produceerde de TRAC‑gerichte methode meer uniforme CAR‑niveaus per cel, snellere T‑celuitbreiding en betere algehele tumorcontrole. Het team verving vervolgens het CAR‑ontwerp door versies die BCMA (een myeloommarker) of B7‑H3 (een eiwit dat op veel solide tumoren voorkomt) richten, en toonde sterke reacties in modellen van multipel myeloom en sarcoom, inclusief duurzame controle na heruitdaging in veel dieren.
Wat dit kan betekenen voor toekomstige kankerzorg
Voor niet‑specialisten is de kernboodschap dat de auteurs het lichaam zelf hebben veranderd in een programmeerbare fabriek voor ontworpen immuuncellen. Door CRISPR‑apparatuur en een zorgvuldig samengesteld DNA‑sjabloon samen te leveren, en beide alleen naar T‑cellen te sturen, bereikten ze een precieze, stabiele “herbedrading” van menselijke T‑cellen in levende dieren. Deze nieuw gevormde CAR‑T‑cellen gedroegen zich in meerdere kankermodellen vergelijkbaar met of beter dan huidige laboratoriumgekweekte versies. Hoewel er nog veel werk nodig is om veiligheid, dosisbeheersing en vertaling naar mensen te bewijzen, schetst de studie een realistisch pad naar kant‑klaar injecties die het eigen immuunsysteem van een patiënt instrueren bloedkankers — en mogelijk sommige solide tumoren — te bestrijden, zonder ooit hun cellen naar een fabriek te hoeven verzenden.
Bronvermelding: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
Trefwoorden: CAR-T-cellen, in vivo genbewerking, CRISPR, kankerimmunotherapie, virale vectoren