Clear Sky Science · de
In vivo ortsspezifische Technik zur Umprogrammierung von T‑Zellen
Den Körper zur eigenen Zellfabrik machen
Ärztinnen und Ärzte können heute einige Blutkrebserkrankungen heilen, indem sie Patientinnen und Patienten individuell hergestellte Immunzellen verabreichen, sogenannte CAR‑T‑Zellen. Diese wirkungsvollen Therapien sind jedoch aufwendig und extrem teuer in der Herstellung. Die vorliegende Studie verfolgt eine andere Idee: Anstatt diese zellulären Medikamente in einer Fabrik zu erzeugen und zurück zu infundieren, was wäre, wenn man die T‑Zellen einer Person direkt im Körper umprogrammieren könnte? Die Forschenden beschreiben eine Methode, die genau das in Mäusen mit humanem Immunsystem erreicht und auf Krebsbehandlungen hinweist, die eines Tages schneller, günstiger und breiter verfügbar sein könnten.
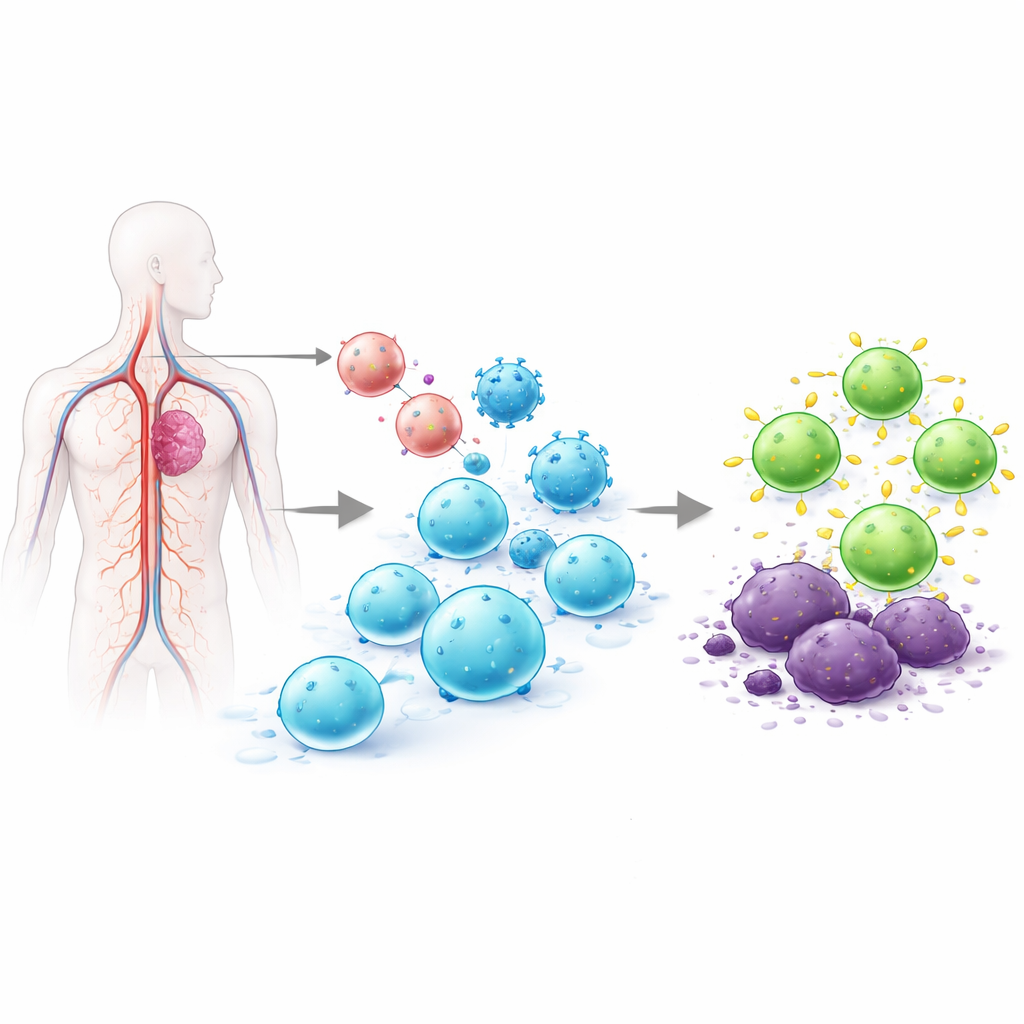
Warum die Umprogrammierung von T‑Zellen so schwierig ist
T‑Zellen sind weiße Blutkörperchen, die infizierte oder krebsartige Zellen aufspüren können. In den heute zugelassenen CAR‑T‑Therapien werden T‑Zellen dem Patienten entnommen, im Labor genetisch so verändert, dass sie einen tumorbindenden Rezeptor tragen, auf große Mengen vermehrt und dann wieder infundiert werden. Dieser ex vivo‑Prozess kann Wochen dauern, kostet Hunderttausende Dollar und liefert wechselhafte Zellprodukte. Frühere Versuche, T‑Zellen direkt im Körper zu programmieren, arbeiteten mit viralen Vektoren, die DNA zufällig ins Genom einfügen, oder mit Messenger‑RNA, die nur kurz exprimiert wird. Zufällige Einfügungen werfen Sicherheitsfragen auf, und kurzlebige Expression kann Krebs kaum dauerhaft in Schach halten. Das Team dieser Arbeit wollte beide Probleme zugleich lösen, indem es das CAR präzise an einen natürlichen Kontrollschalter der T‑Zelle einfügt, sodass nur T‑Zellen verändert werden und der neue Rezeptor auf reguliertere, beständigere Weise exprimiert wird.
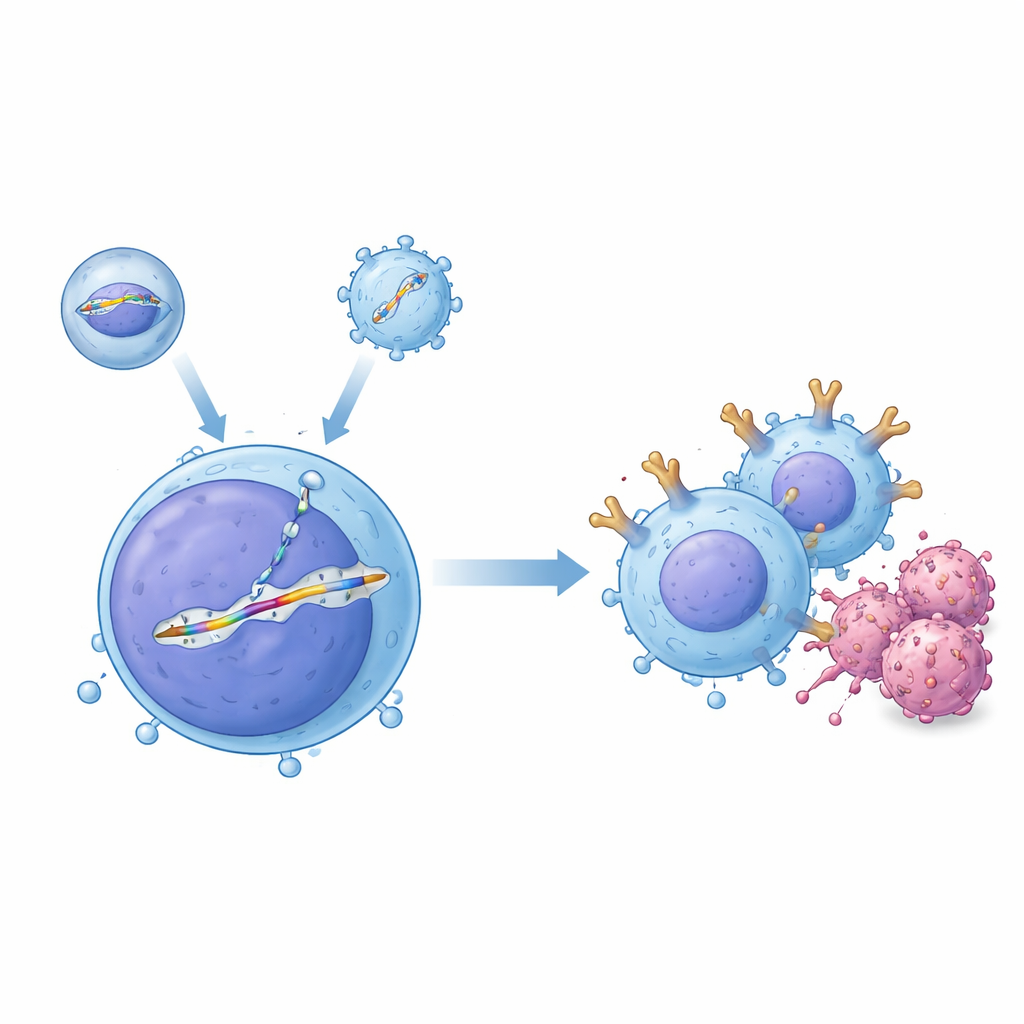
Ein Zwei‑Werkzeug‑System für präzise Editierung im Blutkreislauf
Die Forschenden entwickelten ein „Zwei‑Vektor“‑Lieferungssystem, das im Körper zusammenwirkt. Ein Werkzeug, ein umhüllter Transportträger, bringt das CRISPR–Cas9‑Geneditierprotein ins Ziel, das so programmiert ist, eine bestimmte Stelle in der DNA der T‑Zelle zu schneiden. Das zweite Werkzeug, gebaut aus einem Adeno‑assoziierten Virus (AAV), trägt eine passende DNA‑Schablone, die den Bauplan des CAR enthält, flankiert von Sequenzen, die das Einfügen an die gewählte Stelle leiten — eine Region des T‑Zell‑Rezeptor‑Gens, bekannt als TRAC. Wenn beide Komponenten in derselben Zelle eintreffen, wird der Schnitt durch Kopieren von der Schablone repariert und ein promoterloses CAR‑Kassett sauber unter die Kontrolle des natürlichen An‑/Ausschalters von TRAC eingesetzt. In Reagenzglas‑Experimenten mit humanen T‑Zellen erzeugte dieses Paar große Anteile präzise editierter Zellen, und die Autorinnen und Autoren zeigten, dass die editierten T‑Zellen B‑Zell‑Leukämiezellen effizient abtöten konnten.
Lieferfahrzeuge so gestalten, dass sie T‑Zellen treffen — und falsche Ziele meiden
Genetische Werkzeuge sicher im lebenden Organismus zu liefern, ist weit anspruchsvoller als in der Petrischale, weil Blut Antikörper und viele andere Zelltypen enthält, die gemieden werden müssen. Um dies zu überwinden, entwickelte das Team eine AAV‑Kapsidvariante, AAV‑hT7 genannt, die auch in Gegenwart von menschlichem Serum aktiv bleibt und menschliche T‑Zellen gegenüber Stammzellen und Krebszellen bevorzugt. Mithilfe von CRISPR‑Screens fanden sie, dass ein Oberflächenprotein namens CD7 stark beeinflusst, wie gut dieser Vektor in T‑Zellen eindringt, was seine Spezifität erklärt. Parallel dazu gestalteten sie ihren umhüllten Transportträger neu, indem sie die normale virale Hülle so mutierten, dass sie nicht mehr an ihre üblichen Rezeptoren binden kann, und ihn dann mit einem Antikörperfragment versahen, das CD3 erkennt — ein Kennzeichen von T‑Zellen. Diese Doppelziel‑Strategie lenkte Partikel nicht nur gezielt zu T‑Zellen, sondern aktivierte sie kurzfristig, wodurch mehr Zellen in einen Zellzyklus‑Zustand gedrängt wurden, der präzise DNA‑Reparatur und stabile Einfügung des CAR‑Kassetten begünstigt.
Im Körper erzeugte CAR‑T‑Zellen kontrollieren Leukämie, Myelom und solide Tumore
Mit ihrem optimierten Paar — CD3‑gezielte Partikel plus dem AAV‑hT7‑DNA‑Träger — testeten die Wissenschaftlerinnen und Wissenschaftler den Ansatz in mehreren humanisierten Mausmodellen. Bei Mäusen, die mit menschlichen Blut‑Zellen transplantiert waren, verwandelte eine einzige intravenöse Dosis der beiden Vektoren bis zu etwa eine von fünf T‑Zellen am gewünschten TRAC‑Ort in CAR‑T‑Zellen und beseitigte normale B‑Zellen, ein Kennzeichen aktiver Anti‑CD19‑CAR‑Funktion. In aggressiven Leukämiemodellen expandierte die in vivo erzeugte CAR‑T‑Population schnell, beseitigte Tumoren und schützte oft gegen eine spätere Tumor‑Rechallenge. Im direkten Vergleich mit einer in vivo Lentiviral‑CAR‑Lieferung produzierte die TRAC‑gezielte Methode gleichmäßigere CAR‑Spiegel pro Zelle, schnellere T‑Zell‑Expansion und eine bessere Tumorkontrolle insgesamt. Das Team setzte dann CAR‑Designs gegen BCMA, einen Myelom‑Marker, oder B7‑H3, ein auf vielen soliden Tumoren vorkommendes Protein, ein und zeigte starke Antworten in Modellen von multiplem Myelom und Sarkom, einschließlich anhaltender Kontrolle nach Rechallenge bei vielen Tieren.
Was das für die zukünftige Krebsversorgung bedeuten könnte
Für Nichtfachleute ist die Kernbotschaft, dass die Autorinnen und Autoren den Körper selbst in eine programmierbare Fabrik für maßgeschneiderte Immunzellen verwandelt haben. Durch gleichzeitiges Liefern der CRISPR‑Maschinerie und einer sorgfältig gestalteten DNA‑Schablone und durch das gezielte Lenken beider Komponenten ausschließlich in T‑Zellen erreichten sie eine präzise, stabile „Umschaltung“ menschlicher T‑Zellen in lebenden Tieren. Diese neu erzeugten CAR‑T‑Zellen verhielten sich in mehreren Krebsmodellen ähnlich gut oder besser als die heute im Labor gezüchteten Versionen. Obwohl noch viel Arbeit nötig ist, um Sicherheit, Dosiskontrolle und die Übersetzung auf den Menschen zu beweisen, skizziert die Studie einen realistischen Weg zu fertigen Injektionen, die das eigene Immunsystem einer Patientin oder eines Patienten anleiten, Blutkrebserkrankungen — und möglicherweise einige solide Tumoren — zu bekämpfen, ohne die Zellen jemals in eine Fabrik schicken zu müssen.
Zitation: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
Schlüsselwörter: CAR‑T‑Zellen, in vivo Geneditierung, CRISPR, Krebsimmuntherapie, virale Vektoren