Clear Sky Science · he
הנדסה אתר-ספציפית ב־vivo לתכנות מחדש של תאי T
להפוך את הגוף למפעל תאים משלו
רופאים יכולים כיום לרפא חלק מסוגי סרטן הדם על ידי מתן תאי חיסון מותאמים אישית הנקראים תאי CAR T, אך טיפולים רבי־עוצמה אלה איטיים ויקרי ייצור במידה קיצונית. המחקר הזה חוקר רעיון שונה: במקום לבנות את תרופות התאים הללו במפעל ולהחזירן לגוף, מה אם נוכל לתכנת מחדש את תאי ה‑T של האדם ישירות בתוך הגוף? החוקרים מתארים שיטה שמבצעת בדיוק את זה בעכברים עם מערכת חיסון אנושית, ומביאה לכיווני טיפולים בסרטן שעשויים בעתיד להיות מהירים יותר, זולים יותר וזמינים באופן רחב יותר.
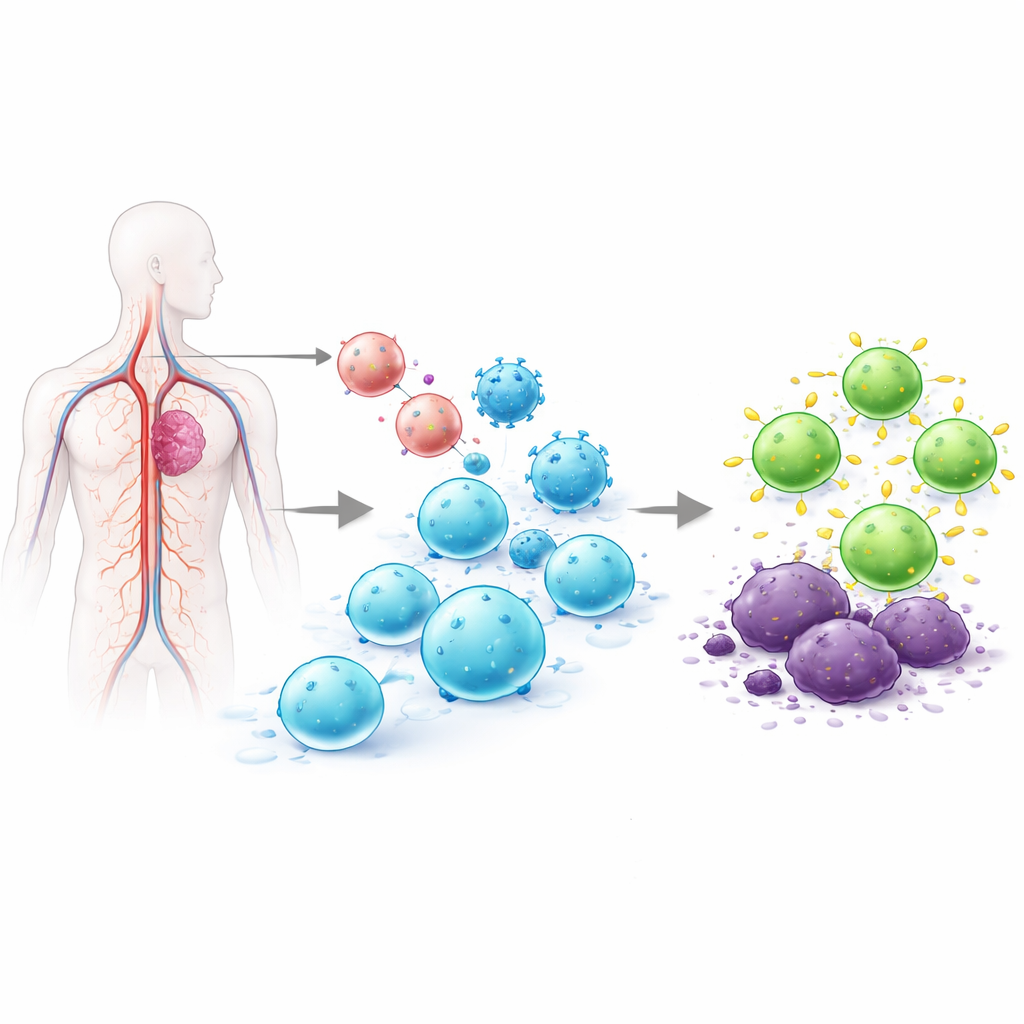
למה תכנות מחדש של תאי T כל כך קשה
תאי T הם תאי דם לבנים היכולים לצוד תאים נגועים או סרטניים. בטיפולי CAR T המאושרים היום, מסירים את תאי ה‑T מהחולה, משנים אותם גנטית במעבדה כדי לשאת קולטן המכוון לגידול, מגדלים אותם בכמויות גדולות ואז מזריקים חזרה. התהליך החיצוני הזה יכול לקחת שבועות, לעלות מאות אלפי דולרים ולהניב מוצרים תאיים משתנים. ניסיונות קודמים לתכנת תאי T ישירות בגוף הסתמכו על וקטורים ויראליים שמחדירים DNA במיקומים אקראיים בגנום, או על RNA שליח שנעלם אחרי זמן קצר. החדרת DNA באקראי מעלה חששות בטיחותיים, והבעה קצרה עלולה שלא לשמור על השליטה בגידולים. הצוות מאחורי המאמר ניסה לפתור את שתי הבעיות בו־זמנית על ידי הכנסת ה‑CAR במדויק למתג בקרה טבעי של התא T, כך שרק תאי T ישתנו והקולטן החדש יביע בצורה מבוקרת ועמידה יותר.
מערכת דו־כלית לעריכה מדויקת במחזור הדם
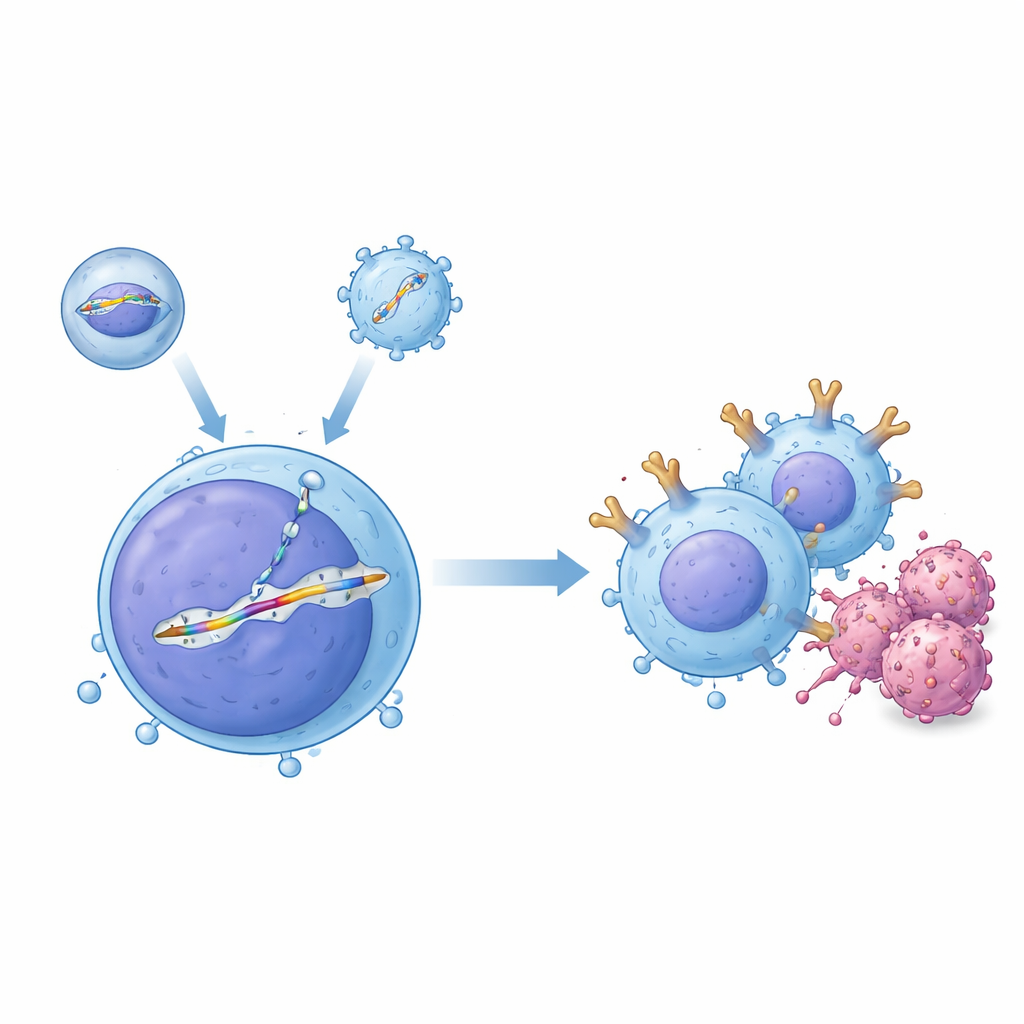
החוקרים יצרו מערכת מסירה "דו־וקטורית" שעובדת יחד בתוך הגוף. כלי אחד, שנקרא גוף מסירה עטוף, מביא את חלבון העריכה הגנטית CRISPR–Cas9 שתוכנת לגזור אתר ספציפי בדנ״א של תא ה‑T. הכלי השני, המבוסס על וירוס מקבוצת adeno-associated virus, נושא תבנית DNA תואמת שמכילה את התכנון של ה‑CAR ומוקפת רצפים שמנחים אותה להיכנס לחריץ הנבחר, אזור של גן קולטן ה‑T הידוע בשם TRAC. כששניהם מגיעים לאותו תא, החתך מתוקן על ידי העתקה מהתבנית, וה‑CAR מוכנס באופן מסודר בקאסטה ללא פרומוטור תחת בקרה של מתג ה‑TRAC הטבעי. בניסויים בצינור מבחנה עם תאי T אנושיים, השילוב הזה ייצר אחוזים גבוהים של תאים שעודכנו במדויק, והחוקרים הראו שהתאים המותאמים יכלו להרוג ביעילות תאי לוקמיה של תאי B.
הנדסת כלי מסירה שפוגעים בתאי T — ומחמיצים מטרות שגויות
מסירה בטוחה של כלים גנטיים בגוף חי היא מאתגרת בהרבה מאשר בצלחת, משום שהדם מכיל נוגדנים והרבה סוגי תאים שיש להימנע מהם. כדי להתגבר על זה, הצוות פיתח וריאנט קפסיד של AAV, שכינו אותו AAV‑hT7, שנותר פעיל גם בנוכחות סרום אנושי ומעדיף תאי T אנושיים על פני תאי גזע ותאי סרטן. בעזרת מסכי CRISPR הם מצאו כי חלבון פני שטח בשם CD7 משפיע חזק על יכולת הווקטור להיכנס לתאי T, מה שמסייע להסביר את הספציפיות שלו. במקביל, הם שינו את גוף המסירה העטוף על ידי מוטציה במעטפת הוויראלית הרגילה כך שלא יוכל עוד להיקשר לקולטנים הרגילים שלו, ולאחר מכן קישטו אותו בקטע נוגדן שמזהה CD3, סימן היכר של תאי T. אסטרטגיית יעד כפול זו לא רק כיוונה את חלקיקי המסירה לתאי T אלא גם הפעילה אותם באופן קצר, מה שדחף יותר מהם למצב מחזור תא שמקדם תיקון דנ״א מדויק והכנסה יציבה של קאסטת ה‑CAR.
תאי CAR T שנוצרו בגוף שולטם בלוקמיה, מיאלומה וגידולים מוצקים
מצוידים בזוג המותאם שלהם — חלקיקים ממוקדי CD3 בתוספת נשא ה‑DNA AAV‑hT7 — המדענים בחנו את הגישה בכמה דגמי עכברים עם מערכת חיסון אנושית. בעכברים שקיבלו השתלה של תאי דם אנושיים, מנה אחת תוך־ורידית של שני הווקטורים המרה עד לערך של כמעט אחד מכל חמשת תאי T לתאי CAR T באתר ה‑TRAC הרצוי והשמידה תאי B נורמליים, מאפיין של פעילות CAR נגד CD19. בדגמי לוקמיה אגרסיביים, אוכלוסיית ה‑CAR T שנוצרה ב‑vivo התרחבה במהירות, ניקתה גידולים ולעתים קרובות הגנה מפני אתגר מחודש של הגידול. בהשוואה ישירה למשלוח CAR ויראלי לנטוויי ב‑vivo, השיטה הממוקדת ל‑TRAC הפיקה רמות CAR אחידות יותר בכל תא, התרחבות מהירה יותר של תאי T ושליטה טובה יותר על הגידול הכולל. הצוות החליף לאחר מכן לעיצובי CAR המכוונים ל‑BCMA, סימן מיאלומה, או ל‑B7‑H3, חלבון הנמצא על גידולים מוצקים רבים, והראה תגובות חזקות בדגמי מיאלומה רבתי וסרקומה, כולל שליטה ארוכת טווח לאחר אתגר מחודש בחיות רבות.
מה זה יכול להעיד על טיפול בסרטן בעתיד
ללא מומחים, המסר המרכזי הוא שהמחברים הפכו את הגוף עצמו למפעל ניתן‑תכנות של תאי חיסון מעוצבים. על ידי מסירת מכונת ה‑CRISPR ותבנית DNA מעוצבת יחד, ועל ידי כוונון שניהם רק לתאי T, הם השיגו "חיבור מחדש" מדויק ועמיד של תאי T אנושיים בתוך בעלי חיים חיים. תאי CAR T שנוצרו כך התנהגו בדומה או טוב יותר מהגרסאות שגודלו במעבדה בכמה דגמי סרטן. אף שנותר עוד עבודה רבה להוכיח בטיחות, לשלוט במינון ולתרגם לבני אדם, המחקר מציג מסלול ריאלי לעבר מנות מוכנות לשימוש שמלמדות את מערכת החיסון של החולה להילחם בסרטני דם — ובאופן פוטנציאלי גם בחלק מהגידולים המוצקים — בלי הצורך לשלוח את התאים למפעל.
ציטוט: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
מילות מפתח: תאי CAR T, עריכת גנים ב־vivo, CRISPR, אימונותרפיה נגד סרטן, וקטורים ויראליים