Clear Sky Science · pl
In vivo site-specific engineering to reprogram T cells
Przekształcenie organizmu we własną fabrykę komórek
Lekarze potrafią już wyleczyć niektóre nowotwory krwi, podając pacjentom niestandardowe komórki odpornościowe zwane limfocytami CAR T, ale te potężne terapie są powolne i niezwykle kosztowne w produkcji. W tym badaniu rozważono inną koncepcję: zamiast wytwarzać te „leki komórkowe” w fabryce i podawać je z powrotem, co by było, gdybyśmy mogli przeprogramować własne limfocyty T pacjenta bezpośrednio w organizmie? Naukowcy opisują sposób zrealizowania tego u myszy z ludzkim układem odpornościowym, wskazując drogę do terapii przeciwnowotworowych, które mogłyby być w przyszłości szybsze, tańsze i szerzej dostępne.
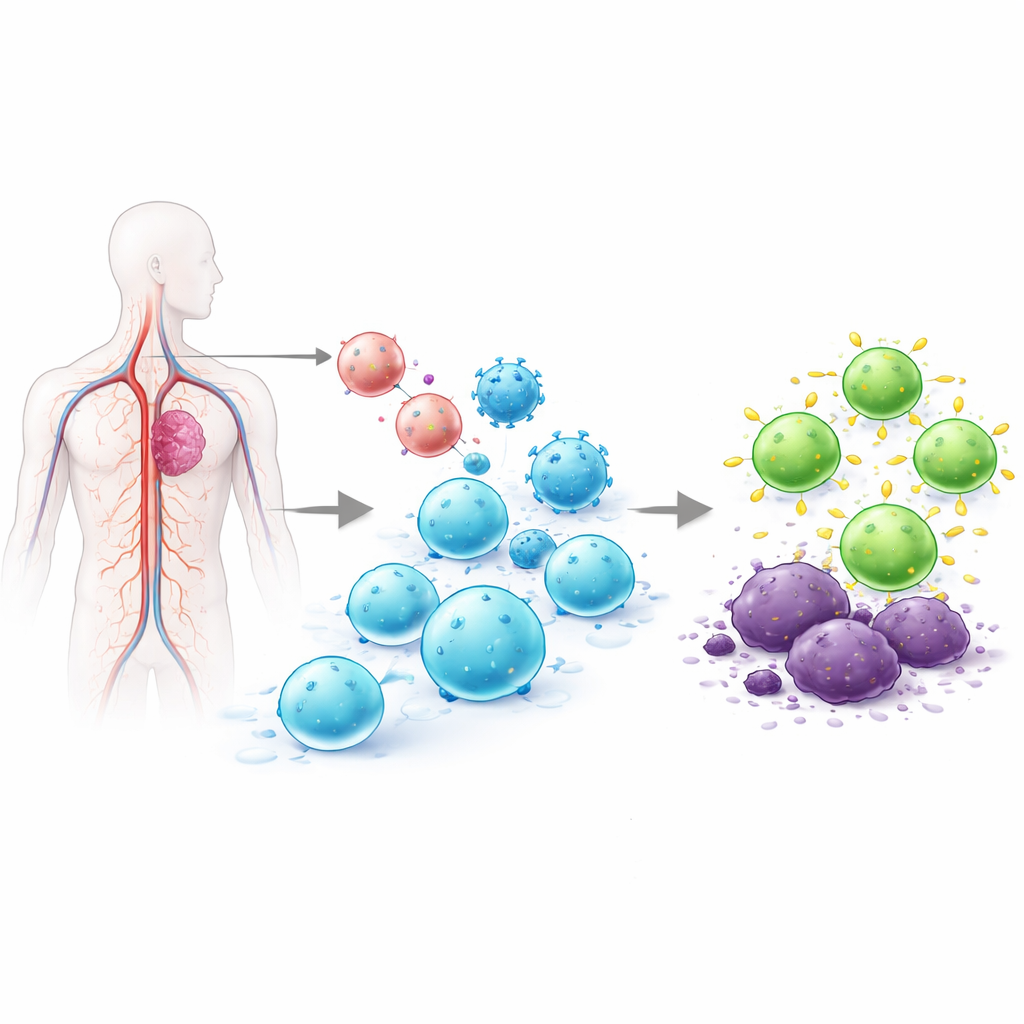
Dlaczego przeprogramowanie limfocytów T jest takie trudne
Limfocyty T to białe krwinki zdolne do wykrywania i niszczenia zakażonych lub nowotworowych komórek. W obecnie zatwierdzonych terapiach CAR T limfocyty są izolowane od pacjenta, genetycznie modyfikowane w laboratorium tak, by przenosiły receptor ukierunkowany na guz, namnażane do dużych ilości, a następnie ponownie podawane. Ten proces ex vivo może trwać tygodnie, kosztować setki tysięcy dolarów i dawać zmienne produkty komórkowe. Wcześniejsze próby programowania limfocytów bezpośrednio w organizmie opierały się na wektorach wirusowych wstawiających DNA losowo w genom lub na mRNA, które znika po krótkim czasie. Losowe wstawienia budzą obawy o bezpieczeństwo, a krótkotrwała ekspresja może nie powstrzymać nowotworu. Zespół autorów pracy postawił sobie za cel rozwiązanie obu problemów jednocześnie poprzez precyzyjne włączenie CAR do naturalnego przełącznika kontrolnego limfocytu T, tak aby zmodyfikowane były wyłącznie komórki T, a nowy receptor był wyrażany w bardziej regulowany i trwały sposób.
System dwu-narzędziowy do precyzyjnego edytowania we krwiobiegu
Naukowcy stworzyli system dostarczania „dwuwektorowy”, w którym dwa narzędzia współpracują wewnątrz organizmu. Jednym z nich jest otoczony pancerzem nośnik dostarczający białko do edycji genów CRISPR–Cas9 zaprogramowane do ucięcia konkretnego miejsca w DNA limfocytu T. Drugie narzędzie, oparte na wirusie AAV (adeno-associated virus), przenosi dopasowany wzorzec DNA zawierający schemat CAR otoczony sekwencjami kierującymi go do wybranego miejsca — regionu genu receptora limfocytów T znanego jako TRAC. Gdy oba składniki trafią do tej samej komórki, przecięcie jest naprawiane poprzez kopiowanie z wzorca, co pozwala schludnie wstawić kasetę CAR bez promotora pod kontrolą naturalnego przełącznika on/off TRAC. W eksperymentach in vitro na ludzkich limfocytach T to połączenie generowało duże ułamki precyzyjnie edytowanych komórek, a badacze wykazali, że zmodyfikowane limfocyty T skutecznie zabijały komórki białaczki z linii B.
Projektowanie nośników, które trafiają w limfocyty T — i omijają niewłaściwe cele
Dostarczanie tych narzędzi genetycznych bezpiecznie w żywym organizmie jest znacznie trudniejsze niż w naczyniu, ponieważ krew zawiera przeciwciała i wiele innych typów komórek, których należy unikać. Aby to obejść, zespół wyewoluował wariant kapsydu AAV, nazwany AAV-hT7, który pozostaje aktywny nawet w obecności surowicy ludzkiej i preferuje ludzkie limfocyty T nad komórkami macierzystymi i komórkami nowotworowymi. Dzięki przesiewom CRISPR odkryli, że białko powierzchniowe o nazwie CD7 silnie wpływa na to, jak dobrze wektor wchodzi do limfocytów T, co pomaga wyjaśnić jego specyficzność. Równolegle przeprojektowali swój otoczony pancerzem nośnik, mutując jego normalną osłonkę wirusową tak, by nie mógł już wiązać swoich zwykłych receptorów, a następnie ozdobili go fragmentem przeciwciała rozpoznającego CD3 — cechę charakterystyczną limfocytów T. Ta strategia podwójnego celowania nie tylko ukierunkowała cząstki na limfocyty T, lecz także krótkotrwale je aktywowała, skłaniając więcej komórek do wejścia w fazę cyklu komórkowego sprzyjającą precyzyjnej naprawie DNA i stabilnemu wstawieniu kasety CAR.
CAR T w organizmie, które kontrolują białaczkę, szpiczaka i guzy lite
Uzbrojeni w zoptymalizowaną parę — cząstki celowane na CD3 plus nośnik DNA AAV-hT7 — naukowcy przetestowali podejście w kilku modelach mysich z humanizowanym układem odpornościowym. U myszy przeszczepionych ludzkimi komórkami krwi pojedyncza dożylna dawka obu wektorów przekształciła do około jednej na pięć limfocytów T w CAR T umieszczone w pożądanym miejscu TRAC i zlikwidowała normalne komórki B, co jest znakiem aktywnej funkcji anty-CD19 CAR. W agresywnych modelach białaczki populacja CAR T powstała in vivo szybko się rozszerzała, usuwała guzy i często chroniła przed późnym ponownym wyzwaniem nowotworem. W porównaniu bezpośrednim z dostarczaniem CAR przez wektory lentiwirusowe in vivo, metoda ukierunkowana na TRAC dała bardziej jednorodny poziom CAR na każdej komórce, szybszą ekspansję limfocytów T i lepszą kontrolę guza. Zespół następnie zastosował konstrukcje CAR skierowane przeciw BCMA — markerowi szpiczaka — lub B7-H3 — białku występującemu na wielu guzach litych — i uzyskał silne odpowiedzi w modelach szpiczaka mnogiego i mięsaka, włącznie z trwałą kontrolą po ponownym wyzwaniu u wielu zwierząt.
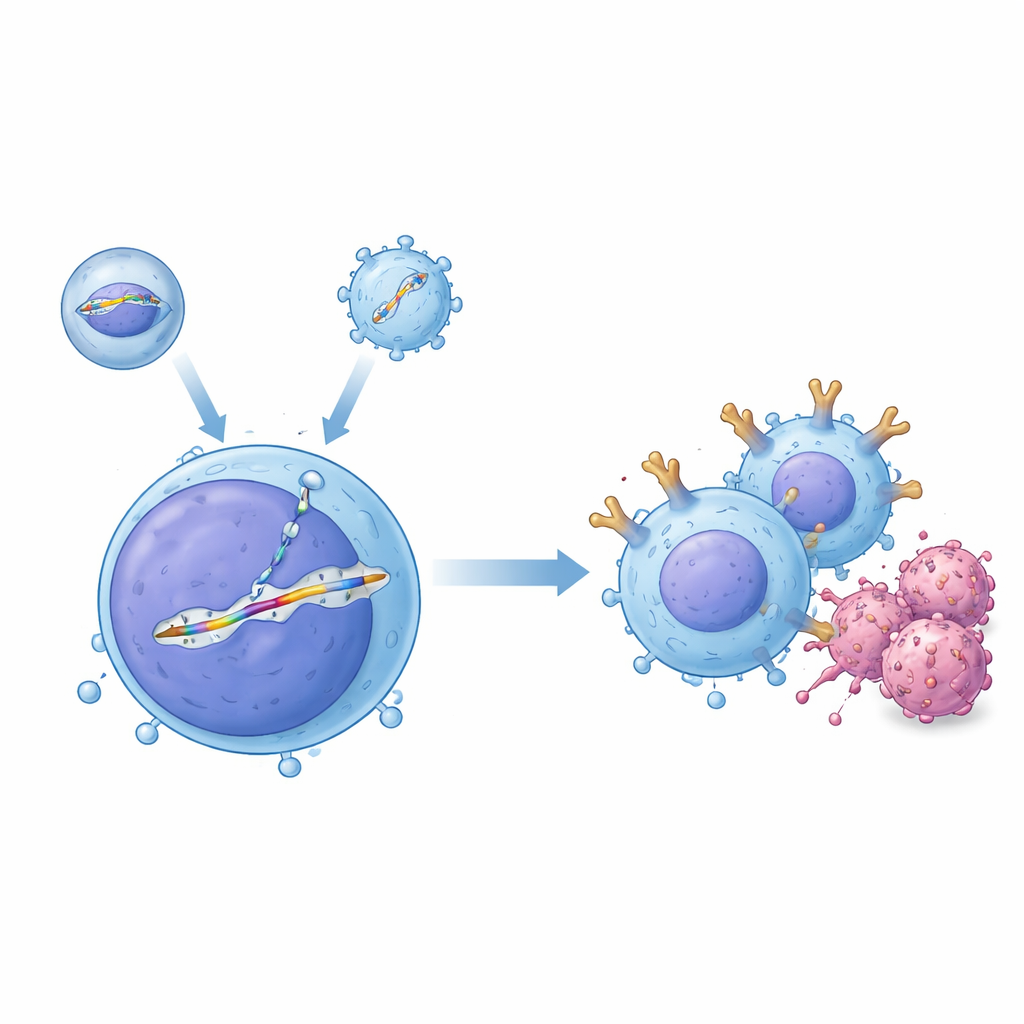
Co to może znaczyć dla przyszłej opieki onkologicznej
Dla osób spoza specjalności kluczowa wiadomość jest taka, że autorzy przekształcili sam organizm w programowalną fabrykę komórek odpornościowych na zamówienie. Poprzez jednoczesne dostarczenie aparatury CRISPR i starannie zaprojektowanego wzorca DNA oraz skierowanie obu elementów wyłącznie do limfocytów T osiągnęli precyzyjne, stabilne „przeprogramowanie” ludzkich limfocytów T w żywych organizmach. Nowo powstałe limfocyty CAR T zachowywały się podobnie do lub lepiej niż obecne, hodowane w laboratorium wersje w kilku modelach nowotworowych. Chociaż wciąż pozostaje wiele pracy, by udowodnić bezpieczeństwo, kontrolować dawkowanie i przełożyć wyniki na ludzi, badanie przedstawia realną ścieżkę ku gotowym do użycia zastrzykom, które poinstruują układ odpornościowy pacjenta do zwalczania nowotworów krwi — i potencjalnie niektórych guzów litych — bez konieczności wysyłania ich komórek do fabryki.
Cytowanie: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
Słowa kluczowe: CAR T cells, in vivo gene editing, CRISPR, cancer immunotherapy, viral vectors