Clear Sky Science · ja
生体内の部位特異的改変でT細胞を再プログラムする
体を自前の細胞工場に変える
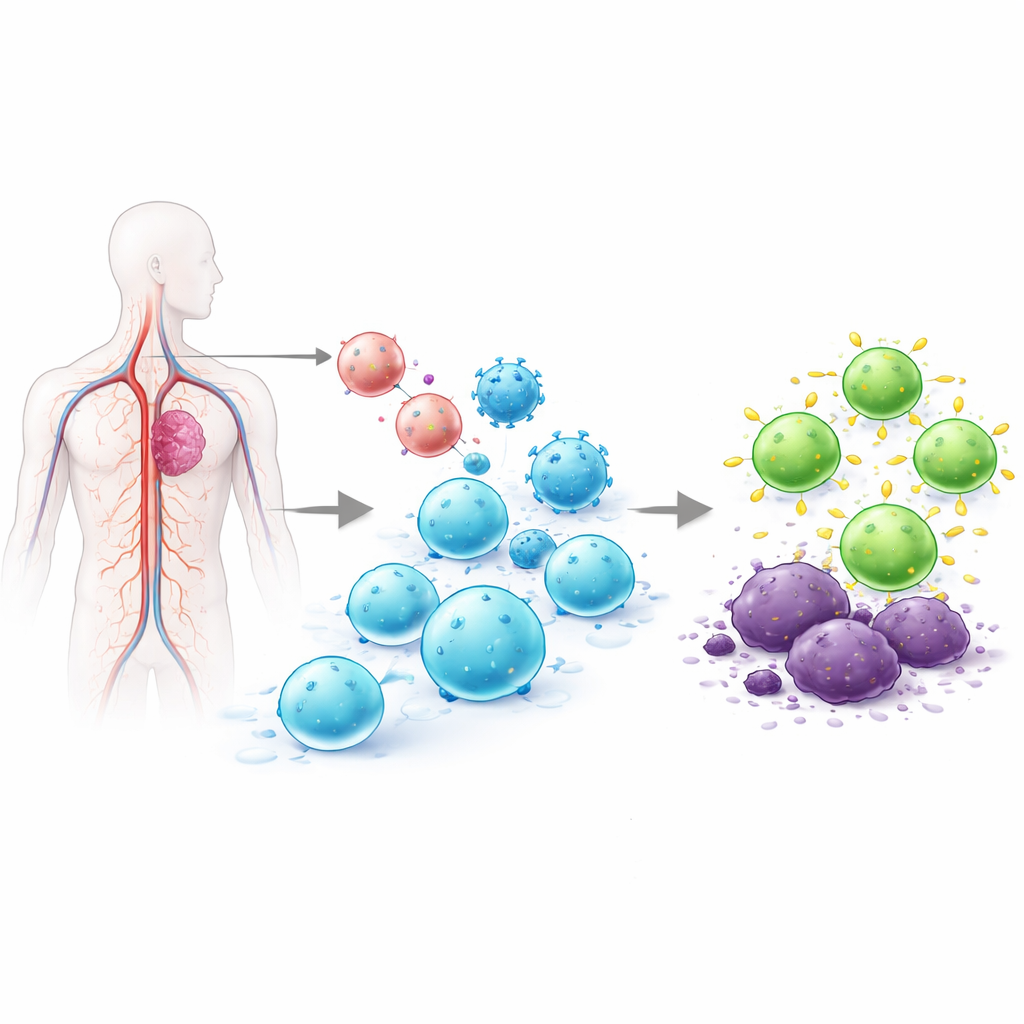
医師は現在、CAR T細胞と呼ばれる患者ごとに作られた免疫細胞を投与することで一部の血液がんを治療できるようになりましたが、これら強力な治療は製造に時間がかかり、非常に高額です。本研究は別の発想を探ります。つまり、これらの細胞医薬を工場で作って戻すのではなく、患者自身のT細胞を直接体内で再プログラムできないか、というものです。研究者らはヒト免疫系を移植したマウスでまさにそれを行う方法を示し、将来、より速く、安価で広く利用可能ながん療法への道を指し示しています。
T細胞の再プログラムが難しい理由
T細胞は感染細胞やがん細胞を見つけ出す白血球です。現在承認されているCAR T療法では、患者からT細胞を取り出して、腫瘍標的を認識する受容体を持つように遺伝子操作し、増殖させてから再び体内に戻します。この体外プロセスは数週間かかり、数十万ドルの費用がかかり、得られる細胞製品にばらつきがあります。体内で直接T細胞を改変しようとしたこれまでの試みは、ゲノムのランダムな位置にDNAを挿入するウイルスベクターや、短期間で消失するmRNAに依存してきました。ランダム挿入は安全性の懸念を生み、短期発現ではがんを抑え続けられない可能性があります。本論文のチームは両方の問題を同時に解決することを目指し、CARをT細胞の自然な制御スイッチに正確に挿入することで、改変されるのがT細胞だけに限られ、新しい受容体がより制御された持続的な形で発現するようにしました。
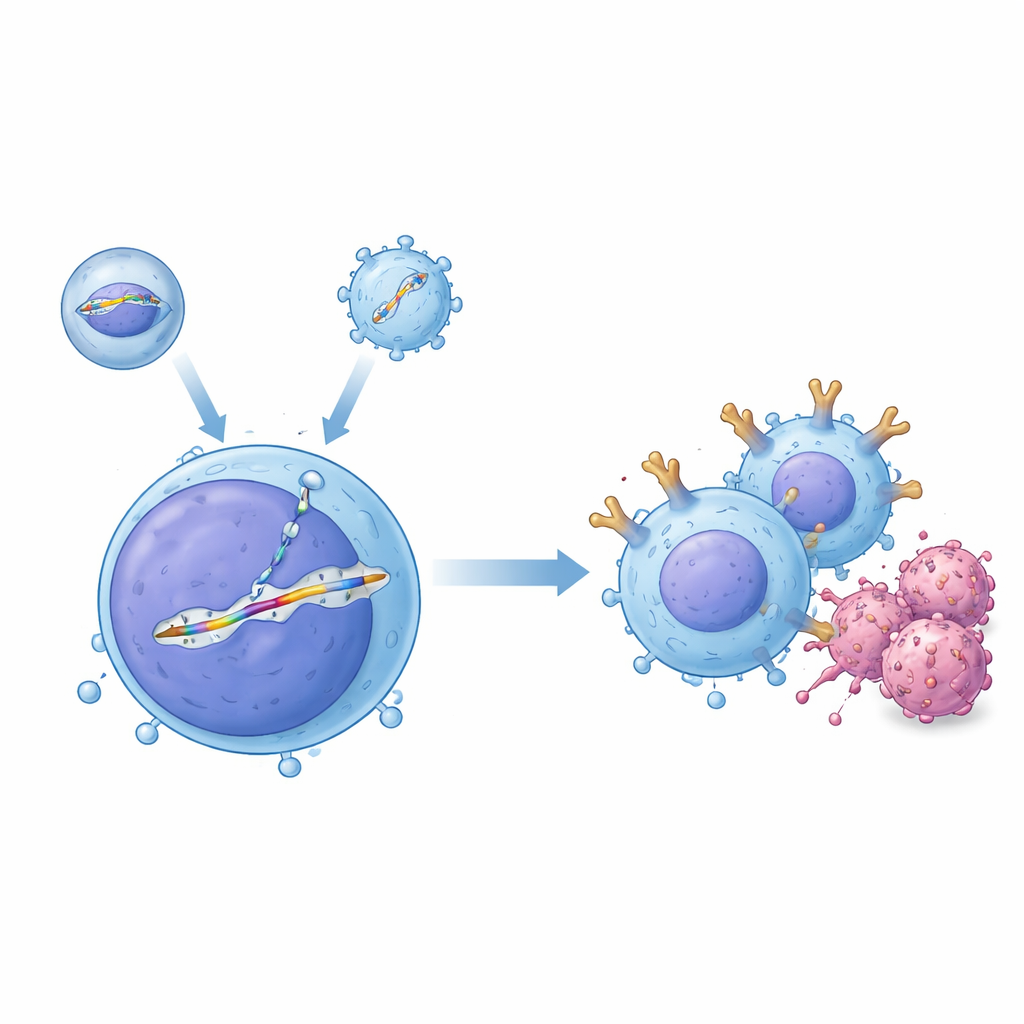
血流内で精密編集を行う二つのツール・システム
研究者らは、体内で協調して働く「二つのベクター」送達システムを作成しました。一つはエンベロープ化された送達体と呼ばれるツールで、T細胞のDNA中の特定部位を切断するようプログラムされたCRISPR–Cas9遺伝子編集タンパク質を運びます。もう一つはアデノ随伴ウイルス(AAV)由来のツールで、TRACとして知られるT細胞受容体遺伝子の選ばれた場所に導く配列で挟まれたCARの設計図を含む一致するDNAテンプレートを運びます。両方が同じ細胞に到達すると、切断部はテンプレートからのコピーで修復され、プロモーターを持たないCARカセットがTRACの自然なオン/オフスイッチの制御下にきれいに挿入されます。ヒトT細胞を用いた試験管内実験では、この組み合わせにより高割合の正確に編集された細胞が得られ、編集されたT細胞がB細胞白血病細胞を効率的に殺せることを示しました。
T細胞を標的にし、誤った標的を避けるための送達体設計
生体内でこれらの遺伝的ツールを安全に届けることは、試験管内よりはるかに難しく、血液には抗体や避けるべき多くの細胞種が含まれています。これを克服するため、チームはAAVカプシド変異体(AAV-hT7と呼ぶ)を進化させ、人血清の存在下でも活性を保ち、幹細胞やがん細胞よりもヒトT細胞を好むようにしました。CRISPRスクリーニングにより、CD7という表面タンパク質がこのベクターのT細胞侵入性に強く影響することが見いだされ、その特異性の説明に役立ちました。同時に、彼らはエンベロープ化送達体を再設計し、通常のウイルス被膜が通常結合する受容体に結合できないよう変異を入れ、その代わりにT細胞の目印であるCD3を認識する抗体断片で飾りました。この二重標的化戦略は粒子をT細胞へ誘導するだけでなく、それらを一時的に活性化し、より多くの細胞を正確なDNA修復と安定したCARカセット挿入を有利にする細胞周期状態に押し込みました。
白血病、骨髄腫、固形腫瘍を制御する生体内生成CAR T細胞
最適化されたペア(CD3標的粒子とAAV-hT7 DNA運搬体)を手に、科学者たちはいくつかのヒト化マウスモデルでこのアプローチを検証しました。ヒト血球を移植したマウスでは、二つのベクターを静脈内に一回投与するだけで、目的のTRAC部位に最大で約5分の1のT細胞がCAR T細胞に変換され、正常B細胞が消失しました。これは抗CD19 CARの活性の特徴です。攻撃的な白血病モデルでは、この生体内で生成されたCAR T集団は速やかに増殖し、腫瘍を消失させ、しばしば後の腫瘍再挑戦に対して保護を示しました。生体内レンチウイルスCAR送達と正面から比較すると、TRAC標的法は各細胞でより均一なCARレベル、より速いT細胞増殖、そして総合的に優れた腫瘍制御を示しました。チームは次に、骨髄腫マーカーであるBCMAや多くの固形腫瘍に見られる蛋白質B7-H3を標的とするCAR設計に切り替え、複数の骨髄腫および肉腫モデルで強い応答を示し、多くの動物で再挑戦後にも持続的な制御を確認しました。
将来のがん治療にとっての意味
専門外の読者への要点は、著者らが体そのものを設計された免疫細胞のためのプログラム可能な工場に変えたことです。CRISPR機構と精巧に設計されたDNAテンプレートを同時に届け、両方をT細胞だけに誘導することで、生体内でヒトT細胞を正確かつ安定的に「配線し直す」ことに成功しました。こうして新たに作られたCAR T細胞は、いくつかのがんモデルで、現在の試験管内で育てたものに匹敵するかそれ以上の挙動を示しました。安全性の実証、用量管理、人への移行にはなお多くの作業が残されていますが、この研究は、患者自身の免疫系に指示を与えて血液がん—そして可能性としていくつかの固形腫瘍—と戦わせるオフ・ザ・シェルフ注射へと続く現実的な道筋を示しています。
引用: Nyberg, W.A., Bernard, PL., Ngo, W. et al. In vivo site-specific engineering to reprogram T cells. Nature 652, 712–721 (2026). https://doi.org/10.1038/s41586-026-10235-x
キーワード: CAR T細胞, 生体内遺伝子編集, CRISPR, がん免疫療法, ウイルスベクター