Clear Sky Science · zh
生物分子凝聚体种子预组装驱动RSV复制
为何某些病毒颗粒能抢得先机
呼吸道合胞病毒(RSV)是婴幼儿、老年人和免疫功能低下者肺部感染的重要病原体。本研究提出了一个看似简单但意义深远的问题:当单个RSV颗粒落在细胞上时,是什么决定了该感染会扩散开来还是悄然停滞?通过在活细胞中追踪单个病毒基因组,作者发现了病毒颗粒之间未曾察觉的差异,这些差异解释了为何有些感染会迅速爆发而另一些则熄火。
受感染细胞内的隐藏病毒小滴
进入细胞后,许多RNA病毒(包括RSV)会建立微小的、无膜的“病毒工厂”。这些类似液滴的结构浓缩了病毒成分,是新病毒基因组和蛋白合成的主要场所。但问题在于:这类液滴通常只有在蛋白质水平已经很高时才会形成,而在感染早期病毒蛋白很稀少。研究者使用先进的荧光显微技术,从vRNP(病毒核蛋白复合体)进入细胞的那一刻起追踪单个RSV基因组复合体。他们发现病毒工厂并非凭空出现;相反,它们由个别进入的vRNP逐渐膨胀并相互融合,最终长成更大的液滴。
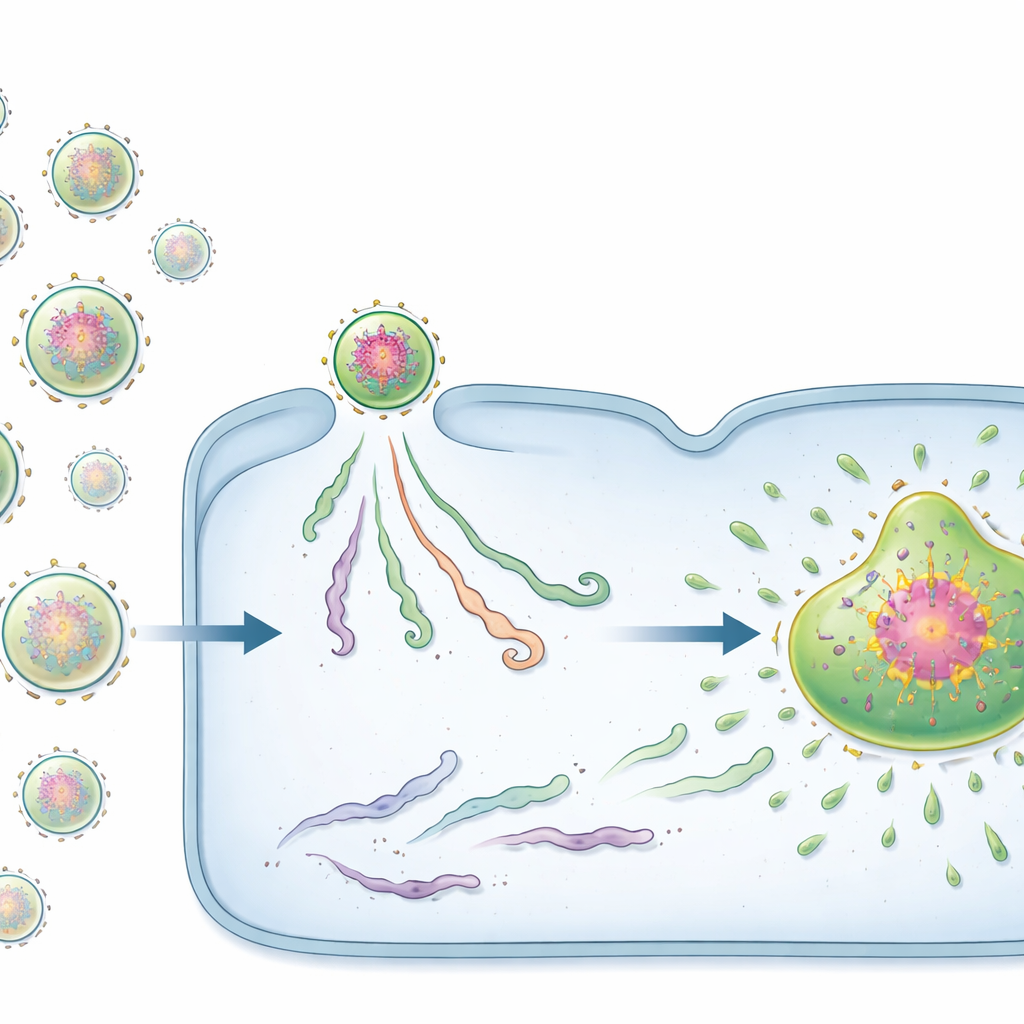
两类病毒启动者:种子与旅客
令人惊讶的是,并非所有进入的vRNP表现相同。借助专门设计的荧光探针,团队发现了两种不同状态。少数vRNP在基因组周围已经组装了致密的病毒蛋白簇。这些富含蛋白的复合体,作者称为预复制中心(PRC),充当了强力的病毒工厂“种子”。即便只有单个PRC感染一个细胞,几乎总能催生工厂并产生大量后代基因组。相反,大多数vRNP缺少这种预装蛋白网络,被称为被动vRNP。由被动vRNP发起的感染常常停滞:病毒物质保持小而孤立,既不形成病毒工厂也不产生后代基因组。
为何种子成功而旅客失败
通过实时测量病毒活性,作者证明PRC能迅速且以远高于被动vRNP的速率转录病毒基因。详尽的成像和生化分析揭示了原因。PRC在每个基因组上携带明显更多的关键病毒蛋白——尤其是聚合酶及其辅因子——即便在进入细胞之前也是如此。进入细胞质后,这些蛋白仍留在PRC上,而会从被动vRNP上脱落。PRC还像粘性支架一样吸引额外的病毒蛋白乃至其他vRNP。随着蛋白积累,PRC跨越了凝聚成液滴状病毒工厂所需的阈值,基因组复制在其中最终被激活。这形成了一个正反馈回路:更多蛋白使种子更有效,种子又捕获更多蛋白并迅速成长为工厂。
病毒颗粒之间的内在差异
研究还显示,从感染细胞释放的RSV颗粒并不全然相同。有些病毒体包装多个vRNP,且许多病毒体内部主要包含PRC或主要包含被动vRNP。富含PRC的病毒体在新细胞中发起有效感染的概率远高于其他病毒体。这种“病毒体异质性”在实验室菌株、临床分离株以及直接来自患者的病毒样本中均被观察到,表明这是RSV生物学的天然特征。每个颗粒内基因组的数量远不及是否至少含有一个PRC那样重要。因此,一小部分装备精良的颗粒可能推动了大多数成功感染,而其他则充当缺乏动力的旅客。
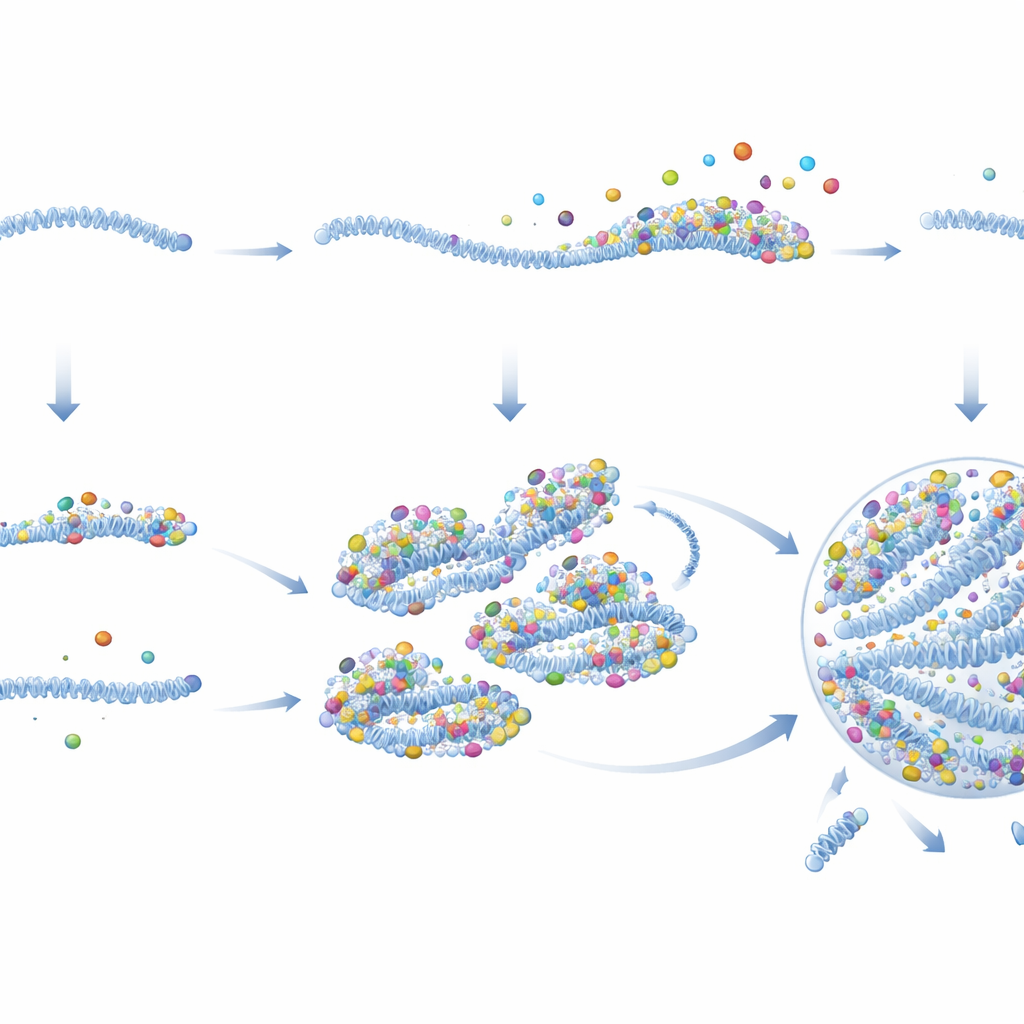
这项发现对感染以及其它领域的意义
简言之,作者得出结论:RSV通过在一些病毒体内出芽前预先组装富含蛋白的种子,解决了一个看似的先有鸡还是先有蛋问题——需要高蛋白水平来构建病毒工厂,但又需要工厂来产生蛋白。当这些被“播种”的基因组进入新细胞时,它们立即开始产生蛋白并聚集更多蛋白,迅速成核出病毒工厂并启动复制。相比之下,被动基因组很少能摆脱这种低活性状态,除非额外提供病毒蛋白。这项工作不仅阐明了为何RSV感染在细胞间差异巨大,也提示了新的策略:阻断这些种子或阻碍其凝聚能力的药物可能在感染的最初步骤就抑制病毒传播,而且类似原则可能也支配着许多其它与疾病相关的细胞内生物分子液滴的形成。
引用: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
关键词: 呼吸道合胞病毒, 病毒工厂, 生物分子凝聚体, 单病毒成像, 感染异质性